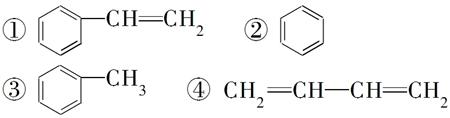2017内蒙古高一下学期人教版高中化学月考试卷
| 1. | 详细信息 |
|
下列物质的主要成分不是甲烷的是( ) A. 沼气 B. 油田气 C. 天然气 D. 水煤气
|
|
| 2. | 详细信息 |
|
下列物质中,在一定条件下能发生取代反应和加成反应,但不能使酸性高锰酸钾溶液褪色的是( ) A. 乙烷 B. 甲烷 C. 苯 D. 乙烯
|
|
| 3. | 详细信息 |
|
在C(s)+CO2(g)===2CO(g)的反应中,现采取下列措施: ①缩小体积,增大压强 ②增加碳的量 ③通入CO2 ④恒容下充入N2 ⑤恒压下充入N2能够使反应速率增大的措施是( ) A.①④ B.②③⑤ C.①③ D.①②④
|
|
| 4. | 详细信息 |
|
某有机物的名称为3,3,4,4四甲基己烷,它的结构简式为( ) A.(CH3)2CHCH2CH2C(CH3)3 B. CH3CH2C(CH3)2CH2C(CH3)2CH2CH3 C. CH3CH2C(CH3)2C(CH
|
|
| 5. | 详细信息 |
|
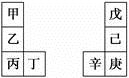
甲~辛等元素在周期表中的相对位置如下表。甲与戊的原子序数相差3,戊的一种单质是自然界硬度最大的物质,丁与辛属同周期元素,下列判断正确的是( )
B. 气态氢化物的热稳定性:戊>己>庚 C. 乙所在周期元素中,其简单离子的半径最大 D. 乙的单质在空气中燃烧生成的化合物只含离子键
|
|
| 6. | 详细信息 |
|
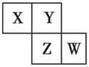
A. 原子半径:W>Z>Y>X B. 最高价氧化物对应水化物的酸性:Z>W>X C. 氢化物的稳定性:X>Y>Z D. 四种元素的单质中,Z单质的熔、沸点最高
|
|
| 7. | 详细信息 |
|
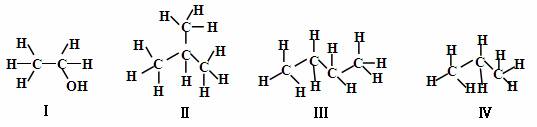
同分异构现象是造成有机物数目繁多的原因之一。下列物质互为同分异构体的是( )
A.Ⅰ和Ⅱ B.Ⅱ和Ⅲ C.Ⅲ和Ⅳ D.Ⅰ和Ⅳ
|
|
| 8. | 详细信息 |
|
可用分液漏斗分离的一组混合物是( ) A. 硝基苯和酒精 B. 溴苯和溴 C. 甲苯和苯 D. 硝基苯和水
|
|
| 9. | 详细信息 |
|
14C是碳的一种同位素,NA为阿伏加德罗常数,下列说法不正确的是( ) ①1 mol 14CH4分子中所含中子数为8NA ②7 g 14C原子形成的石墨中所含质子数为3NA ③17 g 甲基(-14CH3)所含电子数为8NA ④常温常压下22 A.①② B.①③ C.①②③ D.③④
|
|
| 10. | 详细信息 |
|
对可逆反应4NH3(g)+5O2(g) A.达到化学平衡时,4v正(O2)=5v逆(NO) B.若单位时间内生成x mol NO的同时,消耗x mol NH3,则反应达到平衡状态 C.达到化学平衡时,若增加容器体积,则正反应速率减小,逆反应速率增大 D.化学反应速率关系是:2v正(NH3)=3v正(H2O)
|
|
| 11. | 详细信息 |
|
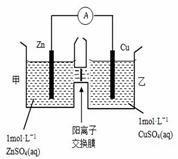
A. 铜电极上发生氧化反应 B. B. 电池工作一段时间后,甲池的c(SO42-)减小 C. 电池工作一段时间后,乙池溶液的总质量增加 D. 电子流向为Zn→导线→Cu→溶液→Zn,形成闭合回路
|
|
| 12. | 详细信息 |
|
下列反应中属于加成反应的是( ) A. 乙烯使溴水褪色 B. 将苯滴入溴水中,振荡后水层接近无色 C. 乙烯使酸性KMnO4溶液褪色 D. 甲烷与氯气混合,黄绿色消失
|
|
| 13. | 详细信息 |
|
实验室用液溴和苯反应制取溴苯,得到粗溴苯后,要用如下操作精制:①蒸馏;②水洗;③用干燥剂干燥;④10%NaOH溶液洗;⑤水洗,正确的操作顺序是( ) A. ①②③④⑤ B. ②④⑤③① C. ④②③①⑤ D. ②④①⑤③
|
|
| 14. | 详细信息 |
|
下列关于苯的说法中,正确的是:( ) A. 苯分子为平面正六边形结构,6个碳原子之间的键完全相同 B. 从苯的结构看,分子中含有单、双键,所以能使酸性高锰酸钾溶液和溴的四氯化碳溶液因反应而褪色 C. 在催化剂存在下,苯能与溴水发生取代反应,生成溴苯 D. 苯是一种密度比水大,不溶于水的有特殊气味的无色液体
|
|
| 15. | 详细信息 |
|
使1mol乙烯与氯气发生完全加成反应,然后使该加成反应的产物与氯气在光照的条件下发生取代反应,则消耗的氯气的总的物质的量是( ) A. 3mol B. 4mol C. 5mol D. 6mol
|
|
| 16. | 详细信息 |
|
物质的量均为1 mol的下列有机物,在适当条件下与H2充分加成后,需氢气的物质的量由多到少的顺序正确的是( )
⑤乙烯 A. ①>②>③>④>⑤ B. ①>②=③>④>⑤ D. ①>③>②>④>⑤
|
|
| 17. | 详细信息 |
|
下列关于有机物 A. 分子中9个碳原子可能位于同一平面内 B. 该物质能使酸性KMnO4溶液褪色 C. 1mol该有机物可与4molH2发生加成反应 D. 该物质能使溴水褪色是因
|
|
| 18. | 详细信息 |
|
下列关于甲烷性质叙述中正确的是( ) A. 甲烷能使酸性KMnO4溶液的紫色褪去 B. 甲烷与足量氯气在光照时有机产物只有 C. 甲烷是一种无色无味、难溶于水的气体 D. 等物质的量的甲烷和乙烷(C2H6)分别完全燃烧时,甲烷消耗的氧气多
|
|
| 19. | 详细信息 |
|
将1.0体积乙烷和乙烯的混合气体在氧气中充分燃烧,生成2.0体积的CO2和2.6体积的水蒸气(同温同压下测定)。则混合物中烷烃和烯烃的体积 A.3∶1 B.1∶3 C.2∶3 D.3∶2
|
|
| 20. | 详细信息 |
|
.下列分子式只能表示一种物质的是 ( ) A. C3H7Cl B. C4
|
|
| 21. | 详细信息 |
|
A、B、C、D、E、F、G为6种短周期主族元素,其原子序数依次增大。A、C可形成A2C和A2C2两种化合物,B的最高正化合价与最低负化合价的绝对值之差为2,D和A同主族,E是地壳中含量最高的金 (1)G的元素名称是__________,在元素周期表中的位置是__________。 (2)C、D、E、F简单离子的半径由大到小的顺序是__________(填离子符号)。 (3)工业上冶炼E的单质反应的化学方程式是__________。 (4)由上述6种元素中的4种元素组成的化合物X,X既能与热的NaOH溶液反应,也
|
|
| 22. | 详细信息 |
|
分别为0.6mol和0.5mol的A、B两种气体,充入0.4L密闭容器中发生反应:3A( (1)m值为__________________; (2)B的转化率为_______________________; (3)平衡时容器内物质的总物质的量为________________________; (4)在四种不同的条件下测定得到以下反应速率,其中表示的反应速率最快的是______ ①v(A)=0.5 mol·L-1·min-1 ② v(B)=0.2 mol·L-1·min-1 ③ v(C)=0.3 mol·L-1·min-1 ④ v(D)=0.1 mol·L-1·min-1
|
|
| 23. | 详细信息 |
|
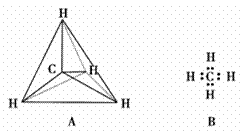
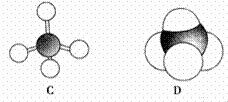
下列各图均能表示甲烷的分子结构
(1)甲烷的球棍模型是________,甲烷的电子式是__________ (填序号)。 (2)写出甲烷与氯气发生反应的化学方程式_____________(只写第一步),该反应的反应类型是________________。 (3)相对分子质量为72的烷烃的分子式是_______________。 (4)甲烷与丙烷互为(______) A. 同位素 B. 同素异形体 C. 同系物 D. 同分异构体
|
|
| 24. | 详细信息 |
|
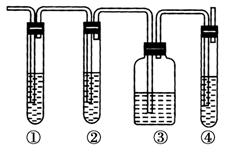
实验室制取乙烯,常因温度过高而使乙醇和浓硫酸反应生成少量的二氧化硫。有人设计下图所示装置进行实验以确认上述混合气体中有乙烯和二氧化硫。试回答下列问题:
(1)图中①、②、③、④装置可盛放的试剂是(填序号):①________;②________; ③________;④________。 A.品红溶液 B.氢氧化钠溶液 C.浓硫酸 D.高锰酸钾酸性溶液 (2)能说明二氧化硫气体存在的现象是_____________________。 (3)使用装置②的目的是_________________________________。 (4)使用装置③的目的是_____________ (5)确定含有乙烯的现象是____________________________
|
|
- 2019-2020年高一下半年期中考试化学题免费试卷(黑龙江省哈尔滨市第三十二中学)
- 安徽高二化学2019年后半期期末考试试卷带解析及答案
- 成都市高三化学下册月考试卷模拟考试训练
- 高二上期期中考试化学题免费在线检测(2019-2020年黑龙江省大兴安岭漠河县高级中学)
- 2019-2020年高二上册第一次月考化学考试完整版(江西省南昌市第二中学)
- 鲁科版选择性必修1第2章化学反应的方向、限度与速率微项目探讨如何利用工业废气中的二氧化碳合成甲醇--化学反应选择与反应条
- 2015-2016年高一下半年期中考试化学考题(上海市金山中学)
- 2019-2020年高二上半期期中考试化学考题(福建省厦门外国语学校)