天津市和平区2016-2017学年高二上学期化学期末考试试卷
天津市和平区2016-2017学年高二上学期化学期末考试试卷
教材版本:化学
试卷分类:化学高二上学期
试卷大小:1.0 MB
文件类型:.doc 或 .pdf 或 .zip
发布时间:2024-05-01
授权方式:免费下载
下载地址:点此下载
教材版本:化学
试卷分类:化学高二上学期
试卷大小:1.0 MB
文件类型:.doc 或 .pdf 或 .zip
发布时间:2024-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 单选题 | |
|
25℃时,水的电离达到平衡:H2O⇌H++OH﹣△H>0,下列叙述正确的是( )
A . 向水中加入氨水,平衡逆向移动,c(OH﹣)降低
B . 向水中加入少量固体硫酸氢钠,c(H+)增大,KW不变
C . 向水中加入少量固体CH3COONa,平衡逆向移动,c(H+)降低
D . 将水加热,KW增大,pH不变
|
|
| 2. 单选题 | |
|
已知醋酸达到电离平衡后,改变某条件电离平衡向正反应方向移动,则下列说法正确的是( )
A . 实现该变化的只能是升高温度
B . 溶液的导电能力一定变强
C . 溶液的pH一定减小
D . 发生电离的分子总数增多
|
|
| 3. 单选题 | |
|
下列叙述正确的是( )
A . 用湿润的pH试纸测溶液的pH一定会有误差
B . 用标准盐酸溶液滴定未知浓度的NaOH溶液时,用待测溶液润洗锥形瓶
C . 用酸式滴定管量取酸性高锰酸钾溶液5.10mL
D . 用标准盐酸溶液滴定未知浓度NaOH溶液的过程中不慎将锥形瓶中的溶液溅出,会使测得的NaOH溶液的浓度偏大
|
|
| 4. 单选题 | |
|
常温下有体积相同的四种溶液:①pH=3的CH3COOH溶液 ②pH=3的盐酸 ③pH=11的氨水 ④pH=11的NaOH溶液.下列说法正确的是( )
A . 若将四种溶液稀释100倍,溶液pH大小顺序:③>④>①>②
B . ③和④分别用等浓度的硫酸溶液中和,消耗硫酸溶液的体积:③=④
C . ①与②分别与足量镁粉反应,生成H2的量:①<②
D . ②和③混合,所得混合溶液的pH大于7
|
|
| 5. 单选题 | |
|
25℃时,下列有关溶液中粒子的物质的量浓度关系正确的是( )
A . 0.1mol/LCH3COONa与0.1mol/LHCl溶液等体积混合:c(Na+)=c(Cl﹣)>c(OH﹣)>cCH3COO﹣)
B . 0.1mol/LNH4Cl与0.1mol/L氨水等体积混合(pH>7):c(NH3•H2O)>c(NH4+)>c(Cl﹣)>c(OH﹣)
C . 0.1mol/LNa2CO3与0.1mol/L NaHCO3溶液等体积混合:
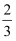 c(Na+)=c(CO32﹣)+c(HCO3﹣)+c(H2CO3)
D . 0.1mol/LNa2C2O4与0.1mol/LHCl溶液等体积混合(H2C2O4为二元弱酸):2c(C2O42﹣)+c(HC2O4﹣)+c(OH﹣)=c(Na+)+c(H+) c(Na+)=c(CO32﹣)+c(HCO3﹣)+c(H2CO3)
D . 0.1mol/LNa2C2O4与0.1mol/LHCl溶液等体积混合(H2C2O4为二元弱酸):2c(C2O42﹣)+c(HC2O4﹣)+c(OH﹣)=c(Na+)+c(H+)
|
|
| 6. 单选题 | |
|
在一定条件下,Na2CO3溶液存在水解平衡:CO32﹣+H2O⇌HCO3﹣+OH﹣ . 下列说法正确的是( )
A . 稀释溶液,水解平衡常数增大
B . 通入CO2 , 平衡朝正反应方向移动
C . 升高温度,
 减小
D . 加入NaOH固体,溶液pH减小 减小
D . 加入NaOH固体,溶液pH减小
|
|
| 7. 单选题 | |
|
关于原电池和电解池的叙述正确的是( )
A . 原电池中失去电子的电极为阴极
B . 原电池的负极、电解池的阳极都发生氧化反应
C . 原电池的两极一定是由活动性不同的两种金属组成
D . 电解时电解池的阴极一定是阴离子放电
|
|
| 8. 单选题 | |
|
下列金属防腐的措施中,使用外加电流的阴极保护法的是( )
A . 水中的钢闸门连接电源的负极
B . 金属护拦表面涂漆
C . 汽车底盘喷涂高分子膜
D . 地下钢管连接镁块
|
|
| 9. 单选题 | |
|
下列有关沉淀溶解平衡的说法中,正确的是( )
A . 在AgCl的沉淀溶解平衡体系中,加入蒸馏水,Ksp(AgCl)增大
B . 在CaCO3的沉淀溶解平衡体系中,加入稀盐酸,平衡不移动
C . 可直接根据Ksp的数值大小比较难溶物在水中的溶解度大小
D . 25℃时,KSP(AgCl)>KSP(AgI),向AgCl的悬浊液中加入KI固体,有黄色沉淀生成
|
|
| 10. 单选题 | |
|
铜锌原电池(如图)工作时,以下说法正确的是( )
①电子流动方向从Zn﹣灯泡﹣Cu﹣盐桥;②Zn电极的质量减轻Cu电极的质量增重;③盐桥中的K+移向CuSO4溶液;④将锌片浸入硫酸铜溶液发生的化学反应与该电池反应相同为:Zn+Cu2+═Zn2++Cu;⑤Zn电极失电子发生还原反应.
A . ①②③
B . ②④⑤
C . ②③④
D . ③④⑤
|
|
高中化学 试卷推荐
- 人教(新课标)高中化学一轮复习:专题7常见的有机化合物
- 广东省汕头市2017-2018学年高三理综-化学第一次模拟考试试卷
- 2015-2016学年江西省赣州市于都三中高二下学期第一次月考化学试卷
- 人教版化学高二选修2第二单元课题2海水的综合利用同步练习
- 湖北省孝感市八校教学联盟2017-2018学年高一下学期化学期末考试试卷
- 2017年高考化学备考复习专题十二:重要的有机化合物
- 专题12:氮族元素及其化合物
- 广东省茂名市高州中学2016-2017学年高二上学期化学期中考试试卷(理科)
- 江苏省徐州市2019-2020学年高二下学期化学期末考试试卷
- 2016-2017学年辽宁省大连市高二上学期期末化学试卷(文科)
- 2015年海南省保亭中学高考化学模拟试卷(二)
- 辽宁省辽南协作校2020年高考化学一模试卷
最近更新




