河北省保定市定州市2021-2022学年高二上学期期中考试化学试题
河北省保定市定州市2021-2022学年高二上学期期中考试化学试题
教材版本:化学
试卷分类:化学高二上学期
试卷大小:1.0 MB
文件类型:.doc 或 .pdf 或 .zip
发布时间:2024-05-01
授权方式:免费下载
下载地址:点此下载
教材版本:化学
试卷分类:化学高二上学期
试卷大小:1.0 MB
文件类型:.doc 或 .pdf 或 .zip
发布时间:2024-05-01
授权方式:免费下载
下载地址:点此下载
以下为试卷部分试题预览
| 1. 单选题 | |
|
下列对化学平衡移动的分析中,错误的是( )
①已达平衡的反应C(s)+H2O(g)
A . ①④
B . ①②③
C . ②③④
D . ①②③④
|
|
| 2. 单选题 | |
|
3 mol H2和1 mol N2放入密闭容器中,使用催化剂发生反应:N2+3H2
 2NH3 , 从反应开始到平衡过程中,不可能出现的是( ) 2NH3 , 从反应开始到平衡过程中,不可能出现的是( )
A . 2 mol NH3
B . 0.5 mol NH3
C . 0.9 mol N2
D . H2和NH3物质的量相等
|
|
| 3. 单选题 | |
|
温度为T℃,向体积不等的恒容密闭容器中分别加入足量活性炭和1molNO2 , 发生反应:2C(s)+2NO2(g)
 N2(g)+2CO2(g)。反应相同时间,测得各容器中NO2的转化率与容器体积的关系如图所示。 N2(g)+2CO2(g)。反应相同时间,测得各容器中NO2的转化率与容器体积的关系如图所示。
下列说法错误的是( )
A . T℃时,该反应的化学平衡常数为Kc=
 mol·L-1
B . 由图可知,c点V正>V逆
C . 向a点平衡体系中充入一定量的NO2 , 达到平衡时,NO2的转化率比原平衡小
D . 容器内的压强:pa∶pb=6∶7 mol·L-1
B . 由图可知,c点V正>V逆
C . 向a点平衡体系中充入一定量的NO2 , 达到平衡时,NO2的转化率比原平衡小
D . 容器内的压强:pa∶pb=6∶7
|
|
| 4. 单选题 | |
|
将浓度均为
 的气体 的气体 和 和 放在某恒容密闭容器中,反应后生成Z,平衡时测得 放在某恒容密闭容器中,反应后生成Z,平衡时测得 , ,  , ,  , 则Z的分子式为( ) , 则Z的分子式为( )
A .
 B .
B .  C .
C .  D .
D . 
|
|
| 5. 单选题 | |
|
据报道,加拿大科学家发明了一种特殊的“电催化剂”,该新型“电催化剂”是一种用于电解器中催化水分解为氢气与氧气的多孔金属氧化物固体。下列有关该催化剂的说法正确的是( )
A . 使用该催化剂,能减小水分解反应的焓变
B . 该催化剂的使用可提高水的分解率
C . 金属氧化物固体的多孔结构,可提高催化剂的催化效率
D . 该催化剂还可以作其他所有液态化合物分解反应的催化剂
|
|
| 6. 单选题 | |
|
下列关于化学反应的自发性和进行方向的说法正确的是( )
A . 非自发反应在任何条件下都不能发生
B . —定温度下,反应 Mg(l) +Cl2(g)==MgCl2(l)的 △H<0, △S<0
C . 由∆G=△H – T△S可知,所有放热反应都能自发进行
D . 只有不需要任何条件就能够自动进行的过程才是自发过程
|
|
| 7. 单选题 | |
|
已知下列反应的平衡常数:①S(s)+O2(g)
 SO2(g),K1;②H2(g)+S(s) SO2(g),K1;②H2(g)+S(s) H2S(g),K2。则反应H2(g)+SO2(g) H2S(g),K2。则反应H2(g)+SO2(g) O2(g)+H2S(g)的平衡常数是( ) O2(g)+H2S(g)的平衡常数是( )
A . K1-K2
B . K2-K1
C .
 D .
D . 
|
|
| 8. 单选题 | |
|
已知某可逆反应在密闭容器中进行:A(g)+2B(g)
 3C(g)+D(s)ΔH<0,如图中曲线b代表一定条件下A物质的转化率随时间变化的曲线。若使曲线b变为曲线a,可采取的措施是( ) 3C(g)+D(s)ΔH<0,如图中曲线b代表一定条件下A物质的转化率随时间变化的曲线。若使曲线b变为曲线a,可采取的措施是( )
①增大A的浓度②缩小容器的容积③增大B的浓度④升高温度⑤加入合适的催化剂
A . ①
B . ②④
C . ②⑤
D . ②③
|
|
| 9. 单选题 | |
|
在一定条件下,反应
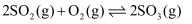 达到了平衡状态,改变某一反应条件,发生下列变化,其中可确定该平衡一定发生移动的是( ) 达到了平衡状态,改变某一反应条件,发生下列变化,其中可确定该平衡一定发生移动的是( )
A . v(SO2)增大
B . v(SO3)减小
C . O2的物质的量分数发生变化
D . SO3的质量不变
|
|
| 10. 单选题 | |
|
某同学设计如图所示装置,探究化学反应中的能量变化。
下列判断正确的是( )
A . 由实验可知,(a)(b)(c)所涉及的反应都是放热反应
B . 将实验(a)中的铝片更换为等质量的铝粉后释放出的热量有所增加
C . 实验(c)中将玻璃搅拌器改为铁质搅拌棒对实验结果没有影响
D . 若用NaOH固体测定中和热,所测定的∆H偏小
|
|
高中化学 试卷推荐
- 吉林省长白实验中学2020-2021学年高一下学期化学第一次月考试卷
- 四川省遂宁市2022届高三第二次诊断性考试(二模)理综化学试题
- 辽宁省沈阳市郊联体2020-2021学年高三上学期化学期中考试试卷
- 安徽省河南省皖豫名校联盟体2022届高三下学期第三次考试理综化学试题
- 四川省凉山州2021年高考化学二模试卷
- 广东省深圳市宝安区2020-2021学年高一上学期化学期末考试试卷
- 山东省日照五莲县2020-2021学年高二下学期化学期中考试试卷
- 浙江省温州市苍南县金乡卫城中学2020-2021学年高二下学期化学开学考试试卷
- 四川省南充市2022届高三 适应性考试(二模)理综化学试题
- 黑龙江省牡丹江市海林市朝鲜族高中2020-2021学年高一下学期化学5月月考试卷
- 广东省深圳市2021年高考化学二模(4月)试卷
- 安徽省马鞍山市2020-2021学年高一下学期期末考试化学试题
最近更新






