第四章 生命之源——水 知识点题库
写出下列反应的化学方程式:
①碳在氧气中充分燃烧。
②铁丝在氧气中燃烧。
③加热铜粉。
④双氧水和二氧化锰的混合物。
⑤实验室制取二氧化碳的反应原理。
⑥向澄清的石灰水中通入二氧化碳气体的反应
水是生命之源,我们应该了解水、爱护水。
-
(1) 从江河等水源取出的水经静置、沉淀、等操作除去水中不溶性杂质,然后加入活性炭,利用活性炭的吸附性,除去异味;
-
(2) 可用鉴别生活用水是硬水还是软水,生活中常用的方法降低水的硬度。
金属在生产生活中有广泛应用。
-
(1) 汽车电路中的导线一般为铜芯线,这是利用了金属铜的延展性和性。
-
(2) 将铜锌合金与铜片相互刻画,在铜片表面留下明显划痕,说明铜锌合金的硬度铜的硬度(填“大于”或“小于”)。
-
(3) 铁粉可作食品脱氧剂,其保鲜原理与铁生锈相同,铁生锈的条件是与接触。
-
(4) 向一定量的硝酸银、硝酸铝和硝酸铜的混合溶液中加入一定量的锌,溶液质量与加入锌的质量关系如图所示。

①A点所发生反应的化学方程式为。
②B点对应的溶液中含有的溶质为(填化学式)。
③当加入锌的质量为m3g时,过滤后,得到的固体中含有(填化学式)。
-
(5) 一氧化碳具有还原性,常用于冶炼金属。某同学取20g氧化铁粉末与一氧化碳反应一段时间后,称量剩余固体的质量为15.2g,则该反应中生成的CO2的质量为g。
在宏观、微观与符号之间建立联系是化学学科的特点。天然气是广泛使用的燃料,其主要成分还可能发生的化学反应微观示意图如下:

-
(1) 写出乙物质的化学式。
-
(2) 请写出工业上用丙物质从赤铁矿中冶炼铁的反应化学方程式。
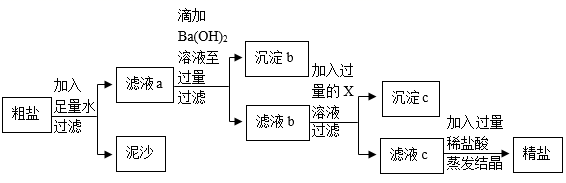
重庆多地曾出现过盐井,从天然盐井中获取粗盐(含泥沙、CaCl2、MgCl2、Na2SO4等杂质)为了除去以上杂质得到精盐,小明设计如下实验。
(提示)杂质含量较少,不考虑微溶物形成沉淀
-
(1) 过滤操作中用到的玻璃仪器有烧杯、玻璃棒和。
-
(2) 沉淀b所含物质为 Mg(OH)2和。
-
(3) 物质X是。
-
(4) 滤液c中加入稀盐酸后发生中和反应的化学方程式为。
-
(5) 为了证明滴加的 Ba(OH)2溶液已过量,取少许上层清液于试管中加入一种试剂即可。下列物质的溶液能达到实验目的的有______。A . Ba(OH)2 B . K2CO3 C . Na2SO4 D . KCl
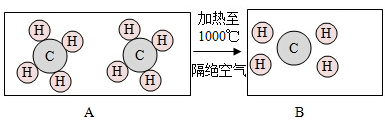
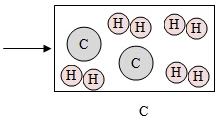
下图是甲烷在一定条件下发生分解的微观模拟图:
-
(1) 在图B中将相关粒子图形补充完整;
-
(2) A是化合物,你判断的微观依据是
-
(3) 结合该图示解释由A到B变化的实质是
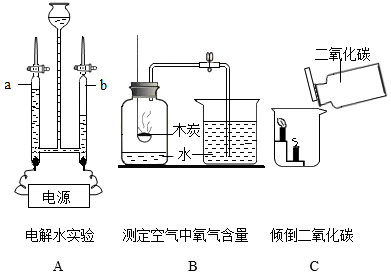
化学是以实验为基础的科学,实验是科学探究的重要手段。根据图示回答下列问题:

-
(1) A实验中,打开活塞,用分别接近a、b玻璃尖嘴口处,检验产生的气体。
-
(2) B实验(填“能”或“不能”)测定空气中氧气的含量。
-
(3) C实验中,能观察到的实验现象是。
-
(4) D实验过程中小气球的变化是,如果将红磷直接放在锥形瓶底部,可能造成的后果是。
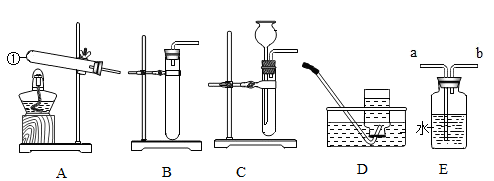
图是实验室里常用的实验装置,回答问题。
-
(1) 写出标号①的仪器名称;
-
(2) 实验室用H2O2溶液和MnO2制 取并用排水法收集O2。
①最好选用的气体发生装置是(选填“A”、“B”或“C”);
②若O2收集满瓶,会观察到的现象是;
-
(3) 医院给危重病人吸氧时,用到了类似图E的装置。
①与病人呼吸罩相连的导管是端(选填“a”或“b”);
②E装置中水的作用是(回答任意一点)。
-
(4) 实验室用125g石灰石与足量稀盐酸充分反应制得44g CO2 , 计算该石灰石中含CaCO3的质量分数。将计算步骤补充完整。
解:设该石灰石中含CaCO3的质量为x。


列出比例式求解
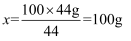
该石灰石含CaCO3的质量分数为。
答(略)。
我省铝土矿储量居全国之首,铝土矿的主要成分是Al2O3 , 还含有Fe2O3、SiO2等杂质。工业上从铝土矿中提取Al可采用下图所示工艺流程。(已知:SiO2不与盐酸反应部分生成物与反应条件已省略。)
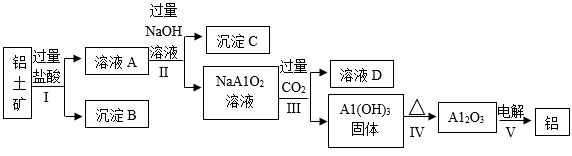
请回答下列问题:
-
(1) 步骤Ⅰ中发生反应的化学方程式是(写一个),溶液A中的阳离子是。
-
(2) 沉淀C是,将沉淀C与NaAlO2溶液分离的操作是。
-
(3) 步骤Ⅲ中发生的反应是:
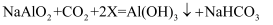 ,其中X的化学式是。
,其中X的化学式是。
-
(4) 步骤Ⅴ中发生了分解反应,除铝外,另一种生成物是。
水是生命之源,下列有关水的说法错误的是( )
A . 煮沸能降低水的硬度
B . 氢氧化钠固体溶于水时,溶液温度升高
C . 电解水时负极产生氧气
D . 用肥皂水鉴别硬水和软水
水是一种宝贵的自然资源,下列有关水的说法正确的是( )
A . 水由氢气和氧气组成
B . 生活中可用煮沸的方法降低水的硬度
C . 河水经沉淀、过滤、吸附,净化成蒸馏水
D . 电解水实验中产生O2和H2的体积比为2:1
逻辑推理是化学常用的思维方法。下列推理正确的是( )
A . 单质由同种元素组成,所以由同种元素组成物质一定是单质
B . 阳离子是带正电荷的粒子,所以带正电荷的粒子一定是阳离子
C . 由同种分子构成物质属于纯净物,所以纯净物都是由同种分子构成的
D . 氧气是由氧元素组成的,所以制取氧气的反应物中一定含有氧元素
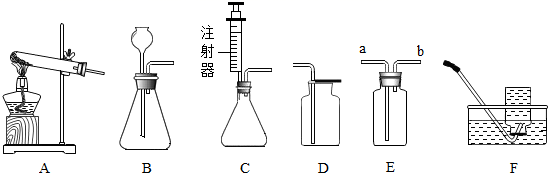
如图所示是实验室制取气体的常用装置。请回答下列问题:
-
(1) 实验室用高锰酸钾制取干燥的氧气应选和(填字母)。
-
(2) 可用C装置制取氧气,写出其方程式;C装置的优点是。
-
(3) 欲使用装置E用排空气法收集二氧化碳,则气体应从(填“a”或“b”)端通入气体;欲使用装置E用排水法收集氧气,操作是先,再从(填“a”或“b”)端通入气体。
-
(4) 为测定石灰石样品中碳酸钙的质量分数。小明取了100g石灰石样品放入烧杯中,加入稀盐酸至不再产生气泡为止(石灰石中杂质不溶于水也不反应),放出气体的质量为4.4g。请计算该石灰石样品中碳酸钙的质量分数。
化学与生活、生产、科技发展息息相关。
-
(1) 硅酸钠(Na2SiO3)可用作黏合剂和防火材料,其中Si元素的化合价为。
-
(2) 汽车是重要的交通工具,为了降低污染可以使用电动车,请完成铅酸电池充电反应的方程式:2PbSO4 + 2H2O
 Pb + 2H2SO4 +。
Pb + 2H2SO4 +。
-
(3) 2020年12月3日,我国“嫦娥五号”成功发射,显示我国科技实力的飞速发展。我国空间站“天宫”内的“空气”与地球上的空气组成基本一致,已知同温同压下,相同体积的气体含有相同数目的分子,“空气”中O2与N2的分子个数比约为。
-
(4) Cu能与空气中的、(写出其中两种物质的化学式)发生化合反应生成“铜锈”[主要成分为Cu2(OH)2CO3]。
-
(5) 一定条件下,CO2和H2反应生成CH4和H2O,见下图。

①该反应的化学方程式是。
②从微观角度分析,A图中的物质属于混合物的原因是。
③请在B图中将该反应的微观粒子补充完整。
绿色化学又称环境友好化学,下列做法符合绿色化学理念的是( )
A . 工厂的废液未经处理便排放到河里
B . 对生活垃圾分类,并进行无害化处理和回收再利用
C . 为了减少白色污染,严禁使用塑料类制品
D . 为了食品安全,在食品加工制作过程中禁止添加任何添加剂
某新型锂离子电池的工作原理为: , 其中物质Y为( )
, 其中物质Y为( )
 , 其中物质Y为( )
, 其中物质Y为( )
A . C
B . Co
C . CO2
D . Li2O
化学是在分子、原子的层次上研究物质的科学。如图是某化学反应的微观示意图,下列有关说法正确的是( )
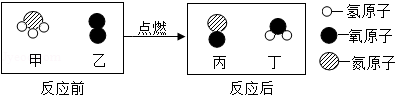
A . 该反应中含氧元素的化合物有3种
B . 反应前后各元素的化合价均不变
C . 生成的丙丁两种物质的分子个数比为2:3
D . 甲物质由一个氮原子和三个氢原子构成
2022年4月16日10时,神州十三号飞船返回舱顺利着陆,标志着我国航天事业又进一步。
-
(1) 返回舱侧壁采用的是铝合金材料,铝合金的优点是(答一点即可)。
-
(2) 铝在空气中与氧气反应,其表面生成一层致密的氧化物薄膜,从而阻止铝进一步氧化。这种氧化物是(填化学式)。
-
(3) 三位航天员在空间站生活了6个月,航天员需要的氧气是通过电解水获得的,请写出电解水的化学方程式:;电解水生成的氢气可以和二氧化碳结合得到甲烷和水,水资源得到了循环利用。
我国是世界上首个成功试采海域可燃冰的国家。可燃冰主要含有甲烷水合物,具有能量高、燃烧值大等优点,将成为未来新能源。
-
(1) 保持甲烷化学性质的最小粒子是。
-
(2) 下图是甲烷在氧气中充分燃烧的微观示意图。

①图中虚线方框内物质C的微观模型图是(填数字序号)。

②参加反应的物质A与B的化学计量数之比是。
-
(3) 甲烷与空气的混合气体点燃可能发生爆炸,因此点燃甲烷前,应该先。
用一氧化碳和氢气生产甲醇(CH3OH)的化学方程式为 , 计算若生产 16t甲醇,至少需要氢气的质量。
, 计算若生产 16t甲醇,至少需要氢气的质量。
 , 计算若生产 16t甲醇,至少需要氢气的质量。
, 计算若生产 16t甲醇,至少需要氢气的质量。
最近更新



