第四章 生命之源——水 知识点题库
根据下列实验示意图回答相关问题
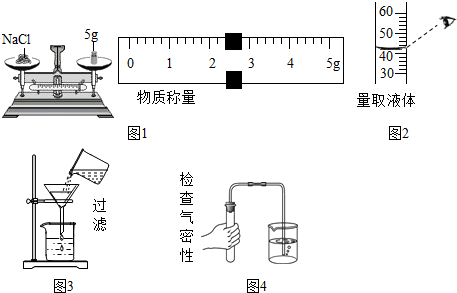
-
(1) 图1实验中称取氯化钠的质量为g,如果要要称取12.5g食盐(1g以下用游码),称量把食盐放在了右盘中,实际称量的食盐质量是g。如药品有腐蚀性应放在中称量。
-
(2) 按照图2所示方式读数比实际液体体积偏(选填“大”或“小”),正确的读数方法是,要量取25mL水,应选择量程为(选填“50mL”或“100mL”)的量筒。
-
(3) 改正图三中的两处明显不正确:;。
-
(4) 图4中实验装置气密性的检验方法是。
四氧化三铁可用于医疗器械、电子等工业。某实验兴趣小组从工厂采集废液(含FeSO4和少量ZnSO4、MgSO4),进行四氧化三铁的制备实验。
[阅读资料]
意义25℃时,氢氧化物沉淀的pH范围如下表。
|
Zn(OH)2 |
Fe(OH)2 |
Mg(OH)2 |
|
|
开始沉淀的pH |
5.7 |
7.6 |
10.4 |
|
沉淀完全的pH |
8.0 |
9.6 |
12.4 |
②25℃时,Zn(OH)2可溶于pH>10.5的碱溶液。
③制备Fe3O4的实验流程如下:

[回答问题]
-
(1) 往废液中加入氢氧化钠溶液生成沉淀的化学方程式为。
-
(2) 操作a的名称为。该操作需要的玻璃仪器有烧杯、玻璃棒、等。玻璃棒在此操作中的主要作用是。
-
(3) 溶液1所含溶质有(至少写两种),溶液3所含溶质的主要成分为(填化学式)。
粗盐中难溶性杂质的去除。
-
(1) 过滤时,用到的玻璃仪器有烧杯、玻璃棒和。
-
(2) 蒸发过程中,需不断进行搅拌,其原因是。
为了研究图一装置的工作原理,在装置左侧连接压强传感器,测定制取二氧化碳过程中的压强变化,如图二所示。

-
(1) 实验室用大理石和稀盐酸制取2.2g二氧化碳气体,求参加反应的碳酸钙的质量。
-
(2) 请描述ab时间段,装置内出现的现象。
如图为某化学反应的微观示意图。下列说法正确的是( )

A . 反应前后分子种类没有改变
B . 反应物的分子个数比为1:3
C . 该反应有3种生成物
D . 该反应可表示天然气主要成分的燃烧过程
某密闭容器中,甲、乙、丙、丁四种物质在反应前后的质量变化如图所示,下列说法正确的是( )

A . 该反应中甲、乙是反应物
B . 该反应是化合反应
C . 丙一定是该反应的催化剂
D . 反应前后甲、乙变化的质量比为9:8
在宏观微观和符号之间建立联系是化学学科的特点。
-
(1) 氢、碳和氧的原子结构示意图如图所示,回答下列问题。

①x的值是。
②氧元素属于(选填“金属”或“非金属”)元素。
③氢元素与碳元素组成的一种物质乙烯(C2H4)是重要的基本化工原料。由乙烯的化学式C2H4获得的信息有(写出一条即可)。
-
(2) 近年来,我国科研人员在“甲烷二氧化碳重整和Ni基催化剂”的研究方面取得突破。如图是甲烷与二氧化碳反应的微观示意图。

①框内缺失的C的微观模型图是。
②该反应利用了两种温室气体,兼具环保和经济价值;反应难点之一是破坏甲烷分子、二氧化碳分子的稳定结构,分解为(填微粒符号)并重新组合。
③写出该反应的符号表达式:。
我国古代将炉甘石、赤铜(Cu2O)和木炭粉混合加热到约800℃,可得到外观似金子的合金,涉及的化学方程式之一为2Cu2O+C  4Cu+X↑,下列说法正确的是( )
4Cu+X↑,下列说法正确的是( )
 4Cu+X↑,下列说法正确的是( )
4Cu+X↑,下列说法正确的是( )
A . X的化学式为CO
B . 该反应中赤铜发生还原反应
C . Cu2O中Cu的化合价为+2
D . 参加反应的Cu2O和C的质量比为2:1
下列有关水的说法错误的是( )
A . 煮沸可对水进行杀菌消毒
B . 生活污水集中处理后排放
C . 用肥皂水可区分硬水和软水
D . 过滤可降低水的硬度
兴趣小组用氧化铜样品(含少量杂质铜)进行了如下实验:用一定量的稀盐酸溶解5g样品,充分反应后过滤,得到100g滤液,向滤液加入NaOH溶液,所得实验数据如图:

-
(1) 配置一定质量分数的NaOH溶液的步骤为:、称量、量取、溶解、装瓶贴标签。
-
(2) 从图可知,加入的NaOH溶液先跟滤液中的(填化学式,下同)反应;图中B点溶质成分为。
-
(3) 求加入NaOH溶液的溶质质量分数。(写出计算过程,结果保留到0.1%)。
钴(Co)的化学性质与铁相似,但钴在常温下对水和空气都比较稳定。
-
(1) 图3是含钴物质的化合价——物质类别图

①物质a的化学式是;物质b的化学式是。
②R处对应的物质类别是。
-
(2) 下列预测钴的化学性质合理的是 (填标号)。A . Co在O2中燃烧生成Co3O4 B . 常温时钴易与H2O反应 C . Co能与稀H2SO4反应 D . CoCl3溶液中的杂质MgCl2可加入钴粉除去
-
(3) 已知CoSO4易溶于水,利用复分解反应原理设计三种制备CoSO4的方案。完成下表:
方案
预期反应的化学方程式
依据的反应规律
①
氧化物和酸反应生成盐和水
②
碱和酸反应生成盐和水
③
盐和酸反应生成新盐和新酸
以高氯冶炼烟灰(主要成分为铜锌的氯化物、氧化物、硫酸盐,少量Fe、As元素)为原料,可回收制备Cu和ZnSO4·H2O,其主要实验流程如下:

-
(1) 两段脱氯均需在85℃条件下进行,适宜的加热方式为。过滤操作时使用玻璃棒下端应放在过滤器内的上。
-
(2) “碱洗脱氯”时,发生:3Na2CO3 + 4CuCl2 + 3H2O=2Cu2(OH)3Cl↓ + 6+ 3CO2↑。若用NaOH溶液进行碱洗操作时,NaOH溶液浓度对脱氯率和其他元素浸出率的影响如下表所示。
NaOH浓度/%
脱氯率/%
元素浸出率/%
Cl
Zn
Cu
As
5.0
51.20
0.51
0.04
0.00
10.0
80.25
0.89
0.06
58.87
15.0
86.58
7.39
0.26
78.22
NaOH溶液的浓度不宜过大,通过上表的数据分析其原因是。
-
(3) “酸浸”时,过滤得到的Cu(OH)2发生的反应方程式是。
-
(4) 已知:国际制单位中,温度T的单位是K。ZnSO4的溶解度曲线如图所示。

①“电解”后,回收ZnSO4·H2O的实验操作:将ZnSO4溶液转移至蒸发皿中,、高于330 K趁热过滤、洗涤、低温干燥。
②若所得晶体含有ZnSO4·6H2O,则所得晶体的Zn的质量分数将(填“偏大”、“偏小”或“不变”)
-
(5) 取17.9 t ZnSO4·H2O固体于在密闭体系中加强热,使其完全分解生成ZnO,理论上可得到多少t ZnO?(写出计算过程)
已知向饱和食盐水中通入氨气得到饱和氨盐水,饱和氨盐水能与CO2发生反应:
 。某学习小组以饱和食盐水等为原料制备纯碱的主要流程如下:
。某学习小组以饱和食盐水等为原料制备纯碱的主要流程如下:
 。某学习小组以饱和食盐水等为原料制备纯碱的主要流程如下:
。某学习小组以饱和食盐水等为原料制备纯碱的主要流程如下: 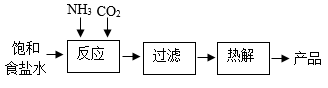
-
(1) 常温时,饱和氨盐水的pH(填“=”“<”或“>”)7.反应时,溶液中生成的NH4Cl中所含原子团的名称是。
-
(2) 过滤时,若过滤后滤液仍浑浊,其原因可能是(任写一条)。
-
(3) 热解时,NaHCO3分解得到纯碱、水和一种使澄清石灰水变浑浊的气体,该反应的化学方程式为。
逻辑推理是一种重要的化学思维方法,下列推理正确的是( )
A . 纯净物一定是由同种分子构成的,所以由同种分子构成的物质是纯净物
B . 如果某物质分解只生成了氧气和水,那么该物质一定只由氢元素和氧元素组成
C . 燃烧都伴随着发光、放热现象,所以有发光、放热现象的就是燃烧
D . 金属元素一般显正价,所以显正价的一定是金属元素
2021年12月9日15时40分,中国空间站开启“天宫课堂”第一课,介绍了空间站里的氧气源自电解水,同时所得的H2还可与CO2反应生成H2O和CH4 , 增强了资源循环利用。该反应的微观过程如图所示,则下列有关说法中错误的是( )

A . 图中x的数值为3
B . 反应生成H2O和CH4的分子个数比为2:1
C . 反应的生成物均为氧化物
D . 反应前、后氢元素的化合价发生了改变
下列指定反应的化学方程式书写正确的是( )
A . 铝在空气中生成氧化物薄膜: B . 碳酸氢铵受热分解:
B . 碳酸氢铵受热分解:  C . 铜和硝酸银溶液反应:
C . 铜和硝酸银溶液反应: D . 绿色植物的光合作用:
D . 绿色植物的光合作用:
 B . 碳酸氢铵受热分解:
B . 碳酸氢铵受热分解:  C . 铜和硝酸银溶液反应:
C . 铜和硝酸银溶液反应: D . 绿色植物的光合作用:
D . 绿色植物的光合作用:
高效消毒杀菌剂二氧化氯(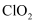 )可用NaClO2与Cl2反应制得,反应的化学方程式为
)可用NaClO2与Cl2反应制得,反应的化学方程式为 , 其中X是( )
, 其中X是( )
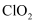 )可用NaClO2与Cl2反应制得,反应的化学方程式为
)可用NaClO2与Cl2反应制得,反应的化学方程式为 , 其中X是( )
, 其中X是( )
A . Na2O
B . NaCl
C . Na2O2
D . NaClO
以铝土矿(主要成分为Al2O3、FeO等)为原料生产金属铝的主要工艺流程如图:
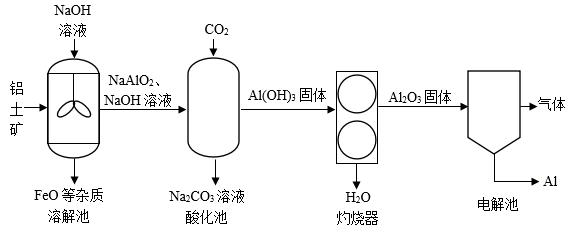
-
(1) 溶解池中搅拌的目的是。
-
(2) 灼烧器中的基本反应类型是。
-
(3) 上述流程中气体X的化学式为:。
下图表示两种气体发生化学反应,其中相同的球代表同种原子。根据图示信息,下列说法正确的是( )
![]()
A . 该反应生成两种物质
B . 该反应是复分解反应
C . 化学反应前后原子的种类不变
D . 分子在化学变化中是不可分的
在宏观、微观和符号之间建立联系是化学学科重要的思维方式。二氧化碳与氢氧化钠溶液反应的微观过程如下图所示,下列有关说法中错误的是( )

A . 反应前后氧元素的化合价不变
B . 乙表示的符号是 C . 氢氧化钠溶液可用来检验CO2
D . 水的化学性质由水分子保持
C . 氢氧化钠溶液可用来检验CO2
D . 水的化学性质由水分子保持
 C . 氢氧化钠溶液可用来检验CO2
D . 水的化学性质由水分子保持
C . 氢氧化钠溶液可用来检验CO2
D . 水的化学性质由水分子保持
最近更新



