课题2 如何正确书写化学方程式 知识点题库
 MgO2
MgO2
 4Fe + 3CO2↑
B . 除铁锈的化学反应:Fe2O3 +6 HCl =2FeCl2 +3 H2O
C . 消石灰吸收二氧化硫:Ca(OH)2 + SO2 =CaSO3+ H2O
D . 工业上制烧碱: K2CO3 + Ca(OH)2 = CaCO3↓+ 2KOH
4Fe + 3CO2↑
B . 除铁锈的化学反应:Fe2O3 +6 HCl =2FeCl2 +3 H2O
C . 消石灰吸收二氧化硫:Ca(OH)2 + SO2 =CaSO3+ H2O
D . 工业上制烧碱: K2CO3 + Ca(OH)2 = CaCO3↓+ 2KOH
(1) P+ FeO P2O5+ Fe
P2O5+ Fe
(2) Fe(红热)+ H2O(气) Fe3O4+ H2
Fe3O4+ H2
(3) N2+ H2 NH3
NH3
(4) Al+ Fe3O4 Fe+ Al2O3 .
Fe+ Al2O3 .
 Cu+CO2↑ 置换反应
D . 溶洞中石笋的形成:Ca(HCO3)2═CaCO3↓+H2O+CO2↑ 分解反应
Cu+CO2↑ 置换反应
D . 溶洞中石笋的形成:Ca(HCO3)2═CaCO3↓+H2O+CO2↑ 分解反应
 2H2O + CO2
B . P+ O2
2H2O + CO2
B . P+ O2  P2O5
C . S+O2
P2O5
C . S+O2  SO2↑
D . 4Fe+3O2
SO2↑
D . 4Fe+3O2  2Fe2O3
2Fe2O3
 2KCl+3O2
B . 2KClO3
2KCl+3O2
B . 2KClO3  2KCl+O2↑
C . 2KClO3
2KCl+O2↑
C . 2KClO3  2KCl+3O2↑
D . 2KClO3 =2KCl+3O2↑
2KCl+3O2↑
D . 2KClO3 =2KCl+3O2↑

-
(1) 实验室利用高锰酸钾制备氧气时,选用的发生和收集装置依次是(填字母序号,化学反应方程式是
-
(2) 请将下述实验步骤补充完整:
①检查装置的;②平放试管,用将反应物送至试管底端;
③先试管,然后集中加热试管底部,观察记录;④结束反应时,先将导管移离液面,再。
-
(3) 某同学用 C 装置收集气体时,发现水槽中的水变成了浅红色,产生该现象的原因是:
-
(4) 实验室利用装置制取二氧化碳,化学反应方程式是,足量盐酸与 200g 碳酸钙充分反应,生成二氧化碳的质量是g。
-
(5) 收集二氧化碳时,将燃着的木条放在瓶口,若观察到,说明瓶中已充满二氧化碳。
-
(6) 查阅资料:①相同条件下,氨气(NH3)的密度比空气小,且易溶于水,其水溶液称为氨水。②加热氯化铵和氢氧化钙固体混合物可制得氨气。根据查阅资料,制取氨气选择的发生装置是(填序号),收集氨气应选择的装置是(填序号)。

(查阅资料)碳酸钠和稀盐酸反应生成氯化钠、水和二氧化碳气体。
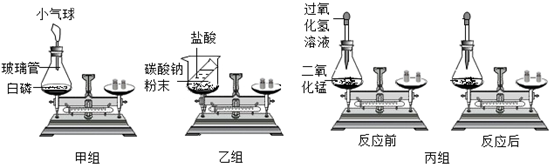
(实验装置设计)甲、乙、丙小组同学分别设计如图装置:
-
(1) (实验探究)
甲小组实验中,反应的化学方程式是。
-
(2) 乙组和丙组设计的“质量守恒定律”的实验如图所示。
①乙组实验结束后可观察到天平(填“平衡”或“不平衡”),此反应(填“遵守”或“不遵守”)质量守恒定律。
②丙组过氧化氢溶液分解反应前后各物质质量总和的测定,得出参加化学反应的各物质的质量总和(填“大于”、“等于”或“小于”)反应后生成的各物质的质量总和。该反应中二氧化锰起作用。
-
(3) (实验结论)参加化学反应的各物质质量总和等于生成的各物质质量总和。
(实验分析)在一切化学反应中,没有发生变化的是,所以参与反应前后各物质的质量总和相等。
A原子种类 B分子种类 C原子数目 D原子质量
-
(4) (反思与交流)
①通过甲、乙、丙小组实验的探究,你得到的启示是:探究质量守恒定律的实验应该在容器中进行。
②结论应用:环保部门常用
 测定空气受
测定空气受  污染的程度,发生反应的化学方程式为:的化学式是
污染的程度,发生反应的化学方程式为:的化学式是  。
。
 B .
B .  C .
C .  D .
D . 
-
(1) 金属的化学性质。完成下列反应的化学方程式:
①镁与氧气反应。
②锌与盐酸反应。
③铁与硫酸铜溶液反应。
-
(2) 金属的获得。
①金属氧化物加热分解。加热氧化银得到银和氧气,写出该反应的化学方程式。
②一定条件下,金属化合物与一些具有还原性的物质发生反应。在高炉内,把铁矿石冶炼成铁的主要反应原理是。
③电解法冶炼。工业上可以利用电解熔融氯化钠得到钠和氯气,该反应的基本反应类型是。
 Hg + O2↑
B . S + O2
Hg + O2↑
B . S + O2  SO2↑
C . 3Fe +2O2
SO2↑
C . 3Fe +2O2  Fe3O4
D . 2P+5O2
Fe3O4
D . 2P+5O2  2P2O5
2P2O5
-
(1) 高炉炼铁过程中生成铁的化学方程式;
-
(2) KIO3与KClO3的化学性质相似,写出KIO3在加热条件下分解的化学方程式。
 MgO2
B . 2KClO3
MgO2
B . 2KClO3  2KCl+3O2↑
C . CaCO3 = Ca0+CO2
D . CO+Fe2O3
2KCl+3O2↑
C . CaCO3 = Ca0+CO2
D . CO+Fe2O3  Fe+CO2
Fe+CO2
 B . 用铜与废洗影液(含硝酸银)制取银:
B . 用铜与废洗影液(含硝酸银)制取银:  C . 用熟石灰处理含硫酸的废水:
C . 用熟石灰处理含硫酸的废水:  D . 用二氧化碳制碳酸饮料:
D . 用二氧化碳制碳酸饮料: 
-
(1) 新能源电动大车使用的磷酸铁锂电池反应原理为
 ,该反应充电时,发生的化学反应属于(填基本反应类型)。
,该反应充电时,发生的化学反应属于(填基本反应类型)。
-
(2) 以下分类对于预测该物质化学性质没有帮助的是 (填标号)。A . 磷酸铁锂属于磷酸盐 B . 锂属于“活泼金属” C . 钴酸锂属于白色固体 D . 磷酸铁属于铁盐
-
(3) 依据各类物质之间的反应规律,设计两种制备磷酸铁(FePO4)的方案(要求依据两种不同的反应规律)。
已知:①磷酸铁(FePO4)的铁元素显正三价,是一种几乎不溶于水的白色固体;
②磷酸(H3PO4)为可溶性酸。完成下表:
方案
原料
预期反应的化学方程式
依据的反应规律
①
金属氧化物与酸反应生成盐和水
②
 氧化反应
B . 工业制烧碱
氧化反应
B . 工业制烧碱  复分解反应
C . 用金属铜置换银
复分解反应
C . 用金属铜置换银  置换反应
D . 用加热的方法除去碳酸铵固体中混有的少量碳酸氢铵
置换反应
D . 用加热的方法除去碳酸铵固体中混有的少量碳酸氢铵  分解反应
分解反应
-
(1) 西汉刘安所著的《淮南万毕术》中记载着“曾青得铁,则化为铜”,把铁放入硫酸铜溶液中会得到铜,这一发现要比西方国家早1700多年,是湿法冶金的先驱。该反应的化学方程式为。

-
(2) 北宋沈括被誉为“中国整部科学史中最卓越的人物”,他所著的《梦溪笔谈》中第一次提到了“石油”这一名称,文中关于石油制品“必大行于世”的科学预见,如今读来令人叹服。石油分馏、裂解出的汽油、柴油可作为燃料,燃料燃烧的过程是将能转化为热能。时至今日,氢气作为新能源与传统化石燃料相比,其优点是。(写一点即可)。

-
(3) 我国近代化学家侯德榜创立的侯氏制碱法,对化肥和制碱工业做出了杰出贡献,将制碱厂、合成氨厂、石灰厂联合起来,降低成本,极大提高了利用率。Na2CO3和NaCl的溶解度曲线如图所示。请回答下列问题:

①t1℃时,Na2CO3饱和溶液的溶质质量分数NaCl饱和溶液的溶质质量分数(填“大于”“小于”“等于”“无法确定”之一)。
②t2℃时,把30gNa2CO3放入盛有100g水的烧杯中,用玻璃棒充分搅拌后,然后降温至t1℃,此时所得溶液中溶质与溶剂的质量之比为(填最简整数比)。
③Na2CO3饱和溶液中混有少量的NaCl杂质,想要提纯Na2CO3可采用的方法是(填“蒸发结晶”“降温结晶”之一)。



