课题2 如何正确书写化学方程式 知识点题库
(1) NH3+Cl2═ N2+NH4Cl
(2) FeS2+ O2═ Fe2O3+ SO2
(3) C3H8+O2═CO2+ H2O
(4)N2O3+ Fe═ Fe3O4+ N2
(5) FeS2+O2═Fe2O3+SO2
(6) Al(OH)3+H2SO4═ Al2(SO4)3+H2O.
【提出问题】他们要探究的问题是这包久置的碱石灰样品的成分是什么?
【查阅资料】①碱石灰是由CaO和NaOH固体混合而成,通常用于吸收二氧化碳及干燥气体。②熟石灰固体溶解度小,溶于水放出的热量少,可以忽略不计。
【提出猜想】该碱石灰的主要成分可能含有CaO、NaOH、Ca(OH)2、CaCO3和。
【实验探究】小组的同学设计实验并进行验证,过程如下:
①小明取部分该碱石灰样品于试管中,加少量水后无放热现象,说明这包碱石灰样品中不含。继续加足量水,振荡,静置后有白色沉淀,小明认为碱石灰样品中一定含有CaCO3 , 小美认为他的结论不准确,原因是。(用化学方程式表示)
②从小明的试管中取少量上层清液于另一试管中,向其中滴加过量BaCl2溶液,有白色沉淀生成。
③把过程②所得物质过滤,向滤液中滴加无色酚酞溶液,溶液变红色。
【解释与结论】根据以上探究:
①你认为该包碱石灰样品一定含有的物质是 ,可能含有的物质是。
②实验探究过程③所得溶液中除酚酞外还含有的溶质是。
【迁移应用】下列气体①氢气 ②氧气 ③一氧化碳 ④氯化氢 ⑤二氧化硫 ⑥氨气 ,不能用碱石灰干燥的是(填字母序号)。
A. ①②③
B. ④⑤⑥
C. ④⑤
D. ⑤⑥
-
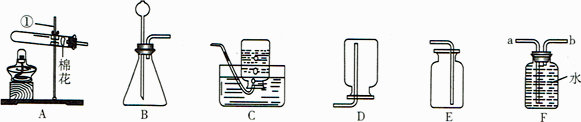
(1) 仪器①的名称是。
-
(2) 实验室若要用高锰酸钾为原料制取氧气,反应的文字表达式为,应选用的发生装置为 (填字母编号),若要收集到干燥的氧气则收集装置为(填字母编号)。
-
(3) 某同学用F装置收集氧气。他应该将氧气的发生装置与F装置的端相连(选填“a"或“b”),请你分析能用F装置收集氧气的原因:。
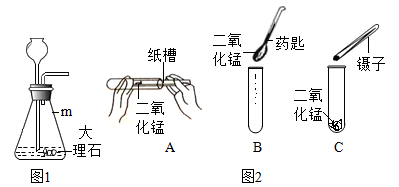
①实验室制取二氧化碳。
I 仪器 m 的名称是。从长颈漏斗中加入的试剂名称是。
II 将二氧化碳通入紫色石蕊试液中,观察到石蕊变色。
III 用法收集一瓶二氧化碳。证明二氧化碳已经收集满的方法是。
②实验室制取氧气。
I 取用二氧化锰操作正确的是(选填编号)。
II 用 3%左右的双氧水可平稳地制取氧气。现有 100g 15%的双氧水,为稀释成 3%的双氧水,需加入g水。
III 如需制取 0.1 摩尔的氧气,所需过氧化氢的质量至少为多少克?(根据化学方程式列式计算)
-
(1) 镁条在空气中点燃剧烈燃烧:
-
(2) 甲烷在空气中燃烧的化学方程式:
-
(3) 铜与硝酸银溶液反应化学方程式:
-
(4) ①写出化学式的名称并标出加点元素的化合价:
SO3:名称 ,化合价
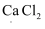 名称,化合价
名称,化合价②写出下列物质的化学式:
钻石:干冰:碳酸氢钠:磁铁矿:
-
(1) 铁丝在氧气中燃烧:;
-
(2) 二氧化碳使澄清的石灰水变浑浊:;
-
(3) 高锰酸钾制氧气:;
-
(4) 水通电分解:。
-
(1) 建造航母用到了钛合金,构成金属钛的粒子是(填“原子”“分子”或“离子”),工业制钛有一种反应为:TiF4+2H2SO4=4HF+2X+TiO2 , X的化学式为。
-
(2) 航母外壳用涂料覆盖,是为了防止钢铁材料与接触而锈蚀。
-
(3) 为了探究航母材料中锌、铁、铜三种金属活动性强弱,某同学设计了下列实验(每步均充分反应),其中能达到目的是 (填序号)。A . 稀盐酸中加入足量铁粉后,再加铜粉,最后加入锌粉 B . ZnCl2溶液中加入足量铁粉后,再加入CuCl2溶液 C . ZnCl2溶液中加入足量铜粉后,再加入铁粉
-
(4) 铝制品形成致密保护膜的化学方程式是。
-
(5) 氢化镁(MgH2)是一种贮氢合金,当它与H2O混合时释放出氢气,同时生成一种碱,该反应的化学方程式是。
-
(1) 嫦娥四号使用了大量复合材料。下列关于复合材料的说法中正确的是 。A . 不锈钢是常见的复合材料 B . 复合材料集中了组成材料的优点 C . 多种材料混在一起就是复合材料
-
(2) 航天器的天线用钛合金制成。钛合金与金属钛相比,的硬度更大。工业上通常是在高温下用四氯化钛(TiCl4)与金属镁发生置换反应获得,该反应的化学方程式为。
-
(3) 航天器上的太阳能电池是将太阳能直接转化为能的装置;大自然利用太阳能最成功的范例是(填序号)。
A.火山爆发 B.温室效应 C.光合作用

①焙烧,GeS2转化为GeO2 , 然后用盐酸溶解得到GeCl4。②用Cl2将杂质转化为不易挥发的H3AsO4。③加热混合溶液使GeCl4气化,再冷凝为液态,经过一系列转化得到GeO2。④用H2将GeO2还原为Ge,同时H2转化为H2O。
-
(1) 步骤①盐酸溶解GeO2的化学方程式为。
-
(2) 完成步骤②除杂反应的化学方程式:AsCl3+4H2O+Cl2=H3AsO4+5
-
(3) 步骤③分离GeCl4的方法是________(填标号)。A . 过滤 B . 蒸馏 C . 升华 D . 蒸发
-
(4) 步骤④消耗H2和生成Ge的质量之比为。
-
(1) 加热高锰酸钾制取氧气 ()
-
(2) 铝在氧气中燃烧生成氧化铝 ()
-
(1) 金刚石和石墨都是由碳元素组成的单质,但是由于不同,它们的物理性质存在着较大差异;
-
(2) 燃烧是人类最早利用的化学反应之一,火善用之为福,不善用之为祸。生活中遇到油锅着火时,通常用锅盖盖灭,其中利用的灭火原理是; 为了提高煤的利用率,通常将煤做成蜂窝状,甚至做成粉末状再使用,这样做的原因是。
-
(3) 氢化镁(MgH2)是一种贮氢合金,当它与水混合时释放出氢气,同时生成一种碱,该反应的化学方程式是。

白炽灯里的钨丝很害怕空气。如果玻璃壳里充满空气,通电以后,钨丝温度升高白烟灯到 2000℃以上,空气就会对它毫不留情地发动袭击,使它很快被烧断,同时生成一种黄白色的三氧化钨(化学式 WO3),所以功率在 40W 以下的钨丝灯泡要抽成真空,有时怕抽气机抽不干净,还要在灯泡的感柱上涂一点红磷。功率在 40W 以上的钨丝灯泡要充入氮气和氩气的混合气体做保护气。白炽灯用久了玻璃壳会变黑,原因是长时间的高温使钨丝表面的钨不断地升华扩散,然后一层又一层地沉积到玻璃壳的内表面上,使玻璃壳慢慢变黑。

节能灯通电时首先经过电子镇流器给灯管灯丝加热,灯丝开端发射电子(在灯丝上涂了一 些 电子粉),电子碰撞充装在灯管内的氩原子,氢原子碰撞后取得了能量又撞击内部的汞 原子,汞原子在吸收能量后产生电离,灯管内构成等离子态发光。节能灯寿命长达 8000 小时, 光效相当于普通灯泡的 6 倍。较白炽灯节能 70~80%,低压快启,无频闪。但节能灯也有弊端: 启动慢,灯管中汞成为一大污染源,1 只普通节能灯的含汞量约 5 毫克,仅够沾满一个圆珠笔尖,但渗入地下后可能造成 1800 吨水受污染。

LED 是发光二极管,是一种能够将电能转化为可见光的固态半导体器件,它可以直接把电能转化为光能。白光 LED 的能耗仅为白炽灯的1/10,节能灯的1/4。寿命可达 104万小时以上,是节能灯的 10~20 倍,绿色环保,不含铅、汞等污染元素,对环境没有任何污染。LED 灯的内在特征决定了它是代替传统光源的最理想光源,它有着广泛的用途。
-
(1) 灯泡的感柱上涂一点红磷,使用过程中红磷可能发生反应的化学方程式为
-
(2) 白炽灯用久了玻璃壳会变黑的微观过程是
-
(3) 节能灯的弊端是(答一点),请写出其灯管内充装的一种原子(写符号)。
-
(4) 下列说法错误的是(填字母)。
A 节能灯是最省电、寿命最长的灯泡 B 三种灯泡都能将电能转变成光能
C LED 灯在现阶段是最理想的光源 D 氮气做灯泡保护气的原因是其物理性质稳定
-
(1) 赤铁矿炼铁,炼铁设备是。
-
(2) 生石灰作为干燥剂的原理,该反应属于热反应(填“放”或“吸”)。
-
(3) 氨水与硫酸反应,基本反应类型是反应。
-
(4) 分别将铜片和锌片连接到电流表的正、负极,然后把锌片和铜片一起插入盛有硫酸铜溶液的烧杯中,发生的反应是。
-
(5) 酒精(C2H6O)完全燃烧,酒精的某种水溶液中溶质和溶剂的氢原子个数相等,则该溶液中溶质的质量分数为。
 2Fe2O3
D . 3CO + Fe2O3
2Fe2O3
D . 3CO + Fe2O3  2 Fe + 3 C O 2
2 Fe + 3 C O 2

-
(1) A的化学式为,D的俗名叫。
-
(2) C的用途为。
-
(3) B→D发生的反应的方程式为,这个反应(填“属于”或“不属于”)复分解反应。
-
(4) D和E反应的化学方程式为。
随着人类社会的发展,化石燃料的消耗量急剧增加,导致温室效应增强。科学家一直致力于将二氧化碳分离回收、循环利用和再生转化成资源。化学吸收法是利用吸收剂与二氧化碳发生化学友应来吸收分离二氧化碳的方法,常见的吸收剂有氢氧化钠溶液、氢氧化钙溶液等,加压水洗法也可用于捕获收集二氧化碳。二氧化碳和氢气在催化剂的作用下会发生一系列反应,生成甲醇、一氧化碳和甲烷等,实现再生转化。我国科学家在催化剂研究方面取得重大突破,分别合成出了镓酸锌(ZnGa2O4)介孔光催化材料和单晶纳米带,成功实现了将二氧化碳转化为碳氢化合物燃料。中国科学家用水、二氧化碳和电人工合成淀粉被国际学术界认为是影响世界的重大颠覆性技术,这一成果2021年9月24日在国际学术期刊《科学》上发表。
-
(1) 造成近几十年来空气中二氧化碳含量激增的主要原因是。
-
(2) 镓酸锌(ZnGa2O4)中镓元素的化合价为。
-
(3) 用氢氧化钠溶液吸收二氧化碳的化学反应方程式为。
-
(4) 二氧化碳和氢气在催化剂的作用下生成甲醇的原理为:


 , 则X的化学式为。
, 则X的化学式为。
-
(5) 你认为人工合成淀粉技术要得到广泛应用还需考虑到哪些问题?(答一点即可)
资料:i.铷原子钟为火箭运载系统提供精确时间,其单质化学性质比钾活泼。图1是元素周期表中铷元素的部分信息,图2是铷原子的结构示意图。
ⅱ.铕(Eu)为铁灰色金属(如图3),用作彩色电视机的荧光粉、激光等的重要材料。新制的金属铕在空气中点燃会猛烈燃烧,生成白色固体。
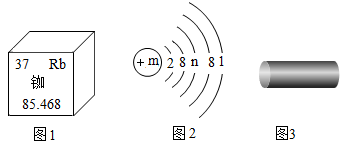
-
(1) 下列说法错误的是____(填标号)。A . 铷元素属于金属元素 B . 铷原子的质子数是37 C . 铷原子的中子数是37 D . 铷原子的相对原子质量85.468g
-
(2) 图2中n的数值为。
-
(3) 根据资料分析,铕的物理性质(写一点),铕的金属活动性可能比锌(填“强”或“弱”)。
-
(4) 铕在空气中燃烧生成+3价铕的氧化物的化学方程式是。



