单元2 质量守恒定律 知识点题库
物 质 | 氧气 | 二氧化碳 | 水蒸气 | M |
反应前的质量/g | 55 | 1 | 3 | 23 |
反应后的质量/g | 7 | y | 30 | x |

 向一定量的氧化铁中通入一氧化碳气体并持续高温
B .
向一定量的氧化铁中通入一氧化碳气体并持续高温
B .  通电使水分解
C .
通电使水分解
C . 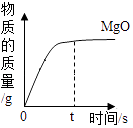 镁在氧气中燃烧
D .
镁在氧气中燃烧
D .  加热氯酸钾与二氧化锰的固体混合物
加热氯酸钾与二氧化锰的固体混合物

-
(1) 彩漂液(图 1)的有效成分为过氧化氢,长期存放会失效.用化学方程式解释失效的原因.

-
(2) 洁厕剂(图 2)含有盐酸,盐酸中的阳离子是(填符号),洁厕剂与“84”消毒液(图 3)混合会发生如下反应:2HCl+NaClO=X+H2O+Cl2↑,对人体造成伤害. 下列说法正确的是(填字母序号).

A.X 的化学式为 NaClB.对人体造成伤害的物质是氯气
C.洁厕剂能用于清除水垢D.NaClO 中氯的化合价为﹣1
-
(3) 洗发液(图 4)洗掉头发分泌的油脂,其原理是(填“乳化”或“溶解”) 作用.

-
(4) 还原铁粉常用于食品包装中(图 5),使用后发现铁粉变为红色,该红色固体主要 成分的化学式为.

-
(1) 区别水是硬水还是软水,可用的物质是;生活中可用降低水的硬度。
-
(2) 自来水生产过程中,可用方法除去水中不溶性杂质,同时还必须进行消毒。X是一种新型的自来水消毒剂,工业上制取X 的化学方程式为:Cl2 + 2 NaClO2 = 2 NaCl + 2 X,则X的化学式为。

-
(1) 从宏观知微观:
①50ml水与50ml乙醇混合后,溶液体积小于100ml,微观解释为;
②某气体X在氧气中燃烧生成氮气和水,X分子中一定含有的原子有(填符号)
③如上图1所示:符号“Cu”能表示多种信息,如表示铜元素、金属铜单质,还能表示。
④从微粒的角度说明图2反应的实质是。
-
(2) 从微观知宏观:
①如图2,微粒A、B、C、D、E中,对应单质化学性质最稳定的是(填化学式),属于同种元素的是(填编号),C在元素周期表位于第周期。
②图4为某化学反应的微观示意图,则该反应的化学方程式为。

计算:
-
(1) 制得氧气的质量是多少g;
-
(2) 过氧化氢质量分数是多少?
| 清洁剂名称 | 洁厕灵 | 84消毒液 |
| 有效成分 | HCl | NaClO |
| 混合后的反应 | NaClO+2HCl=NaCl+X↑+H2O | |
-
(1) 分类角度,CO2属于(填字母)。
a.单质 b.氧化物 c.有机物
-
(2) 微观角度,我国研制的一种新型催化剂可将CO2和H2转化为甲醇(CH3OH)和X。若用“○”表示氢原子,“⊕”表示氧原子, “●”表示碳原子,该反应的微观示意图如下:

画出X分子的微观示意图:。
-
(3) 性质角度,三百多年前,人们发现一些洞穴内有一种能使燃烧的木柴熄灭的气体,后来该气体被证实是CO2。据此推测CO2具有的化学性质是。
-
(4) 变化角度,如图是某同学整理的物质间转化图。

实验室中常用CO2→ CaCO3检验CO2气体,写出其化学反应方程式:。
-
(5) 应用角度
I.可用下图所示方法自制汽水来消暑解热。

制汽水时, NaHCO3与柠檬酸反应生成柠檬酸钠、二氧化碳和水。
①据此推测,通常条件下不能与柠檬酸反应的物质是(填字母)。
a.镁带 b.氯化钠 c.烧碱
②打开汽水瓶盖时汽水会自动喷出来。说明气体在水中的溶解度与有关。
Ⅱ.Al-CO2电池是一种新型电池。
③电池的工作原理:在O2的催化下,Al与CO2生化合反应生成Al2(C2O4)3。写出此反应的化学方程式:。
-
(6) 环保角度,全球参与控制CO2的排放量是防止温室效应进一步增强的根本对策。下列限制CO2排放量的做法不合理的是(填字母)。
a.制定旨在限制CO2排放的国际规定
b.减少化石能源的使用,开发太阳能等新能源
c.工厂通过加高烟囱直接排放含CO2的废气
 MnCl2 + Cl2↑ + 2X,则X的化学式是( )
MnCl2 + Cl2↑ + 2X,则X的化学式是( )
-
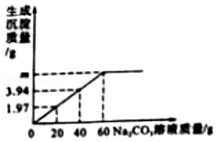
(1) m的值是g。
-
(2) 碳酸钠溶液的质量分数是多少?
-
(1) 铜粉在空气中加热后,生成物的质量要比原来铜粉质量;
-
(2) 将10gA和适量B混合加热至恰好完全反应型成8gC和4gD,则B的质量为g;
-
(3) 将蔗糖隔绝空气加热只得到黑色的炭和水,依据,可推断蔗糖中含有碳、氢、氧元素。
 Al2O3+AlCl3+3NO↑+6X↑,则X的化学式为( )
Al2O3+AlCl3+3NO↑+6X↑,则X的化学式为( )
 。向含溶质32.5g的FeCl3溶液中慢慢加入一定量的Cu粉,反应过程中FeCl3、CuCl2的质量随Cu粉质量变化如图.下列说法正确的是( )
。向含溶质32.5g的FeCl3溶液中慢慢加入一定量的Cu粉,反应过程中FeCl3、CuCl2的质量随Cu粉质量变化如图.下列说法正确的是( ) 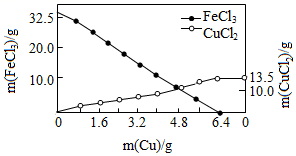
物质 | a | b | c | d |
反应前质量/g | 6.4 | 3.2 | 4.0 | 0.5 |
反应后质量/g | 待测 | 2.4 | 7.2 | 0.5 |
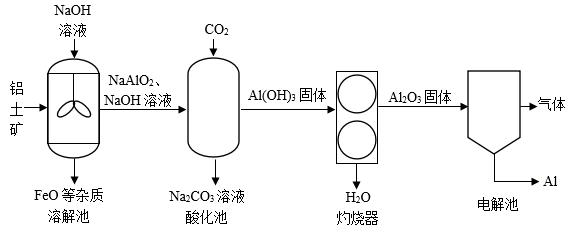
-
(1) 溶解池中搅拌的目的是。
-
(2) 灼烧器中的基本反应类型是。
-
(3) 上述流程中气体X的化学式为:。



