实验2-1 纸上层析分离甲基橙和酚酞 知识点题库
A.将一块pH试纸浸入稀盐酸中,测定溶液pH
B.用25mL酸式滴定管量取18.80mLKMnO4溶液
C.用苯萃取碘水中的I2时,有机层从分液漏斗的上口倒出
D.各放一张质量相同的滤纸于天平的两盘上,将NaOH固体放在左盘纸上称量
E.某钾盐溶于盐酸,产生能使澄清石灰水变浑浊的无色无味气体,则该钾盐为K2CO3
F.向某溶液中加入Ba(NO3)2溶液有白色沉淀产生,加盐酸沉淀不消失,则原溶液中一定含有SO42﹣ .
①石蕊试纸(检验气体): .
②容量瓶: .
③滴定管: .
④集气瓶(收集氨气): .
⑤托盘天平:
-
(1) 该学生的操作 (填“正确”或“错误”),其理由是
-
(2) 如不正确请说明理由,同时请分析是否一定有误差?
-
(3) 若用此方法分别测定c(OH﹣)相等的氢氧化钠溶液和氨水的pH,误差较大的是 ,原因是
-
(4) 只从下列试剂中选择实验所需的试剂,你能否区分0.1mol•L﹣1硫酸溶液和0.01mol•L﹣1硫酸溶液? ,简述操作过程.
试剂:A.紫色石蕊试液 B.酚酞试液 C.甲基橙溶液 D.蒸馏水 E.氯化钡溶液 F.pH试纸.
①用pH试纸测得氯水的pH为2
②不宜用瓷坩埚灼烧氢氧化钠固体
③使用容量瓶的第一步操作是先将容量瓶用蒸馏水洗涤后烘干
④比色分光光度计可以用于测量化学反应速率
⑤使用pH试纸测定溶液pH时先润湿,测得溶液的pH都偏小
⑥实验室配制氯化铁溶液时,可以先将氯化铁溶解在盐酸中,再配制到所需要的浓度
完成下列填空:
-
(1) N原子核外未成对电子的电子云空间伸展方向有个;CS2的电子式。
为了减少CO2的排放,利用CO2和H2在一定条件下可以合成CH3OH,反应的化学方程式为:CO2(g) + 3H2(g)
 CH3OH(g) + H2O(g),在5L密闭容器中充入1mol CO 2和3mol H2 , 测得一定时间内混合气体中CH3OH的体积分数φ(CH3OH)与温度的关系如下图所示。
CH3OH(g) + H2O(g),在5L密闭容器中充入1mol CO 2和3mol H2 , 测得一定时间内混合气体中CH3OH的体积分数φ(CH3OH)与温度的关系如下图所示。 
-
(2) 该反应的平衡常数K=;若温度为T时,反应10分钟,φ(CH3OH)=30%,则0~10分钟内,CH3OH的平均反应速率 ʋ =。
-
(3) 该反应是反应(选填“吸热”或“放热”);其它条件相同时,CH3OH在a点的正反应速率 CH3OH在b点的正反应速率(选填“>”、“<”或“=”);解释温度低于T时,φ(CH3OH)逐渐增加的原因。
-
(4) 化石燃料燃烧的烟气中含有影响环境的氮氧化物,因此要对烟气进行脱硝处理。液相氧化法采用碱性NaClO2溶液做吸收剂,反应如下:_ClO
 + _NO + _OH- → _NO
+ _NO + _OH- → _NO  + _Cl- + _H2O
+ _Cl- + _H2O 配平上述方程式。
写出使用广范pH试纸测定溶液pH的方法。
 )在工业上广泛应用于生产荧光粉。已知锶和镁位于同主族且锶比镁活泼,锶与氮气在加热条件下反应产生氮化锶,氮化锶遇水剧烈反应。某学习小组拟设计两套方案制备氮化锶并测定产品的纯度。
)在工业上广泛应用于生产荧光粉。已知锶和镁位于同主族且锶比镁活泼,锶与氮气在加热条件下反应产生氮化锶,氮化锶遇水剧烈反应。某学习小组拟设计两套方案制备氮化锶并测定产品的纯度。
-
(1) 方案I:根据下列装置制备氮化锶:

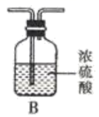


已知:实验室用饱和氯化铵溶液和亚硝酸钠溶液共热制备氮气。回答下列问题:
气流从左至右,选择装置并排序为 (用字母表示)。
-
(2) 写出实验室制备N2的化学方程式。
-
(3) 实验时先点燃处酒精灯(填“A”或“D”),一段时间后,点燃另一只酒精灯。
-
(4) 方案II:某氮气样品可能含有少量的CO、CO2、O2等气体杂质,某同学设计如下装置制备氮化锶(各装置盛装足量试剂)。已知:醋酸二氨合亚铜
 溶液能定量吸收CO,但易被O2氧化,失去吸收CO能力;连苯三酚碱性溶液能定量吸收O2。
溶液能定量吸收CO,但易被O2氧化,失去吸收CO能力;连苯三酚碱性溶液能定量吸收O2。 
试管II、III、IV盛装的试剂分别是(填标号),装置Ⅵ的作用是。
a.连苯三酚碱性溶液 b.浓硫酸 c.醋酸二氨合亚铜溶液
测定产品纯度:称取9.0g方案II中所得产品,加入干燥的三颈瓶中,然后由恒压漏斗加入蒸馏水,通入水蒸气,将产生的氨全部蒸出,用
 的盐酸标准溶液完全吸收(吸收液体体积变化忽略不计)。从烧杯中量取
的盐酸标准溶液完全吸收(吸收液体体积变化忽略不计)。从烧杯中量取  的吸收液,用
的吸收液,用  标准溶液滴定过剩的HCl,到终点时消耗
标准溶液滴定过剩的HCl,到终点时消耗  溶液(图中夹持装置略)
溶液(图中夹持装置略)
-
(5) 用
 标准溶液滴定过剩的盐酸时所选指示剂为(填标号)。
标准溶液滴定过剩的盐酸时所选指示剂为(填标号)。 a.石蕊试液 b.甲基橙 c.酚酞试液
-
(6) 产品纯度为%(保留一位小数)。
-
(7) 下列实验操作可能使氮化锶(
 )测定结果偏低的是(填标号)。
)测定结果偏低的是(填标号)。 a.锥形瓶洗涤干净后未干燥,直接装入待测液
b.滴定时未用
 标准溶液润洗滴定管
标准溶液润洗滴定管c.滴定前滴定管尖嘴处有气泡,滴定结束后气泡消失
d.读数时,滴定前平视,滴定后俯视
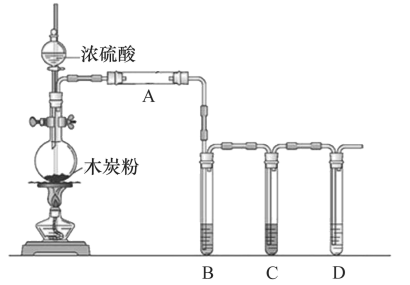
-
(1) 圆底烧瓶中发生反应的化学方程式为。
-
(2) A中应加入的试剂是。
-
(3) B中实验现象是,证明产物中有。
-
(4) C中装有过量的酸性高锰酸钾溶液,其作用是。
-
(5) 证明产物中有CO2的实验现象。



