课题一 物质的检验 知识点题库
 B . 制取乙酸乙酯
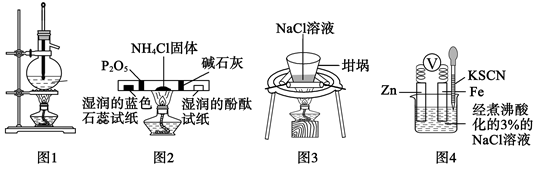
B . 制取乙酸乙酯 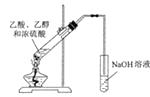 C . 比较氮、碳、硅元素非金属性
C . 比较氮、碳、硅元素非金属性  D . 检验碘离子
D . 检验碘离子 
| 选项 | 实验 | 现象 | 结论 |
| A. | 将稀硝酸加入过量铁粉中,充分反应后滴加KSCN溶液 | 有气体生成,溶液呈血红色 | 稀硝酸将Fe氧化为Fe3+ |
| B. | 将铜粉加1.0mol·L-1Fe2(SO4)3溶液中 | 溶液变蓝、有黑色固体出现 | 金属铁比铜活泼 |
| C. | 用坩埚钳夹住一小块用砂纸仔细打磨过的铝箔在酒精灯上加热 | 熔化后的液态铝滴落下来 | 金属铝的熔点较低 |
| D. | 将0.1mol·L-1MgSO4溶液滴入NaOH溶液至不再有沉淀产生,再滴加0.1mol·L-1CuSO4溶液 | 先有白色沉淀生成后变为浅蓝色沉淀 | Cu(OH)2的溶度积比Mg(OH)2的小 |
| 实验操作 | 现象 | 结论 | |
| A | 将石蜡油加强热(裂解)所产生的气体通入酸性高锰酸钾溶液中 | 溶液褪色 | 产物不都是烷烃 |
| B | 向盛有3 mL鸡蛋清溶液的试管里,滴入几滴浓硝酸 | 鸡蛋清变黄色 | 蛋白质可以发生颜色反应 |
| C | 将碘酒滴到新切开的土豆片上 | 土豆片变蓝 | 淀粉遇碘元素变蓝 |
| D | 将新制Cu(OH)2与葡萄糖溶液混合加热 | 产生红色沉淀 | 葡萄糖具有还原性 |
 C .
C .  D .
D . 

-
(1) 仪器a的名称是,应盛放下列药品中的(填字母)。
A.稀硫酸 B.亚硫酸 C.氢硫酸 D.盐酸
-
(2) 仪器b的名称是,应盛放下列药品中的(填字母)。
A.碳酸钙 B.硫酸钠 C.氯化钠 D.碳酸钠
-
(3) 仪器c中盛放的试剂是澄清石灰水,如果看到的现象是,说明b中发生反应的化学方程式为,即可证明H2SO4比H2CO3酸性强。
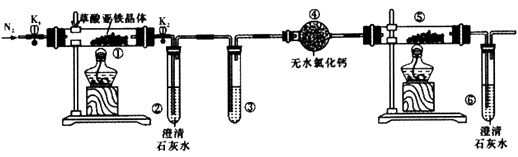
 )水溶液除去H2S,并使用2 mol·L-1 CuSO4溶液检验H2S是否除尽。
)水溶液除去H2S,并使用2 mol·L-1 CuSO4溶液检验H2S是否除尽。
回答下列问题:
-
(1) 仪器1的名称是。装置甲制取CO2 , 实验室制取CO2的离子方程式为。
-
(2) 仪器2盛装0.001 mol·L-1H2S水溶液,三颈烧瓶丙中盛装溶液是。
-
(3) 操作步骤:
①打开开关A、C,放入酸溶液产生CO2 , 目的是;
②一段时间后,关小开关C的出气量,打开压缩机开关,同时打开活塞放入H2S水溶液;逐渐减缓仪器1中酸溶液滴入速率并控制气压。使用CO2压缩机的作用是。
-
(4) 通入二氧化碳所形成的混合气体中,经测量含H2S的量为1000 ×10-6mg·m-3 , 则该混合气体中c(H2S)计算式为mol·L-1。
-
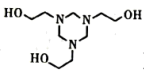
(5) 三嗪(
 )水溶液吸收H2S,生成
)水溶液吸收H2S,生成 和
和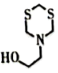 化学方程式为。CuSO4溶液没有出现 (填现象), 证明三嗪吸收H2S的化学反应具有、等特征,20%三嗪水溶液是很好的脱硫剂。
化学方程式为。CuSO4溶液没有出现 (填现象), 证明三嗪吸收H2S的化学反应具有、等特征,20%三嗪水溶液是很好的脱硫剂。
实验步骤与方法 | 实验现象 |
①将5瓶液体分别依次标号为A、B、C、D、E,然后闻气味 | 只有E没有明显气味 |
②各取少量5种液体于试管中,加水稀释 | 只有C、D不溶解并浮在水面上 |
③各取少量5种液体于试管中,滴加新制Cu( OH)2悬浊液并加热 | 只有 B使悬浊液中的固体溶解,E中产生砖红色沉淀 |
④各取少量C、D于试管中,加NaOH稀溶液并加热 | 只有C仍有分层现象,在D的试管口闻到特殊香味 |
-
(1) A为,E中溶质的分子式为。
-
(2) B中所含官能团的名称为。
-
(3) C的二氯代物有种。
-
(4) 写出C在Ni做催化剂的条件下与H2反应的化学方程式。
-
(5) 乙醇可通过乙烯与水在一定条件下反应得到,其对应的化学方程式为,反应类型为。



