第2节 氮的循环 知识点题库
绿色化学提倡化工生产应提高原子利用率。原子利用率表示目标产物的质量与生成物总质量之比。在下列用氨气氮肥的制备反应中,原子利用率最高的是( )
A . NH3+NaCl+H2O+CO2=NaHCO3+NH4Cl
B . 2NH3+CO2=2H2O+CO(NH2)2
C . 8NH3+3Cl2=N2+6NH4Cl
D . NH3+HCl=NH4Cl
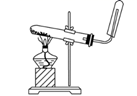
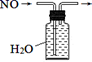
某学生利用以下装置探究氯气与氨气之间的反应.其中A、F分别为氨气和氯气的发生装置,C为纯净干燥的氯气与氨气反应的装置

请回答下列问题:
-
(1) 装置F中发生反应的化学方程式为;
-
(2) B装置的名称是;
-
(3) E装置的作用;
-
(4) 装置C内出现浓厚的白烟并在容器内壁凝结,另一生成物是空气的主要成分之一.请写出反应的化学方程式:;
-
(5) 从装置C的G处逸出的尾气中可能含有黄绿色的有毒气体,如何处理?(用离子方程式表示).
-
(6) 实验室通常利用质量分数36.5%盐酸(密度为1.14g/mL)与二氧化锰通过反应制取Cl2。通过计算回答下列问题:(要求有计算过程)
①质量分数36.5%(密度为1.14g/mL)盐酸的物质的量浓度为多少?
②若要制取Cl2 2.24L(标准状况),理论上需要消耗MnO2多少克?
下列有关物质性质与用途具有对应关系的是( )
A . H2O2具有强氧化性,可用作消毒剂
B . Fe2(SO4)3易溶于水,可用作净水剂
C . NH3具有还原性可用作制冷剂
D . C2H4具有可燃性可用作催熟剂
经过多方努力,郑州市的空气质量有明显改善。造成雾霾的重要原因之一是汽车尾气的排放,汽车加装尾气处理装置可以减少有害尾气的排放。在汽车尾气净化装置里,气体在催化剂表面吸附与解吸作用的过程如下图所示。下列说法错误的是( )

A . NO2是该过程的中间产物
B . 汽车尾气的主要污染成分为CO和NO
C . NO和O2必须在催化剂表面才能反应
D . 该催化转化的总反应方程式:2NO+O2+4CO  4CO2+N2
4CO2+N2
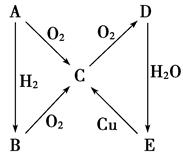
根据如图所示转化关系,判断A、B、C、D各是什么物质,写出有关的化学方程式:
-
(1) 当A为气体单质时,A是,B是,C是,D是,E是,E→C的化学方程式:。
-
(2) 当A为固体单质时,A是,B是,C是,D是,E是,E→C的化学方程式是。
加入NaOH溶液并加热,用湿润pH试纸靠近容器口时,试纸变蓝,这是在检验( )
A . Al3+
B . HCO3-
C . SO42-
D . NH4+
下列有关实验操作、现象、解释和结论都正确的是( )
| 操作 | 现象 | 解释、结论 | |
| A | 过量的Fe粉中加入硝酸充分反应,滴入KSCN溶液 | 溶液呈红色 | 稀硝酸将Fe氧化为Fe3+ |
| B | 向饱和Na2CO3溶液中通入足量CO2 | 溶液变浑浊 | 析出了Na2CO3晶体 |
| C | Al箔插入稀硝酸中 | 无现象 | Al在硝酸中钝化,形成致密的氧化膜 |
| D | 用玻璃棒蘸取浓氨水点到红色石蕊试纸上 | 试纸变蓝色 | 浓氨水呈碱性 |
A . A
B . B
C . C
D . D
今年我国多个城市遭遇雾霾天气,这表明污染严重,空气质量下降。因此研究NO2、SO2、CO等大气污染气体的处理具有重要现实意义。
-
(1) NO2可用水吸收,相应的化学反应方程式为。
-
(2) 利用反应6NO2+8NH3
 7N2+12H2O也可处理NO2。当转移1.2 mol电子时,消耗的NO2在标准状况下的体积是L。
7N2+12H2O也可处理NO2。当转移1.2 mol电子时,消耗的NO2在标准状况下的体积是L。
-
(3) 硝酸工业尾气中含NO和NO2气体,常用NaOH溶液来吸收,反应方程式为NO+NO2+2NaOH=2NaNO2+H2O,该反应中氧化剂和还原剂的物质的量之比是。
-
(4) 3.2gCu与30mL 8mol·L-1HNO3反应,硝酸的还原产物为NO,NO2 , 反应后溶液中所含H+为amol,则:
①溶液中n(
 )为。
)为。②所生成的NO在标准状况下体积为。
在给定条件下,下列选项所示物质间不满足每一步转化均能实现的是( )
A . N2(g) 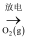 NO(g)
NO(g)  NaNO2(aq)
B . SiO2(s)
NaNO2(aq)
B . SiO2(s)  Na2SiO3(aq)
Na2SiO3(aq)  H2SiO3(s)
C . Al(s)
H2SiO3(s)
C . Al(s)  NaAlO2(aq)
NaAlO2(aq)  Al(OH)3(s)
D . Fe2O3(s)
Al(OH)3(s)
D . Fe2O3(s)  Fe(s)
Fe(s)  Fe(NO3)3(aq)
Fe(NO3)3(aq)
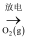 NO(g)
NO(g)  NaNO2(aq)
B . SiO2(s)
NaNO2(aq)
B . SiO2(s)  Na2SiO3(aq)
Na2SiO3(aq)  H2SiO3(s)
C . Al(s)
H2SiO3(s)
C . Al(s)  NaAlO2(aq)
NaAlO2(aq)  Al(OH)3(s)
D . Fe2O3(s)
Al(OH)3(s)
D . Fe2O3(s)  Fe(s)
Fe(s)  Fe(NO3)3(aq)
Fe(NO3)3(aq)
下列关于物质用途的叙述中,错误的是( )
A . 硅可用于制作半导体材料
B . 二氧化硅可用于制造光导纤维
C . 石墨可用作绝缘材料
D . 液氨可用作制冷剂
已知A、B、C、D、E、F是含有同一种元素的化合物,其中A是一种红棕色气体,B是一种无色气体,F是能使湿润的红色石蕊试纸变蓝的气体,它们之间能发生如下反应:
①A + H2O→ B + C;②C + F→D;③D + NaOH→F + E + H2O。
-
(1) 写出它们的化学式:A、C、D、F。
-
(2) 写出下列反应的离子方程式,并按要求填空:
①,该反应的氧化剂是,还原剂是
③。
-
(3) 工业生产C的过程中有一步反应为F经催化氧化生成B和H2O,写出该步反应的化学方程式。
下列各物质间的转化在给定条件下能实现的是( )
A . NH4H CO3  NH3
NH3  NO
B . 石油
NO
B . 石油 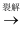 CH3CH3
CH3CH3  CH2BrCH2Br
C . 稀HNO3
CH2BrCH2Br
C . 稀HNO3  NO2
NO2  NO
D . 油脂
NO
D . 油脂  葡萄糖
葡萄糖  银镜
银镜
 NH3
NH3  NO
B . 石油
NO
B . 石油 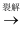 CH3CH3
CH3CH3  CH2BrCH2Br
C . 稀HNO3
CH2BrCH2Br
C . 稀HNO3  NO2
NO2  NO
D . 油脂
NO
D . 油脂  葡萄糖
葡萄糖  银镜
银镜
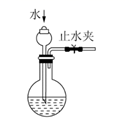
图中装置不能达到实验目的的是( )
| A | B | C | D |
| | | | |
| 实验室制取并收集氨气 | 吸收氨气 | 检验装置气密性 | 利用排空气法收集氨气 |
A . A
B . B
C . C
D . D
氨可用来处理氮氧化物,如氨与二氧化氮发生如下反应:6NO2 + 8NH3=7N2 + 12H2O。已知处理a L(标准状况,下同)某工厂排出的废气,需要b L氨,则废气中NO2的含量(体积分数)为( )
A . b/a
B . 0.75b/a
C . 0.75a/b
D . 75b/a
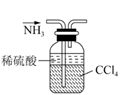
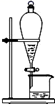
某中学一实验小组组装了下列所示实验装置。能达到实验目的的是( )
| A | B | C | D |
| | | | |
| 分离碘的四氯化碳溶液中的碘和四氯化碳 | 实验室制氨气 | 排水集气法收集NO | 除去NO气体中的NO2 |
A . A
B . B
C . C
D . D
已知甲、乙、丙三种物质均含有同种元素,其转化关系如下(反应条件已略去)。
![]()
下列推断错误的是( )
A . 若丙为红棕色气体,则甲可能为  B . 若丙为
B . 若丙为  ,则X与稀盐酸反应可以得到丙
C . 若乙为
,则X与稀盐酸反应可以得到丙
C . 若乙为  ,则甲可能是
,则甲可能是  D . 若乙能使品红溶液褪色,则甲一定是S单质
D . 若乙能使品红溶液褪色,则甲一定是S单质
 B . 若丙为
B . 若丙为  ,则X与稀盐酸反应可以得到丙
C . 若乙为
,则X与稀盐酸反应可以得到丙
C . 若乙为  ,则甲可能是
,则甲可能是  D . 若乙能使品红溶液褪色,则甲一定是S单质
D . 若乙能使品红溶液褪色,则甲一定是S单质
实验室模拟氨催化氧化法制硝酸的装置如图所示。下列说法错误的是 ( )

A . 装置④中溶液可使紫色石蕊溶液变红,说明有 HNO3生成
B . 装置③中产生红棕色气体
C . 装置①、②、⑤依次盛装碱石灰、P2O5、NaOH溶液
D . 通空气的主要作用是鼓出氨气,空气可用 N2代替
下列实验室制取、干燥、收集NH3并进行尾气处理的装置和原理能达到实验目的的是( )
A . 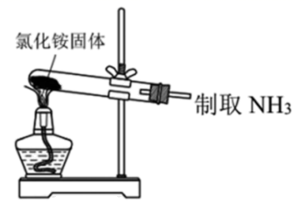 B .
B . 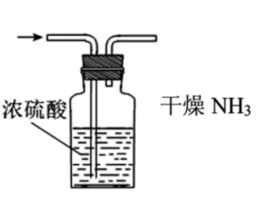 C .
C .  D .
D . 
 B .
B .  C .
C .  D .
D . 
NSR技术能降低柴油发动机在空气过量条件下NOx的排放,其工作原理如图所示。下列说法错误的是( )

A . 降低NOx排放可以减少酸雨的形成
B . 储存过程中NOx被氧化
C . 还原过程中消耗1molBa(NO3)2转移的电子数为5NA(NA为阿伏加德罗常数的值)
D . 通过BaO和Ba(NO3)2的相互转化实现NOx的储存和还原
下列说法正确的是( )
A . 淀粉、油脂和蛋白质均能发生水解反应
B . 合成纤维和光导纤维都是新型无机非金属材料
C . 煤的干馏和石油的分馏均属于物理变化。
D . 常温下,铁制的容器不能盛装浓硝酸
最近更新