4.1 物质在溶解过程中有能量变化吗? 知识点题库
下列说法中正确的是( )
A . 物质发生反应时放出的热量来源于对反应的加热
B . 化学反应除了生成新物质外,还发生能量变化,且总表现为吸热
C . 化学反应过程中有时吸热,有时放热
D . 化学反应总是放出热量
据新浪网报道,欧洲一集团公司拟在太空建立巨大的集光装置,把太阳光变成激光用于分解海水制氢,其反应可表示为:2H2O 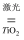 2H2↑+O2↑.有下列几种说法:①水分解反应是放热反应;②若用生成的氢气与空气中多余的二氧化碳反应生成甲醇储存起来,可改善生存条件;③使用氢气作燃料有助于控制温室效应;④氢气是一级能源.其中叙述正确的是( )
2H2↑+O2↑.有下列几种说法:①水分解反应是放热反应;②若用生成的氢气与空气中多余的二氧化碳反应生成甲醇储存起来,可改善生存条件;③使用氢气作燃料有助于控制温室效应;④氢气是一级能源.其中叙述正确的是( )
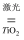 2H2↑+O2↑.有下列几种说法:①水分解反应是放热反应;②若用生成的氢气与空气中多余的二氧化碳反应生成甲醇储存起来,可改善生存条件;③使用氢气作燃料有助于控制温室效应;④氢气是一级能源.其中叙述正确的是( )
2H2↑+O2↑.有下列几种说法:①水分解反应是放热反应;②若用生成的氢气与空气中多余的二氧化碳反应生成甲醇储存起来,可改善生存条件;③使用氢气作燃料有助于控制温室效应;④氢气是一级能源.其中叙述正确的是( )
A . ①②
B . ③④
C . ②③
D . ①②③④
如图为反应2H2(g)+O2(g)═2H2O(g)的能量变化示意图,下列说法不正确的是( )
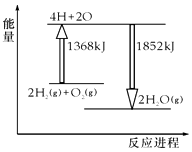
A . 拆开2molH2(g)和1 molO2(g)中的化学键成为H、O原子,共吸收1368 kJ能量
B . 由H、O原子形成2 molH2O(g),共放出1852 kJ能量
C . 2 molH2(g)和1 molO2(g)反应生成2 molH2O(g),共吸收484 kJ能量
D . 2 molH2(g)和1 molO2(g)反应生成2 molH2O(g),共放出484 kJ能量
图中没有涉及到的能量转化形式是( )

A . 化学能转化为热能
B . 太阳能转化为化学能
C . 势能转化为电能
D . 化学能转化为势能
海水晒盐的原理是( )
A . 海水分解
B . 温度升高,其他溶质的溶解度增大
C . 升高温度,降低食盐在水中的溶解度
D . 利用阳光、风力蒸发水分使氯化钠成晶体析出
下列设备工作时,将化学能转化为电能的是( ) 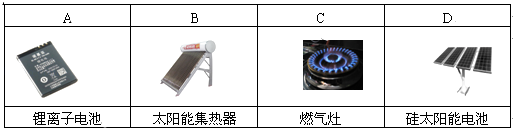

A . A
B . B
C . C
D . D
已知反应X + Y =M + N,该反应为吸热反应,下列说法不正确的是( )
A . 无法比较X的能量与M的能量的大小
B . Y的能量可能小于N的能量
C . X和Y的总能量一定小于M和N的总能量
D . 因该反应为吸热反应,所以一定要在加热条件下才能反应
反应A+B→C (放热反应)分两步进行①A+B→X(吸热反应)②X→C(放热反应)下列示意图中,能符合题意表示总反应过程中能量变化的是( )
A . 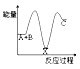 B .
B . 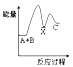 C .
C .  D .
D . 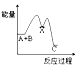
 B .
B .  C .
C .  D .
D . 
已知反应物的总能量高于产物的总能量,则反应是( )
A . 放热反应
B . 吸热反应
C . 有催化剂作用
D . 无法判断
下列反应既属于氧化还原反应,又属于吸热反应的是( )
A . 双氧水受热分解
B . Ba(OH)2·8H2O晶体与NH4Cl晶体的反应
C . 灼热的木炭与二氧化碳化合
D . 甲烷在空气中燃烧的反应
由反应物X转化为Y和Z的能量变化如图所示。下列说法正确的是( )

A . 由X→Y反应的ΔH=E5-E2
B . 由X→Z反应的ΔH>0
C . 降低压强有利于提高Y的产率
D . 升高温度有利于提高Z的产率
某反应由两步反应A→B→C构成,它的反应能量曲线如图所示(E1、E2、E3、E4表示活化能)。下列有关叙述正确的是( )

A . 三种化合物中C最稳定
B . 加入催化剂会改变反应的焓变
C . 两步反应均为吸热反应
D . A→C反应中ΔH=E1 - E2
下图表示某可逆反应在使用和未使用催化剂时,反应过程和能量的对应关系。下列说法一定正确的是( )
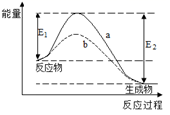
A . 该反应为吸热反应
B . a与b相比,a的反应速率更快
C . a与b相比,反应的平衡常数一定不同
D . E2大于E1 , 说明总能量生成物比反应物低
下列反应既是氧化还原反应,又是吸热反应的是( )
A . 锌与稀硫酸反应
B . 氢氧化钡与氯化铵反应
C . 灼热的炭与二氧化碳反应
D . 盐酸与碳酸氢钠的反应
下列相关实验所推出的结论正确的是( )
A .  受热能分解,所以可以用加热
受热能分解,所以可以用加热  固体的方法制氨气
B . Fe与稀
固体的方法制氨气
B . Fe与稀 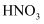 、稀
、稀  反应均有气泡产生,说明Fe与两种酸均发生置换反应
C . 向溶液中滴加硝酸酸化的
反应均有气泡产生,说明Fe与两种酸均发生置换反应
C . 向溶液中滴加硝酸酸化的 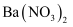 溶液出现白色沉淀,不能说明该溶液中一定有
溶液出现白色沉淀,不能说明该溶液中一定有  D . 铝热剂发生的铝热反应需要用镁带和氯酸钾引燃,所以铝热反应是吸热反应
D . 铝热剂发生的铝热反应需要用镁带和氯酸钾引燃,所以铝热反应是吸热反应
 受热能分解,所以可以用加热
受热能分解,所以可以用加热  固体的方法制氨气
B . Fe与稀
固体的方法制氨气
B . Fe与稀 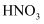 、稀
、稀  反应均有气泡产生,说明Fe与两种酸均发生置换反应
C . 向溶液中滴加硝酸酸化的
反应均有气泡产生,说明Fe与两种酸均发生置换反应
C . 向溶液中滴加硝酸酸化的 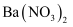 溶液出现白色沉淀,不能说明该溶液中一定有
溶液出现白色沉淀,不能说明该溶液中一定有  D . 铝热剂发生的铝热反应需要用镁带和氯酸钾引燃,所以铝热反应是吸热反应
D . 铝热剂发生的铝热反应需要用镁带和氯酸钾引燃,所以铝热反应是吸热反应
已知下列热化学方程式:
①H2(g)+  O2(g)=H2O(l);△H=﹣285kJ/mol
O2(g)=H2O(l);△H=﹣285kJ/mol
②H2O(g)=H2(g)+  O2(g);△H=+241.8kJ/mol
O2(g);△H=+241.8kJ/mol
③C(s)+  O2(g)=CO(g);△H=﹣110.4kJ/mol
O2(g)=CO(g);△H=﹣110.4kJ/mol
④C(s)+O2(g)=CO2(g);△H=﹣393.5kJ/mol
回答下列各问:
-
(1) 上述反应中属于放热反应的是.(用序号填写)
-
(2) C的燃烧热为.
-
(3) 燃烧10g H2生成液态水,放出的热量为.
-
(4) CO的燃烧热的热化学方程式为.
Na2S2O3•5H2O是重要的化工原料,有关制备和应用如下。
-
(1) Ⅰ.制备Na2S2O3•5H2O反应原理:Na2SO3(aq)+S(s)
 Na2S2O3(aq)
Na2S2O3(aq)实验步骤:
①称取15gNa2SO3加入圆底烧瓶中,再加入80mL蒸馏水。另取5g研细的硫粉,用3mL乙醇润湿,加入上述溶液中。
②安装实验装置(如图所示,部分夹持装置略去),水浴加热,微沸60min。回答下列问题:
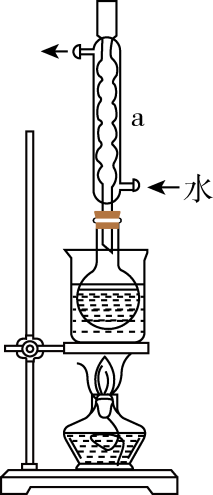
硫粉在反应前用乙醇润湿的目的是。
-
(2) 仪器a的作用是。
-
(3) 产品中除了有未反应的Na2SO3外,是可能存在的无机杂质是,检验是否存在该杂质的方法是。
-
(4) Ⅱ.分离Na2S2O3•5H2O。已知:Na2S2O3•5H2O于40~45℃熔化,48℃分解;Na2S2O3易溶于水,不溶于乙醇。
分离Na2S2O3•5H2O晶体的流程如图所示:





回答下列问题:
为减少产品的损失,操作①要(填操作),其目的是;操作②的包括的过程是快速过滤、洗涤、干燥,其中洗涤操作是用(填试剂)作洗涤剂。
-
(5) 蒸发浓缩滤液直至溶液为止,蒸发时要控制温度不宜过高原因。
-
(6) Ⅲ.研究外界条件对化学反应速率的影响,设计实验如表(所取溶液体积均为10mL):
实验编号
实验温度/℃
c(Na2S2O3)/mol·L-1
c(H2SO4)/mol·L-1
⑴
25
0.1
0.1
⑵
25
0.1
0.2
⑶
50
0.2
0.1
⑷
50
0.1
0.1
探究浓度对化学反应速率的影响,应选择(填实验编号)。
-
(7) 探究温度对化学反应速率的影响,应选择(填实验编号)。
现代社会人类的一切活动都离不开能量,下列说法正确的是( )
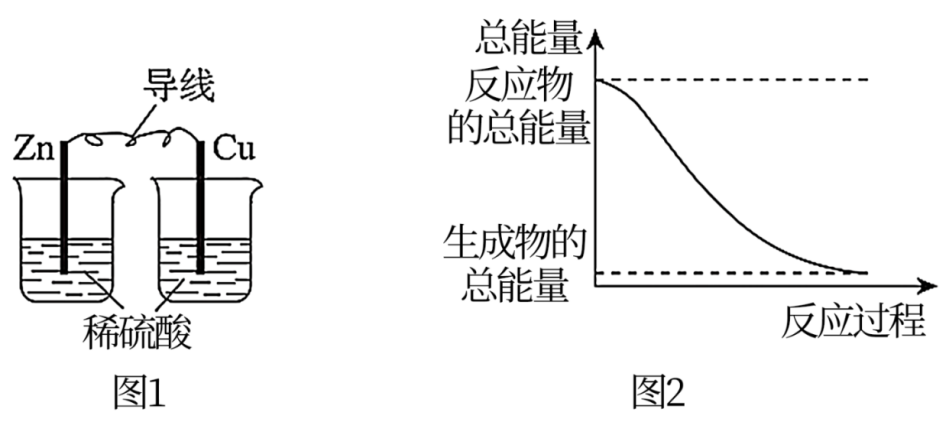
A . 图1所示装置能将化学能转化为电能
B . 图2所示反应为吸热反应
C . 手机锂离子电池属于二次电池
D . 锌锰干电池中,锌做正极
先进的甲醇蒸气重整—变压吸附技术可得到高浓度 混合气、
混合气、 , 化学反应原理是
, 化学反应原理是 , 其能量变化如图所示。下列说法正确的是( )
, 其能量变化如图所示。下列说法正确的是( )
 混合气、
混合气、 , 化学反应原理是
, 化学反应原理是 , 其能量变化如图所示。下列说法正确的是( )
, 其能量变化如图所示。下列说法正确的是( )
A .  转变成
转变成 的过程是一个吸收能量的过程
B . 反应物的总能量大于生成物的总能量
C . 形成
的过程是一个吸收能量的过程
B . 反应物的总能量大于生成物的总能量
C . 形成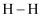 键吸收能量
D . 断开
键吸收能量
D . 断开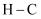 键放出能量
键放出能量
 转变成
转变成 的过程是一个吸收能量的过程
B . 反应物的总能量大于生成物的总能量
C . 形成
的过程是一个吸收能量的过程
B . 反应物的总能量大于生成物的总能量
C . 形成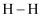 键吸收能量
D . 断开
键吸收能量
D . 断开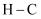 键放出能量
键放出能量
下列图示实验操作错误的是( )
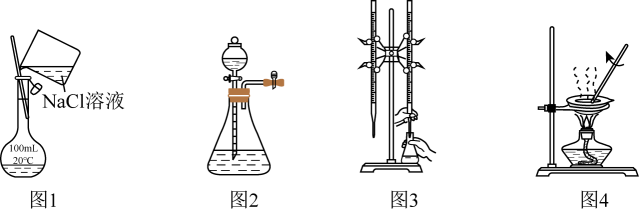
A . 图1装置可配制100mL一定物质的量浓度的NaCl溶液
B . 图2装置中打开分液漏斗的瓶塞和活塞,液面高度不变,说明装置气密性良好
C . 图3装置用已知浓度的KMnO4溶液滴定未知浓度的FeSO4溶液
D . 图4装置用蒸发皿加热MgCl2溶液得到MgCl2固体
最近更新



