第二节 氯及其化合物 知识点题库
某兴趣小组拟利用如下图装置探究验证干燥的Cl2和潮湿的Cl2有无漂白性.

回答下列问题:
(1)A装置中的主要玻璃仪器有:导管、酒精灯、圆底烧瓶、 .
A装置中发生反应的化学方程式是 .
(2)按气体从左向右流向将各装置依次连接起来(填接口标号):a 接 , 接 , 接 , 接 , 接 .
(3)A装置中发生反应,产生Cl2后,从集气瓶B、C中有色布条的现象可得出的结论是 ;其中发生反应的化学方程式为 .
(4)F装置中饱和NaCl溶液作用为 .D装置中浓 H2SO4作用为 .
(5)烧杯E中发生反应的化学方程式为 .
(6)工业生产漂白粉的化学方程式
在反应中消耗2mol氯气,则转移了 mol电子.
(7)工业上可用氨与Cl2反应检验输送氯气的管道是否漏气,反应方程式如下:8NH3+3Cl2═6NH4Cl+N2 . 该反应中, 是还原剂;若反应中有1.5mol氧化剂参与反应,则发生转移的电子的物质的量为 mol,被氧化的物质有 mol.
(1)活性炭(2)氯水(3)二氧化硫(4)臭氧 (5)过氧化钠 (6)双氧水.
X气体 | Y溶液 | 预测的现象 |
| |
① | CO2 | 饱和Na2CO3溶液 | 白色沉淀析出 | |
② | SO2 | Ba(NO3)2溶液 | 白色沉淀析出 | |
③ | Cl2 | AgNO3溶液 | 白色沉淀析出 | |
④ | NH3 | AlCl3溶液 | 白色沉淀析出 |

-
(1) 制备氯气选用的药品为固体二氧化锰和浓盐酸,则相关的化学反应方程式为:;
装置B中饱和食盐水的作用是;同时装置B亦是安全瓶,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象.
-
(2) 装置C的实验目的是验证氯气是否具有漂白性,为此C中Ⅰ、Ⅱ、Ⅲ依次放入
A
B
C
D
Ⅰ
干燥的有色布条
干燥的有色布条
湿润的有色布条
湿润的有色布条
Ⅱ
碱石灰
浓硫酸
浓硫酸
无水氯化钙
Ⅲ
湿润的有色布条
湿润的有色布条
干燥的有色布条
干燥的有色布条
-
(3) 设计装置D、E的目的是比较氯、溴、碘单质的氧化性强弱.当向D中缓缓通入少量氯气时,溶液中发生的反应方程式为;打开活塞,将装置D中少量溶液加入装置E中,振荡.观察到的现象.说明氯、溴、碘单质的氧化性强弱顺序为.

已知:①SOCl2遇水剧烈反应,液面上产生白雾,并有气体产生。
②SOCl2沸点为77℃,SCl2的沸点为 50 ℃。
请回答:
-
(1) 实验室制取SOCl2的反应方程式为。
-
(2) 实验室制取SOCl2在三颈烧瓶中合成,整个装置所选仪器的连接顺序是⑥→ →①,→②(某些仪器可以重复使用)。
-
(3) 使用冷凝管的作用是;冷凝管上连接的干燥管的作用是 。
-
(4) 实验结束后,将三颈烧瓶中混合物分离实验操作名称是。
-
(5) 若反应中消耗的Cl2的体积为896mL (已折算为标准状况,SO2足量) 最后得到纯净的SOCl26.76g,则SOCl2的产率为(保留二位有效数字)。
-
(6) 取少量的SOCl2加入足量NaOH溶液,振荡静置得到无色溶液,检验溶液中存在Cl-的方法是。
-
(1) 写出新制氯水中含量最多的微粒的化学式(水分子除外)
-
(2) 写出漂白粉中有效成分的名称
-
(3) 描述检验溶液中K+离子的实验操作过程
-
(4) 配平下列化学方程式
()Cu+()HNO3(稀)=()Cu(NO3)2+()NO↑+()H2O
-
(5) 按照物质的分类,次磷酸(H3PO2)属于二元酸,其与足量的NaOH溶液反应的化学方程式为
 B .
B .  C .
C .  D .
D . 

已知:该装置气密性良好,铁粉放在耐高温托盘内(防止硬质玻璃管炸裂)。
请回答下列问题:
-
(1) 为防止铁粉被空气中的氧气氧化,在加热之前应该进行的操作为。
-
(2) 实验中,观察到紫色石蕊溶液颜色的变化为。
-
(3) 实验装置中空试管的作用是。
-
(4) 烧杯中氢氧化钠溶液的作用是。
-
(5) 盛水的试管中,溶液的颜色为,说明氯气(填“能”或“不能”)溶于水。
 )、氯化亚砜(
)、氯化亚砜(  )常作氯化剂,用于制造药品、染料和表面活性剂。它们部分性质如下:
)常作氯化剂,用于制造药品、染料和表面活性剂。它们部分性质如下: | 物理性质 | 化学性质 | |
| | 熔点:-54.1℃ 沸点:69.1℃ | ①100℃分解生成 ②遇水蒸气产生大量白雾 |
| | 在空气中遇水蒸气发生剧烈反应,产生大量白雾 |
实验室合成  的原理:
的原理:  。某小组设计实验如图所示(夹持仪器已省略):
。某小组设计实验如图所示(夹持仪器已省略):

回答下列问题:
-
(1) D中试剂是 ,活性炭的作用是 ;
-
(2) 实验室常用高锰酸钾固体与浓盐酸在常温下反应制氯气,写出反应的离子方程式 ;
-
(3) 实验室用
 粉末与75%的浓硫酸反应制备
粉末与75%的浓硫酸反应制备  ,发现产生
,发现产生  很少,可能的原因是 ;
很少,可能的原因是 ;
-
(4) E中碱石灰的作用是 ;
-
(5) 氯化亚砜遇水蒸气发生反应的化学方程式是 ;实验室蒸干
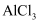 溶液不能得到无水
溶液不能得到无水 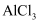 ,但是
,但是  和
和  混合物加热,可得到无水
混合物加热,可得到无水 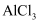 ,其主要原因是 ;
,其主要原因是 ;
-
(6) 为了测定
 产品纯度(杂质不参与反应),称取a g
产品纯度(杂质不参与反应),称取a g  产品于锥形瓶中(如图所示),向锥形瓶中加入足量蒸馏水,充分反应后,用c
产品于锥形瓶中(如图所示),向锥形瓶中加入足量蒸馏水,充分反应后,用c  溶液滴定至终点(滴几滴
溶液滴定至终点(滴几滴  溶液作指示剂),消耗
溶液作指示剂),消耗  溶液为V mL。
溶液为V mL。 ①用棕色滴定管盛装
 溶液,其原因是 ;
溶液,其原因是 ;②该
 产品的纯度为 ;
产品的纯度为 ;③实验中,控制分液漏斗活塞,缓慢滴加水,避免氯化氢挥发。如果操作时滴加水过快,测得结果 (填“偏高”“偏低”或“无影响”)。

-
(1) 将容积为50 mL的量筒充满二氧化氮和氧气的混合气体,将量筒倒置在盛满水的水槽里,一段时间后,量筒里剩余气体体积为5 mL。则原混合气体中NO2和O2体积比可能是或。
-
(2) 工业制硫酸的过程中,SO2被氧气氧化的化学方程式为。
-
(3) 工业制漂白粉的化学方程式。

 既可被氧化,也可被还原
B .
既可被氧化,也可被还原
B . 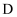 的浓溶液可与
的浓溶液可与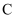 的固体反应生成
的固体反应生成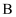 与
与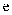 C . 实验室可通过加热
C . 实验室可通过加热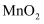 与
与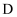 的浓溶液制得
的浓溶液制得 D . 可存在
D . 可存在 的循环转化关系
的循环转化关系
 HCl
B . KClO3
HCl
B . KClO3  KCl
C . Cl2
KCl
C . Cl2  FeCl2
D . NaClO(ag)
FeCl2
D . NaClO(ag) 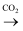 HClO
HClO

请回答下列问题:
-
(1) 仪器E中收集的Cl2颜色是;
-
(2) 仪器A的名称是;
-
(3) 仪器C中的饱和食盐水可以除去Cl2中混有的杂质气体是(填化学式):
-
(4) 自来水厂使用ClO2给自来水进行消毒,ClO2中氯元素的化合价是。
-
(5) 在新冠疫情防控期间,公共场所要求勤通风勤消毒,其中84消毒液经常用于公共场所消毒,制取84消毒液发生化学反应的离子方程式是。





