第一节 原子结构与元素周期表 知识点题库
氧族元素的各种性质可归纳整理出如表(部分):
元素 性质 | 8O | 16S | Se | 52Te |
单质沸点(℃) | ﹣183 | 444.6 | 685 | 1 390 |
主要化合价 | ﹣2 | ﹣2,+4,+6 | ﹣2,+4,+6 | |
原子半径(nm) | 0.074 | 0.102 | 0.116 | 0.143 |
单质与H2反应 | 点燃易化合 | 加热化合 | 加热难化合 | 不能直接化合 |
回答下列问题:
-
(1) S2﹣的电子式为
-
(2) 氧元素比硫元素非金属性 (填强或弱).请用化学方程式证明该结论:
完成下列各题
-
(1) 填写下列各题
①微粒2311Na+中的质子数是 ,中子数是 ,核外电子数是 .
②将 A.质子数 B.中子数 C.核外电子数 D.最外层电子数 E.电子层数
填入下列空格内 (只填写序号)
ⅰ.原子种类由 决定ⅱ.元素种类由 决定
ⅲ.元素的同位素由 决定ⅳ.同位素的相对原子质量由 决定
ⅴ.元素的原子半径由 决定ⅵ.元素的化合价主要由 决定
ⅶ.元素的化学性质主要由 决定ⅷ.价电子数通常是指
ⅸ.核电荷数由 决定
-
(2)
下列是用化学方程式表示的化学变化,请在每小题后的横线上注明能量的转化形式
①C2H5OH+3O2
 2CO2+3H2O:
2CO2+3H2O: ②Pb+PbO+2H2SO4
 2PbSO4+2H2O:
2PbSO4+2H2O: ③6H2O+6CO2
 C6H12O6+6O2:
C6H12O6+6O2: ④2Mg+O2
 2MgO:
2MgO: -
(3) H2O2、KCl、NaOH、Na2O2、HCl、O2中只含离子键的是 ;只含极性键的是 ;只含非极性键的是 ;既含离子键又含极性键的是 ,既含离子键又含非极性键的是 ,既有极性键又有非极性键的是
五种短周期元素A,B,C,D,E的原子序数依次增大,A和C同族,B和D同族,C离子和B离子具有相同的电子层结构.A和B,D,E均能形成共价型化合物.A和B形成的化合物在水中呈碱性,C和E形成的化合物CE在水中呈中性.
回答下列问题:
-
(1) 五种元素中,原子半径最大的是,非金属性最强的是(填元素符号);
-
(2) 由A和B,D,E所形成的共价型化合物中,热稳定性最差的是(用化学式表示);
-
(3) A和E形成的化合物与A和B形成的化合物反应,产物的化学式为,其中存在的化学键类型为;
-
(4) 单质E与水反应的离子方程式为.
两种短周期的元素X和Y,可组成化合物XY3 . 当Y的原子序数为m时,X的原子序数可能是:①m﹣4,②m+4,③m+8,④m﹣2,⑤m+6,其中正确的组合是( )
A . ①②
B . ①②③
C . ①②⑤
D . ①②③④⑤
下列各关系中,正确的是( )
A . 原子半径:O>S>Se
B . 单质的化学活动性:Cl2>F2>I2
C . 气态氢化物的稳定性:H2O>H2S>H2Se
D . 最高价氧化物对应水化物的碱性:LiOH>NaOH>KOH
A,B,C,D,E是同周期元素,A,B的最高价氧化物的水化物呈碱性,且B比A的碱性强,C,D最高价氧化物水化物是酸,且C比D的酸性强,E是这五种元素中原子半径最大的,则它们的原子序数由小到大的顺序为( )
A . E,B,A,D,C
B . D,B,C,A,E
C . E,C,D,B,A
D . A,B,C,D,E
下列叙述中能肯定说明金属A比金属B的活泼性强的是( )
A . A原子最外层电子数比B原子的最外层电子数少
B . 由金属A和金属B构成的原电池,电子由A流向B
C . 1molA从酸中置换生成的H2比1mol B从酸中置换生成的H2多
D . 常温时,A能从酸中置换出氢,而B不能
氯元素有 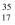 Cl、
Cl、  Cl两种同位素,其中
Cl两种同位素,其中  Cl的中子数和电子数之差为( )
Cl的中子数和电子数之差为( )
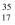 Cl、
Cl、  Cl两种同位素,其中
Cl两种同位素,其中  Cl的中子数和电子数之差为( )
Cl的中子数和电子数之差为( )
A . 17
B . 20
C . 1
D . 3
【化学——选修3:物质结构与性质】2017年4月26日,海军成立68周年时,我国第一艘国产航母成功下水。建造航母需要大量的新型材料。航母的龙骨要耐冲击,航母的甲板要耐高温,航母的外壳要耐腐蚀。
-
(1) 镍铬钢抗腐蚀性能强,Ni2+最高能级电子的运动状态有种,铬元素在周期表中区。
-
(2) 航母甲板涂有一层耐高温的材料聚硅氧烷(结构如图所示),其中C原子杂化方式为杂化。

-
(3) 海洋是元素的摇篮,海水中含有大量卤族元素。
①根据下表数据判断:最有可能生成较稳定的单核阳离子的卤素原子是(填元素符号)
氟
氯
溴
碘
第一电离能(kJ/mol)
1681
1251
1140
1008
②根据价层电子对互斥理论,预测ClO3-的空间构型为形,写出一个ClO3-的等电子体的化学符号。
③已知高碘酸有两种形式,化学式分别为H5IO6(
 )和HIO4 , 前者为五元酸,后者为一元酸。请比较二者酸性强弱:H5IO6HIO4(填“>”“<”或“= ”)
)和HIO4 , 前者为五元酸,后者为一元酸。请比较二者酸性强弱:H5IO6HIO4(填“>”“<”或“= ”) -
(4) 海底金属软泥是在洋海底覆盖着的一层红棕色沉积物,蕴藏着大量的资源,含有硅、氧化铁、锰、锌等。Zn2+与S2-形成的一种晶体结构如图所示(黑球表示Zn2+ , 白球表示S2-)。则该晶体中与Zn2+等距且最近的S2-形成的立体图形为。已知该晶体的密度为ρg·cm-3 , 阿伏加德罗常数为NA , 该晶体中Zn2+和S2-原子之间的最短距离为体对角线的1/4,则该晶体中S2-和Zn2+之间的最短距离为pm。(写出计算式即可)

如图为元素周期表中前四周期的一部分,若B元素的核电荷数为x , 则这五种元素的核电荷数之和为()

A . 5x+10
B . 5x
C . 5x+14
D . 5x+16
下列各组元素中,属于同一主族的是( )
A . N、Cl
B . O、S
C . H、Mg
D . Na、 Al
人工合成的18F在衰变过程中会生成稳定的不具放射性的18O。下列说法正确的是( )
A . 18O核内中子数为8
B . 18F和18O互为同位素
C . 18F和18O电子数相同而中子数不同
D . 18F与19F最外层电子数相等
根据原子结构特征,可以把 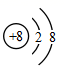 、
、 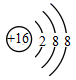 、
、 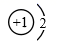 三种微粒归为一类。下列微粒中,可以归入此类的微粒是( )
三种微粒归为一类。下列微粒中,可以归入此类的微粒是( )
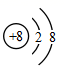 、
、  、
、
A . 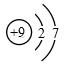 B .
B .  C .
C . 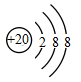 D .
D . 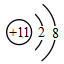
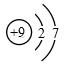 B .
B .  C .
C .  D .
D . 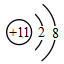
已知X、Y、Z、W原子序数都不超过18,它们的离子aX(n+1)+、bYn+、cZ(n+1)-、dWn-具有相同的电子层结构,则下列说法正确的是( )
A . 原子序数:a>b>c>d
B . 离子半径:X(n+1)+>Yn+>Z(n+1)->Wn-
C . 离子氧化性:X(n+1)+< Yn+
D . 单质氧化性:Z<W
冬季下雪后,城市道路常使用融雪剂,其主要成分的 化学式为 XY2 , X、Y 均为周期表前 20 号元素,其阳离子和阴离子电子层结构相同,且 1 mol XY2 含有 54 mol 电子。
-
(1) Y在周期表中的位置为,该融雪剂的化学式是,该物质中化学键类型是。
-
(2) 元素 D、E 原子的最外层电子数均是其电子层数的2倍,D与Y相邻,则D的原子结构示意图是;D 与 E 能形成一种结构类似于 CO2 的三原子分子,且每个原子均达到了 8e-稳定结构,该分子的电子式为。
-
(3) 元素Z的M层电子比L层少5个,Z与NaOH溶液反应的现象是,反应的离子方程式为。
已知某元素的+2价离子的电子排布式为1s22s22p63s23p6 , 则该元素在周期表中属于( )
A . 第3周期ⅤB族
B . 第4周期ⅡB族
C . 第4周期Ⅷ族
D . 第4周期ⅡA族
X、Y、Z、W,R是原子序数依次增大的五种元素,且原子的核电荷数均小于18,X元素的单质是标准状况下密度最小的气体,Y和Z元素的原子核外电子总数均为电子层数的4倍,W元素原子的M层电子数是K层的3倍。
-
(1) X元素的一种核素原子核内只有1个中子,写出这种核素的符号。
-
(2) 1mol
 所含电子的数目为。
所含电子的数目为。
-
(3) 由X、Y、Z三种元素构成的常见化合物与稀硫酸反应的化学方程式为。
-
(4) W的一种氧化物为常见空气污染物。写出该氧化物与过量
 溶液反应的化学方程式为。
溶液反应的化学方程式为。
-
(5) 写出Z和R两种元素形成的化合物在水溶液中的电离方程式。
下列关于化学用语的表述正确的是( )
A . BF3的电子式: 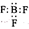 B . Fe2+的原子结构示意图:
B . Fe2+的原子结构示意图: 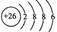 C . 中子数为143的U原子:
C . 中子数为143的U原子:  D . 乙醇的结构简式:C2H6O
D . 乙醇的结构简式:C2H6O
 D . 乙醇的结构简式:C2H6O
D . 乙醇的结构简式:C2H6O
短周期主族元素W、X、Y、Z的原子序数依次增大,基态W的原子2p轨道处于半充满状态,基态X的原子的2p能级上只有一对成对电子,基态Y的原子的最外层电子运动状态只有1种,元素Z与X同主族。下列说法不正确的是( )
A . 第一电离能: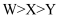 B . 电负性:
B . 电负性: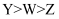 C . 简单离子半径:
C . 简单离子半径: D . 这些元素中有3种属于p区元素
D . 这些元素中有3种属于p区元素
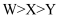 B . 电负性:
B . 电负性: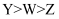 C . 简单离子半径:
C . 简单离子半径: D . 这些元素中有3种属于p区元素
D . 这些元素中有3种属于p区元素
下列有关物质性质的比较,说法错误的是( )
A . 碱性: B . 酸性:
B . 酸性: C . 金属性:
C . 金属性: D . 原子半径:
D . 原子半径:
 B . 酸性:
B . 酸性: C . 金属性:
C . 金属性: D . 原子半径:
D . 原子半径:
最近更新



