物质除杂或净化 知识点题库

-
(1) 小试管中澄清石灰水变浑浊,说明碳酸氢钠受热有 生成(填化学式)
-
(2) 通过上述实验,下列归纳出的碳酸氢钠性质或推理正确的有 (填编号)。
A.NaHCO3能与NaOH溶液发生反应
B.NaHCO3受热易分解:

C.加热时NaHCO3比Na2CO3易分解
D.无法比较NaHCO3与Na2CO3受热分解的难易程度
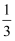 体积的水,盖紧瓶盖,振荡
体积的水,盖紧瓶盖,振荡
选项 | 物 质 | 杂 质 | 除杂药品或方法 |
A | CaCl2溶液 | 盐酸 | 过量的碳酸钙、过滤 |
B | CaO | CaCO3 | 适量稀盐酸 |
C | N2 | O2 | 灼热的钢网 |
D | CO | CO2 | 足量的氢氧化钠溶液、浓硫酸 |
序号 | 物质 | 杂质 | 试剂 | 操作 |
A | Fe | Fe2O3 | 盐酸 | 结晶 |
B | NH4HCO3 | NaCl | ﹣ | 加热 |
C | Cu(NO3)2溶液 | BaCl2 | AgNO3溶液 | 过滤 |
D | O2 | 水蒸气 | 浓硫酸 | 洗气 |
选项 | 实验目的 | 实验操作 |
A | 验证二氧化碳能与水反应生成碳酸 | 向收集满二氧化碳的集气瓶中加入约 |
B | 检验氢氧化钠溶液已部分变质 | 取少量溶液,滴加足量的氯化钡溶液,过滤,向滤液中滴加酚酞溶液 |
C | 探究稀硫酸与氢氧化钠溶液是否完全反应 | 向反应后所得的溶液中滴加硝酸银溶液 |
D | 除去CO2中的SO2气体和水蒸气 | 将混合气体依次通过NaOH溶液和浓硫酸 |
①高温下用碳还原二氧化硅制得粗硅;
②粗硅与干燥HCl气体反应制得SiHCl3:Si+3HCl ![]() SiHCl3+H2;
SiHCl3+H2;
③SiHCl3与过量H2在1 000~1 100℃反应制得纯硅已知SiHCl3能与H2O强烈反应,在空气中易自燃.
请回答下列问题:
-
(1) 粗硅与HCl反应完全后,经冷凝得到的SiHCl3(沸点33.0℃)中含有少量SiCl4(沸点57.6℃)和HCl(沸点﹣84.7℃),提纯SiHCl3采用的方法为.
-
(2) 用SiHCl3与过量H2反应制备纯硅的装置如下(热源及夹持装置略去):

①装置B中的试剂是.装置C中的烧瓶需要加热,其目的是.
②反应一段时间后,装置D中观察到的现象是,装置D不能采用普通玻璃管的原因是,装置D中发生反应的化学方程式为.
③为保证制备纯硅实验的成功,操作的关键是检查实验装置的气密性,控制好反应温度以及.

根据流程图回答:
-
(1) 沉淀B化学式是 , 试剂甲是 , 滤液C中溶质成分有。
-
(2) 根据以上方案得到NaCl固体测定含有杂质,同学们通过分析后对上述方案作出改进:在步骤Ⅴ滤液C蒸发结晶之前,先滴加足量的 , 既能除去所含杂质,又能有效防止新杂质的引入,上述反应的化学方程式为。
-
(3) 为测定原混合物中氯化钠的质量分数,同学们提出了如下两个数据测定方案。
方案1:称量混合物A的总质量和干燥的沉淀B或CaCl2固体的质量,并进行计算;
方案2:称量混合物A的总质量和实验改进后所得纯净氯化钠固体的质量,并进行计算。
请你判断:上述所选称量数据不合理的是(填:“方案1”或“方案2”)。
理由是。
下列操作顺序中,不正确的是( )
| 物质 | 杂质 | 除杂质应选用的试剂和操作方法 | |
| A | CO2 | CO | 通入O2点燃 |
| B | NaOH固体 | Na2CO3固体 | 加入过量盐酸,蒸发 |
| C | KNO3溶液 | KOH溶液 | 加入适量的CuSO4溶液,过滤 |
| D | Cu(NO3)2溶液 | AgNO3溶液 | 加入过量的铜粉,过滤 |
-
(1) 汗水中产生咸味的含钠物质是由(填“原子”、“分子”或“离子”)构成的。
-
(2) 向滴有酚酞试液的氢氧化钠溶液中加入下列物质(可多选),可以证明氢氧化钠溶液中OH-能使酚酞试液变红,
①稀盐酸②KNO3③CaCl2溶液④MgSO4溶液
-
(3) 下列是分析放置在空气中的NaOH固体的相关实验,其中不合理的是A . 证明变质:取样,加入过量稀盐酸,观察是否有气泡 B . 确定成分:取样,加入适量的Ca(OH)2溶液,过滤,向滤液中滴加酚酞溶液 C . 除去杂质:取样,加水溶解,加入适量的Ca(OH)2溶液,过滤

-
(1) 实验前要检查A装置的气密性,具体操作是。
-
(2) D装置中的试剂是。
-
(3) 实验中看到B中无水硫酸铜变蓝色,这说明产生的气体中含有水蒸气。为了检验气体中还可能含有的杂质,可将F装置连接到上述装置 (填字母)之间
| 选项 | 待提纯的物质 | 选用的试剂 | 操作方法 |
| A | Na2SO4(NaOH) | 稀硫酸 | 加过量的稀硫酸、蒸发结晶 |
| B | NaCl(Na2CO3) | BaCl2溶液 | 加入适量的BaCl2溶液,过滤,将滤液蒸发结晶 |
| C | KCl(K2CO3) | 稀盐酸 | 加过量的稀盐酸 |
| D | CaO(CaCO3) | 稀盐酸 | 加入足量的稀盐酸,过滤、洗涤、干燥 |
| 选项 | 物质 | 杂质 | 所选试剂(或操作) |
| A | 盐酸 | 硫酸 | 加适量氯化钡溶液、过滤 |
| B | CaCl2 | CaCO3 | 加水溶解、过滤、蒸发 |
| C | Fe | Cu | 加过量稀盐酸、过滤 |
| D | CO | CO2 | 通入足量氢氧化钠溶液、干燥 |
| 选项 | 待提纯物质 | 选用试剂 | 操作方法 |
| A | CuCl2(MgCl2) | 镁片 | 过滤 |
| B | CaO(CaCO3) | 盐酸 | 蒸发 |
| C | Cu(Fe) | 稀硫酸 | 过滤 |
| D | FeCl3溶液(盐酸) | 氢氧化钠溶液 | 滴加 |
| 选项 | 物质 | 杂质 | 试剂或方法 |
| A | CO | CO2 | 通过灼热的氧化铜粉末 |
| B | NaCl | Na2CO3 | 滴入适量稀盐酸,过滤 |
| C | KNO3溶液 | Ba(NO3)2 | 滴加适量Na2SO4溶液,过滤 |
| D | H2 | HCl | 先通过NaOH溶液,再通过浓硫酸 |

供选试剂:K2SO4溶液、Na2CO3溶液、K2CO3溶液、盐酸、稀硫酸。
-
(1) 步骤①中,分离A、B的实验使用的试剂是。
-
(2) 沉淀 B 表面残留少量滤液,需用蒸馏水多次洗涤,为了检验沉淀 B 是否洗涤干净, 可向步骤②的最后一次洗涤液中加入的试剂是 (双选,填序号)。A . 氢氧化钠溶液 B . 氯化钙溶液 C . 氯化钠溶液 D . 硝酸银和稀硝酸混合溶液
-
(3) 步骤③中,发生反应的化学方程式为。
-
(4) 要达到预期的目的,还需要改进的方法为。
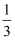 体积的滴有酚酞的水,振荡
体积的滴有酚酞的水,振荡


