物质除杂或净化 知识点题库
鉴别 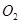 、CO、
、CO、 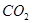 三种气体,可行简便的方法是 ( )
三种气体,可行简便的方法是 ( )
选项 | 物质 | 杂质(少量) | 试剂及操作方法 |
A | 氧化钙 | 石灰石 | 高温 |
B | 稀盐酸 | 稀硝酸 | 加入过量的硝酸银溶液,过滤 |
C | 氯化钠 | 泥沙 | 加入足量的水溶解、蒸发、结晶 |
D | 氨气 | 水蒸气 | 通过足量的氢氧化钠固体干燥 |
序号 | 物质 | 杂质 | 所选试剂 |
A | NaOH | Na2CO3 | 适量稀盐酸 |
B | MnO2 | KCl | 足量水 |
C | Cu | CuO | 足量稀硫酸 |
D | CaCl2溶液 | 盐酸 | 足量CaCO3 |
实验目的 | 实验方案 | |
A | 鉴别AgNO3溶液与NaNO3溶液 | 分别滴加稀盐酸,振荡,观察是否产生沉淀 |
B | 除去CO中混有的CO2 | 将混合气体通过灼热的氧化铜 |
C | 鉴别纯铝和硬铝 | 将两者相互刻画,比较硬度 |
D | 检验集气瓶中是否集满氧气 | 将带火星的木条伸入集气瓶口,观察木条能否复燃 |
-
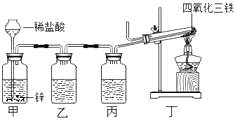
(1) 广口瓶乙中盛放的物质是.
-
(2) 导管在广口瓶乙和丙中的插入情况相同,请在图中画出导管在广口瓶乙中的插入情况.
-
(3) 加热前,如何用实验检验装置中的空气是否排尽?
-
(4) 普通铁粉不易燃烧,而“引火铁”易自燃下列对此现象的认识中,错误的是 .A . “引火铁”的自燃是吸热反应 B . “引火铁”的自燃是氧化反应 C . “引火铁”的自燃需要达到它的着火点 D . “引火铁”比普通铁粉更易与氧气反应.
物 质 | 选用的方法或试剂 | |
A | 空气和氮气 | 带火星的木条 |
B | 水和过氧化氢 | 二氧化锰 |
C | 氧气和二氧化碳 | 通入澄清石灰水 |
D | 红磷和白磷 | 颜色 |
|
反应时间(秒) |
20 |
40 |
60 |
80 |
100 |
120 |
140 |
|
|
收集到的气体体积(毫升) |
甲金属 |
25 |
60 |
95 |
130 |
160 |
170 |
170 |
|
乙金属 |
30 |
75 |
120 |
150 |
150 |
150 |
150 |
|
-
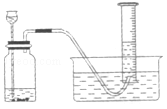
(1) 由实验结果可知:金属活动性较强的是。
-
(2) 为了使得到的实验数据准确,小科开始收集气体的时间点应该是 。A . 导管口一有气泡冒出时 B . 冒出气泡连续且均匀时 C . 检验产生的气体纯净时
-
(3) 根据已有实验数据,要比较甲、乙两种金属的相对原子质量大小,还需知道 。A . 参加反应的硫酸质量 B . 生成物中金属元素的化合价
-
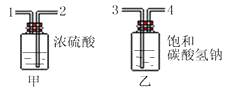
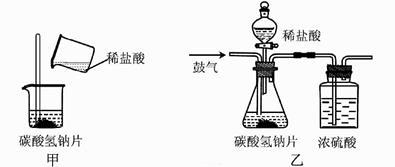
(1) 小科认为,要测定药片中碳酸氢钠的含量,实验中需要采集两个数据:一是测出碳酸氢钠片样品的质量;二是根据碳酸氢钠与盐酸的反应原理,通过实验测出反应生成的质量。
-
(2) 小科按如图甲的实验方案,取药片和足量的稀盐酸进行实验,通过测量反应前后总质量的变化来采集实验数据。同学们认为,测得碳酸氢钠的质量分数会偏大,原因是(答出一点即可)。
-
(3) 为减小实验误差,小科又设计了如图乙的实验方案,取药片和足量的稀盐酸进行了三次实验,采集的实验数据如表:
实验序号
1
2
3
碳酸氢钠片样品质量/克
3.0
3.0
3.0
反应前总质量/克
193.8
194.6
193.6
反应后总质量/克
192.6
193.6
192.5
二氧化碳质量/克
请计算药片中碳酸氢钠的质量分数。
【发现问题】菠菜为什么不能与豆腐同食?
【查阅资料】a.制作豆腐需要加入石膏(主要成分:CaSO4);
b.菠菜中含有草酸、草酸盐等成分;
c.草酸钙是一种既不溶于水也不溶于醋酸的白色固体,是诱发人体结石的物质之一。【提出猜想】菠菜与豆腐同食可能会产生人体不能吸收的沉淀物。
-
(1) 【设计实验】
实验步骤
实验现象
实验结论
①将菠菜在少量开水中煮沸2~3min,取1~2mL滤液于试管中,并滴加少量溶液
产生白色沉淀
有草酸钙生成
②在步骤①的沉淀物中加入过量醋酸
沉淀部分溶解,且产生气泡
被溶解的沉淀一定不是
-
(2) 【发现新问题】被溶解的沉淀是什么?产生的气体又是什么?于是她又设计如下实验进一步探究:
实验步骤
实验现象
实验结论
③将步骤②产生的气体通入 中
产生的气体是 ;步骤②被溶解的沉淀是碳酸钙
-
(3) 【反思与应用】
①家庭中常常将菠菜放在开水中煮沸2~3min捞出后再烹饪,其目的是;
②联想到人体胃液中含有盐酸,请提出一个你想要探究的新问题:。
| 选项 | 实验操作 | 现象 | 解释或结论 |
| A | 将水加入浓硫酸中配置成稀硫酸,将镁条置于其中 | 有气泡产生 | Mg是活泼金属 |
| B | 验纯后,将纯净氢气直接在空气中点燃 | 产生淡蓝色火焰 | 氢气可以在空气中安静的燃烧 |
| C | 向一未知无色溶液中,加入适量的AgNO3溶液 | 有白色沉淀产生 | 该无色未知溶液中一定有Cl- |
| D | 将ag的铁钉投入到硫酸铜溶液中,反应一段时间后,取出、洗净、烘干、称量为bg | 铁钉上覆盖一层红色的物质 | 金属活动顺序为:Fe>Cu,且析出铜的质量为(b-a)g |
| 选项 | 物质 | 杂质 | 试剂或方法 |
| A | NaCl固体 | 泥沙 | 加水溶解、过滤、蒸发 |
| B | NaCl溶液 | Na2CO3 | 滴加硫酸溶液至不再产生气泡 |
| C | KNO3溶液 | Ba(NO3)2 | 滴加适量K2SO4溶液、过滤 |
| D | CO2 | CO | 通过灼热的氧化铜 |
| 选项 | 实验目的 | 实验原理 | 主要操作方法 |
| A | 除去粗盐中的泥沙 | 各成分的溶解性差异 | 蒸发 |
| B | 分离水与酒精的混合物 | 各成分的密度差异 | 蒸馏 |
| C | 鉴别稀盐酸和稀硫酸 | 酸根离子的化学性质差异 | 加碳酸钠溶液,观察产生气泡快慢 |
| D | 除去FeSO4、CuSO4混合溶液中的CuSO4 | 金属活动性差异 | 加过量铁粉,充分反应后过滤 |
| 选项 | 实验目的 | 所选试剂 |
| A | 鉴别稀硫酸和稀盐酸 | 硝酸银溶液 |
| B | 鉴别硝酸铵固体和氢氧化钠固体 | 水 |
| C | 除去CaCl2溶液中的稀盐酸 | 碳酸钙 |
| D | 除去N2中混有的O2 | 灼热的铜网 |
| 选项 | 物质 | 所含杂质 | 除去杂质的方法 |
| A | 铁锈 | KNO3粉末 | 加入足量水,过滤 |
| B | CO2气体 | CO | 通入氢氧化钠溶液 |
| C | NaOH溶液 | Na2CO3 | 加入足量稀盐酸至不再产生气泡 |
| D | NaCl溶液 | BaCl2 | 加入适量硫酸钾,充分反应,过滤 |
| 选项 | 物质 | 杂质 | 除杂质的方法 |
| A | | | 加适量水溶解、过滤、蒸发结晶 |
| B | | | 将气体通入足量氢氧化钠溶液 |
| C | 银粉 | 锌粉 | 加入过量硫酸亚铁溶液,过滤 |
| D | | | 加适量硝酸钙溶液,过滤 |
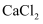
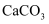


 溶液
溶液



