影响化学反应速率的因素 知识点题库
研究和控制化学反应条件有重要意义.
(1)同学们想探究双氧水的溶质质量分数对反应速率的影响.在其他条件相同的情况下进行了三次实验,记录各收集一瓶相同体积氧气所需要的时间.
实验 | 30%双氧水的质量(g) | 加入的水的体积(mL) | 二氧化锰质量(g) | 收集时间(s) |
1 | 10 | 40 | 5 | 200 |
2 | 20 | 30 | 5 | 100 |
3 | 30 | 20 |
| 67 |
①取用二氧化锰的仪器是图1中的 (选填编号).

②写出上述反应的化学反应方程式 .
③实验3中,加入的二氧化锰质量为 g.
④相同条件下,实验3产生氧气的速率最快,说明 .
(2)同学通过查阅资料得知,双氧水在70℃以上会较快分解产生氧气.为了验证加热双氧水也可以产生氧气,同学们选择图2装置(气密性良好)进行实验.实验中观察到试管内产生气泡,但将带火星的木条放在导管口没有复燃,可能的原因是 , 同学分析原因后,采用了法收集气体,再检验,证明加热双氧水也可产生氧气.
序号 | 化学反应事实 | 影响化学反应的因素 |
A | 铁丝在空气中很难燃烧,而在氧气中能剧烈燃烧 | 反应物浓度 |
B | 碳在常温下不与氧气发生反应,而在点燃时能与氧气反应 | 反应温度 |
C | 过氧化氢溶液在常温下较难分解,而在加入二氧化锰后迅速分解 | 催化剂 |
D | 铜片在空气中很难燃烧,铜粉在空气中较易燃烧 | 反应物的种类 |
序号 | 化学反应事实 | 影响化学反应的因素 |
A | 铁丝在空气中很难燃烧,而在氧气中能剧烈燃烧 | 反应物浓度 |
B | 碳在常温下不与氧化铜反应,而在高温时能与氧化铜反应 | 反应温度 |
C | 双氧水在常温下较难分解,而在加入二氧化锰后迅速分解 | 催化剂 |
D | 大木桩在空气中很难燃烧,小木条在空气中较易燃烧 | 反应物的种类 |
序号 | 化学反应事实 | 影响化学反应的因素 |
A | 纸在空气中常温不会燃烧,而点燃后可以燃烧 | 反应温度 |
B | 肉质食物易腐烂,而加了防腐剂后却不易变质 | 催化剂 |
C | 大块木头不易点燃,而刨成刨花却易点燃 | 反应物种类 |
D | 木炭在氧气中燃烧比在空气中更剧烈 | 反应物浓度 |
在制取CO2的实验中,小刚发现选用颗粒大小不同的大理石与稀盐酸反应时,CO2的产生速度有差异。经思考后,小刚设计了如图所示的实验及记录表。请你完成下列问题:

实验 序号 | 温 度 (℃) | 大 理 石 | 稀 盐 酸 | ||
质量(g) | 颗 粒 | 体积(ml) | 质量分数(%) | ||
① | 20 | 5 | 大 | 20 | 5 |
② | 20 | 5 | 小 | 20 | 5 |
③ | 20 | 5 | 小 | 20 | 10 |
-
(1) 实验①②探究的是大理石和稀盐酸的反应速度与的关系。
-
(2) 探究大理石和稀盐酸的反应速度与稀盐酸质量分数的关系,应选择的实验组是。
-
(3) 如图所示,如要检验该集气瓶是否已收集满CO2 , 你的方法是。
-
(4) 如要判断产生的CO2速度,最后一列需填写收集满一瓶CO2所需要的。
-
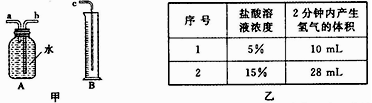
(1) 图甲中A,B仪器可以组装一套测量气体体积的装置,利用该装置时A中管接c。
-
(2) 他选用2克完全相同的锌片分别和同体积5%,15%的稀盐酸进行实骏。获得表格数据.由此推断实验是通过来体现反应快慢的.
-
(3) 小敏分析数据得到如下结论:锌与盐酸反应快慢与盐酸浓度有关。盐酸浓度越大反应越快。其他同学认为结论不可靠,他们的依据是:。
-
(4) 实验中小敏发现锌与盐酸反应时,一开始产生氢气速度并没有随盐酸浓度的减少而减慢,查阅资料得知化学反应中往往伴随着能量变化。由此作出猜想:锌与盐酸反应快慢还与有关.
| 选项 | 化学反应事实 | 影响反应因素 |
| A | 红热的铁丝在空气中很难燃烧,在氧气中能剧烈燃烧 | 反应物浓度 |
| B | 碳在常温下不与氧气反应,在点燃时能与氧气反应 | 反应的温度 |
| C | 常温下,过氧化氢溶液分解速率缓慢,加入二氧化锰后迅速分解 | 催化剂 |
| D | 铜片在空气中很难燃烧,铜粉在空气中较易燃烧 | 反应物的种类 |
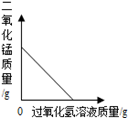 B . 等质量 CaCO3分别与等体积等质量分数的稀盐酸(足量)反应
B . 等质量 CaCO3分别与等体积等质量分数的稀盐酸(足量)反应  C . 等质量的Fe粉和Zn粉分别与足量等浓度的稀硫酸反应
C . 等质量的Fe粉和Zn粉分别与足量等浓度的稀硫酸反应 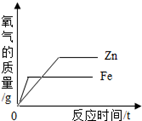 D . 向硝酸铜和硝酸的混合溶液中逐滴加入氢氧化钠溶液
D . 向硝酸铜和硝酸的混合溶液中逐滴加入氢氧化钠溶液 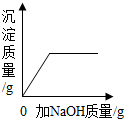
|
实验序号 |
1 |
2 |
3 |
4 |
|
金属 |
丝状 |
粉末状 |
丝状 |
丝状 |
|
稀硫酸质量分数 |
5% |
5% |
10% |
10% |
|
溶液温度/℃ |
20 |
20 |
20 |
35 |
|
金属消失的时间/s |
500 |
50 |
125 |
50 |
分析上述数据,回答下列问题:
-
(1) 该实验需要用到的测量仪器除了天平、量筒、秒表之外还应该有;
-
(2) 小明是比较分析来判断反应的速率;
-
(3) 通过实验1和3,可得出的实验结论是。
 B .
B .  C .
C .  D .
D . 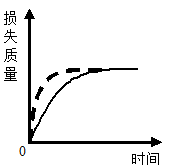

-
(1) 请完成以下实验设计表。
实验编号
实验目的
温度/℃
pH
浓度/(mg·L-1)
H2O2
Fe2+
①
为②③提供参照
25
3
204
16.8
②
探究温度对降解反应速率的影响
3
204
16.8
③
探究溶液pH对降解反应速率的影响
25
10
204
16.8
-
(2) 进一步实验发现,温度过高时,降解反应较难发生。请从所用试剂H2O2的角度分析原因。
-
(3) 由实验③可以得出的结论是。
-
(4) 为测定不同时间内有机物降解的浓度,需在不同时间从反应器中取样,并使所取样品中的降解反应立即停止。根据图示信息,请写出迅速停止反应的一种方法 。
|
实验编号 |
盐酸的质量分数/% |
反应温度/℃ |
铝丝消失的时间/秒 |
|
① |
3 |
20 |
500 |
|
② |
6 |
20 |
300 |
|
③ |
6 |
30 |
80 |
-
(1) 分析实验数据,得出影响铝丝与盐酸反应快慢的因素有。
-
(2) 小明实验时误用了稀硫酸与铝丝进行反应,意外发现铝丝与稀硫酸反应现象不明显。查阅资料发现钠离子、硫酸根离子不影响铝丝和酸反应的快慢,那么,为什么铝丝易与盐酸反应而难与稀硫酸反应呢?他认为是氯离子对铝丝和酸反应起促进作用。请利用下列器材帮助小明设计实验方案。(要求写出实验步骤、预期现象和结论) 。
可提供的实验器材:清水、稀HCl、稀H2SO4溶液、NaCl溶液、Na2SO4溶液;试管、水槽。
-
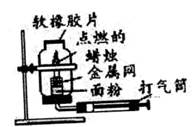
(1) 吹散面粉的目的是增大面粉与空气的。
-
(2) 软橡胶片被冲飞时内能转化为 。
-
(3) 蜡烛熄灭的原因是。


-
(1) 写出上述生成红褐色氢氧化物的化学方程式。。
-
(2) 海绵铁除去溶解氧的反应中,氧气表现了性(选填“氧化”或“还原”)。跟成分相同的普通铁块相比较,海绵铁除氧效果要好得多,原因是。
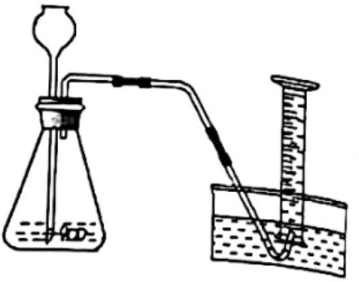
①检查装置气密性。
②取5毫升10%H2O2溶液,放入锥形瓶中,并加入1克MnO2。
③观察记录收集10亳升气体所需的时间。
④分别换用1克红砖粉末和1克CuO代替1克MnO2 , 重复实验步骤②和③,
记录数据如下表。
|
试剂 |
①MnO2 |
②红砖粉末 |
③CuO |
|
时间/秒 |
10 |
60 |
20 |
-
(1) 本实验装置气密性的操作是。
-
(2) 实验中观察记录收集10 亳升气体所需时间有2种方案:
方案一:等水中导管口气泡连续均匀冒出时开始收集,并开始计时。
方案二:水中导管口气泡一冒出马.上开始收集。并开始计时。
为了提高实验的准确性,你选择的方案是。
-
(3) 根据表中数据,小明认为MnO2和CuO对H2O2分解存催化作用,而红砖粉末无催化作用,小华对该结论有质疑,认为还需补充实验才能得出结论、小华的补东实验是。
【实验原理】CaCO3+2HCl═CaCl2+H2O+CO2↑
【发生装置】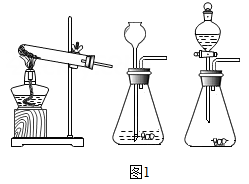
-
(1) 结合实验原理,图1中发生装置可用于实验室制取CO2气体的是;(填字母)
-
(2) 【实验探究】
探究Ⅰ.影响因素探究
在制取CO2气体时,为了探究影响反应快慢的因素,小组同学进行了四组实验,如表所示
实验组别
甲
乙
丙
丁
大理石的质量/g、颗粒大小
m块状
m块状
m粉末状
m粉末状
盐酸的体积/mL、浓度
V稀盐酸
V浓盐酸
V稀盐酸
V浓盐酸
若探究盐酸的浓度对上述反应的影响,可选择实验甲与(选填实验组别)进行对照。
-
(3) 探究Ⅱ.性质探究
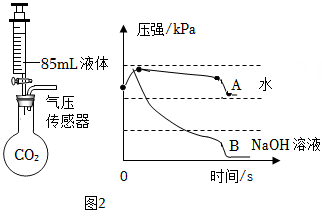
做CO2与NaOH溶液发生反应的验证实验时,同学们将NaOH溶液加入到充满CO2气体且质地较软的塑料瓶中,观察到塑料瓶变扁,由此得到CO2与NaOH发生反应的结论。但有同学认为上述现象产生的原因还可能是CO2气体溶于水导致气压减小。
为回答该同学的质疑,小科进行了如下实验:在两个250mL的烧瓶中分别充满CO2气体,通过注射器同时向两个烧瓶中分别注入同体积的水和NaOH溶液,最后得到烧瓶内压强与时间的关系曲线(如图2所示)。由此,小科得出CO2气体溶于水会导致塑料瓶变扁,同时CO2与NaOH也发生了化学反应的结论。
结合图2中A、B曲线变化特点,写出能证明CO2与NaOH发生了化学反应的证据。
-
(4) 【拓展提高】小组同学完成某石灰石样品中CaCO3的质量分数测定,其方法是:将样品与一定量的稀盐酸反应,测定反应后生成的CO2质量,再根据CO2的质量求出样品中CaCO3的质量分数。
小组同学在实验室中组装了相应的实验装置(如图3)。小科利用该实验装置按如下步骤进行实验:
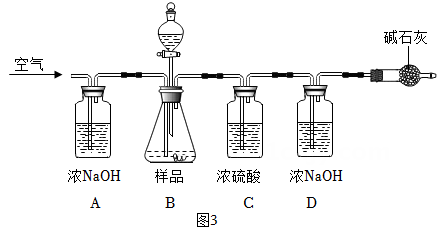
①先通一段时间的空气
②称量D装置的质量为m1
③打开分液漏斗的活塞,将稀盐酸全部加入锥形瓶,待充分反应后,关闭活塞
④再次通空气一段时间
⑤再次称量D装置的质量为m2
有同学指出实验步骤③操作明显不合理,你认为该同学的理由是。



