复分解反应及其应用 知识点题库
下列物质在含有HCl和H2SO4的溶液中能大量共存的是( )
A . Na2CO3
B . NaOH
C . NaNO3
D . BaCl2
新型纳米材料MFe2Ox (3<x<4)中M表示+2价的金属元素,在反应中化合价不发生变化。常温下,MFe2Ox能使工业废气中的SO2转化为S,在反应中M的化合价不发生改变。转化流程如图所示,已知MFe2Oy中Fe为+3价。下列说法中,正确的是( )

A . SO2是该反应的催化剂
B . 该反应属于复分解反应
C . y的数值为4
D . MFe2Oy中M的质量分数大于MFe2Ox中M的质量分数
甲乙丙丁四种物质的转化关系如图所示.下列说法正确的是( )
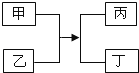
A . 若丙为沉淀,则甲、乙中一定有一种物质是碱
B . 若丙为气体,则甲、乙中一定有单质
C . 若丁为水,则该反应一定是复分解反应
D . 若甲、丁为单质,则该反应一定是置换反应
在下列类型的化学反应中,各元素的化合价一定不会发生变化的是( )
A . 化合反应
B . 分解反应
C . 置换反应
D . 复分解反应
下列反应不属于复分解反应的是( )
A . CuO+H2SO4═CuSO4+H2O
B . Na2CO3+2HCl═2NaCl+CO2↑+H2O
C . Cu(OH)2+2HCl═CuCl2+2H2O
D . Ca(OH)2+CO2═CaCO3↓+H2O
掌握初中化学中物质间反应规律是继续学习化学的必备知识。在下列物质中按要求选出能相互反应的组合(填物质编号如“①⑥”,如有多种组合,组合间用分号“;”相隔)。
①CO2 ②KNO3溶液 ③Ag ④CuSO4溶液 ⑤稀H2SO4 ⑥NaOH溶液 ⑦Fe ⑧NaCl溶液
-
(1) 常温下能发生置换反应的组合有。
-
(2) 常温下能发生复分解反应的组合有。
将Na2CO3溶液滴入Ba(OH)2溶液中至恰好完全反应,反应前后溶液中存在的离子如图。

-
(1) 实验可观察到的现象是。
-
(2) 能与Ba(OH)2溶液反应,产生上述实验现象的一种酸是(填写化学式)。
-
(3) 图形○代表的离子是(填离子符号)。
向甲物质中逐渐加入乙物质至过量。若x轴表示加入乙物质的质量,则下列选项与下图不相符合的是( )

| 选项 | 甲物质 | 乙物质 | y轴表示的含义 |
| A | 硫酸钡 | 稀盐酸 | 硫酸钡的质量 |
| B | 猪肝 | 过氧化氢溶液 | 猪肝的质量 |
| C | 饱和石灰水 | 生石灰 | 溶液的质量 |
| D | t℃的水 | 氯化钠 | t℃时氯化钠的溶解度 |
A . A
B . B
C . C
D . D
以下四个化学反应都有气体产生,其反应类型和产生的气体性质均正确的是( )
| 选项 | 化学反应方程式 | 反应类型 | 气体性质 |
| A | Fe+H2SO4=FeSO4+H2↑ | 置换反应 | 还原性 |
| B | 2H2O2 | 分解反应 | 可燃性 |
| C | 2KClO3 | 化合反应 | 氧化性 |
| D | CaCO3+2HCl=CaCl2+H2O+CO2↑ | 复分解反应 | 酸性 |
A . A
B . B
C . C
D . D
下列各组离子能在指定溶液中大量共存的一组是( )
A . 在稀盐酸中:Ba2+、CO32-、Zn2+
B . 在氢氧化钠溶液中:H+、Mg2+、Cl-
C . 在氯化钠溶液中:K+、Ca2+、NO3-
D . 在硝酸铵溶液中:Na+、Cu2+、OH-
生活垃圾分类投放回收后,含镉(Cd)固体废弃物必须及时处理。下面是处理过程中某一重要反应:CdSO4+Na2S=CdS↓+Na2SO4。该反应属于( )
A . 复分解反应
B . 置换反应
C . 分解反应
D . 化合反应
氢氧化钴[Co(OH)2]能与酸性溶液反应,可作涂料和清漆的干燥剂。制备方法为:
①Co+2HCl═CoCl2+H2↑;②CoCl2+2NaOH═Co(OH)2↓+2NaCl下列判断正确的是( )
A . ①为复分解反应
B . 钴的金属活动性比铜弱
C . 氢氧化钴可以干燥氯化氢气体
D . 氢氧化钴是一种难溶性碱
为了选择实验室制取二氧化碳的反应物,某实验小组取等量的碳酸盐和足量等浓度的酸,设计了以下四种反应物组合进行探究实验,结果如图所示。
实验①:碳酸钠粉末与稀盐酸
实验②:大理石粉末与稀盐酸
实验③:块状大理石与稀盐酸
实验④:块状大理石与稀硫酸

-
(1) 根据实验结果,他们决定选择块状大理石与稀盐酸来制取二氧化碳,发生反应的化学方程式为。他们不选择①的原因是。
-
(2) 探究结果说明,影响碳酸盐与酸反应产生二氧化碳快慢的因素有。
-
(3) 上述四种反应都属于反应(填基本反应类型)。
请根据酸、碱、盐的相关知识,回答下列问题:
-
(1) 氢氧化钠溶液敞口放置会变质,其原因是(用化学方程式表示)。
-
(2) 能将稀盐酸、硝酸钾溶液和氢氧化钠溶液一次性鉴别出来的试剂是。
-
(3) 从稀硫酸、氢氧化钠溶液和 碳酸钾溶液中,每次取出两种溶液混合,其能发生个复分解反应;写出有气体产生的化学反应方程式。
如图所示为A、B、C、D、E五种不同类别物质卡片组成的“化学拼图”,相邻两张卡片所标的物质的(或其溶液)间能发生反应。(本流程涉及均为初中科学常见的反应)

-
(1) 若C是铁锈,请写出盐酸除铁锈的方程式: 。
-
(2) 从初中科学知识的角度,根据图判断:属于复分解反应的组合是(填序号) 。
①A+B ②A+E
③A+D ④ D+E
质量守恒定律是化学反应中的重要规律。在催化、加热的条件下,A与B反应生成C和D,反应前后分子变化的微观示意图如右所示,下列说法正确的是( )
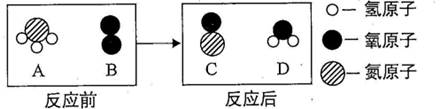
A . 该化学反应属于复分解反应
B . 4种物质中,C,D都属于氧化物
C . 反应前后,氮元素化合价保持不变
D . 该反应物中反应物A与B分子个数比是1:1
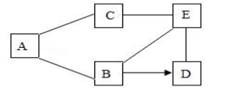
如图是铁、盐酸、氢氧化钙、硫酸铜和氯化镁五种物质的反应与转化关系,“﹣”表示两种物质之间能发生化学反应,“→”表示在一定条件下的物质转化。
-
(1) A 物质是(填化学式)。
-
(2) C 与 E 反应的基本类型是。
-
(3) 从物质反应规律分析,在单质、氧化物、酸、碱和盐中,能与 B 反应生成D 的物质有(填序号)。
①2 类②3 类③4类④5 类
下列表中物质、用途、反应方程式和基本反应类型完全正确的是( )
| 选项 | 物质 | 用途 | 反应方程式 | 反应类型 |
| A | 过氧化氢 | 制氧气 | H2O2=H2↑+O2↑ | 分解反应 |
| B | 稀硫酸 | 制氢气 | 2Fe+3H2SO4=Fe2(SO4)3+3H2↑ | 复分解反应 |
| C | 生石灰 | 干燥剂 | CaO+H2O=Ca(OH)2 | 化合反应 |
| D | 一氧化碳 | 冶炼金属 | CO+CuO | 置换反应 |
A . A
B . B
C . C
D . D
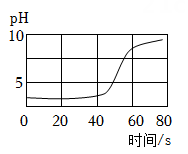
如图是小科做稀盐酸与氢氧化钠溶液混合实验时,记录的溶液pH随时间的变化曲线。
-
(1) 由图可知,实验操作过程是将 ;A . 稀盐酸逐渐加到氢氧化钠溶液中 B . 氢氧化钠溶液逐渐加到稀盐酸中
-
(2) 该反应属于基本反应类型中的;
-
(3) 当时间为60秒时,溶液中的溶质为。
下图是某反应前后的微观示意图,“O和“●”表示两种不同元素的原子。下列有关说法正确的是( )

A . 该反应没有单质生成
B . 该反应属于复分解反应
C . 该反应中,原子个数发生了改变  个数比为1:1
个数比为1:1
![]()
最近更新
 2H2O+O2↑
2H2O+O2↑ 2KCl+3O2↑
2KCl+3O2↑ Cu+CO2
Cu+CO2


