复分解反应及其应用 知识点题库
2005年的诺贝尔化学奖授予法国和美国的三位科学家,以表彰他们在烯烃(一类有机化合物)复分解反应研究方面的重要贡献。烯烃复分解反应的过程被化学家描述为“交换舞伴的交谊舞”。下列图示可以被理解为烯烃复分解反应过程的是( )
A .  B .
B .  C .
C . 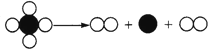 D .
D . 
 B .
B .  C .
C . 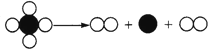 D .
D . 
从理论上判断复分解反应能否发生,一般不考虑的因素是( )
A . 反应物的溶解性
B . 生成物中有无气体、沉淀或水
C . 反应物中有无酸、碱、盐
D . 金属活动性强弱
甲、乙两工厂的生产污水中各含有下列五种离子中的三种(两厂含有一种相同的离子):H+、Cu2+、K+、NO3﹣、0H﹣ . 若两厂单独排放都会造成严重的污染.若将两厂的污水按一定比例混合,沉淀后污水会变成只含一种溶质的无色澄清溶液,此溶质可做化肥.下列关于污水的分析,正确的是( )
A . OH﹣和Cu2+来自同一工厂
B . Cu2+和K+来自同一工厂
C . K+和OH﹣来自同一工厂
D . H+和K+来自同一工厂
两种物质发生反应的微观示意图如图,下列说法正确的是( )

A . 反应前后物质的总质量保持不变
B . 该反应属于复分解反应
C . 反应前后分子种类保持不变
D . 该图可示意CO与O2的反应
酸、碱、盐的溶解性表是学习化学的重要工具,请完成:
离子 | OH﹣ | Cl﹣ | CO3﹣ | SO42﹣ |
H+ | ﹣﹣ | 溶 | 溶 | 溶 |
Na+ | 溶 | 溶 | 溶 | 溶 |
Ca2+ | 微 | 溶 | 溶 | 微 |
Ba2+ | 溶 | 溶 | 不 | 不 |
-
(1) 碳酸钠和碳酸钾的化学性质相似,是因为其溶液中都含有(填符号);检验方法和现象是:.
-
(2) 从表中选择离子组成两种化合物,按要求写化学方程式:
①一个同时有沉淀和气体生成的复分解反应;
②一个碱与盐的反应.
下列反应,属于复分解反应的是
A.Zn+Hg(NO3)2═Hg+Zn(NO3)2 B.Ca(OH)2+CO2═CaCO3↓+H2O
C.Fe(OH)2+2HCl═FeCl2+2H2O D.
将下列各组中的物质混合,若每组中最后一种物质过量,充分反应后过滤,则滤纸上仅留下一种不溶性物质(纯净物)的是( )
①氢氧化钠溶液、氯化镁溶液、硝酸;②氯化钡溶液、硝酸钠溶液、稀硫酸;③氯化铜溶液、氯化亚铁溶液、锌粒;④氯化钠溶液、硝酸银溶液、盐酸;⑤硫酸铁溶液、硝酸钠溶液、氢氧化钡溶液;
A . ②④
B . ②③
C . ③⑤
D . ①④
下列方程式书写和对反应类型的判断,都正确的是( )
A . 4Fe+3O2  2Fe2O3 化合反应
B . Cu+2AgCl=2Ag+CuCl2 置换反应
C . SiO2+3C
2Fe2O3 化合反应
B . Cu+2AgCl=2Ag+CuCl2 置换反应
C . SiO2+3C  SiC+2CO↑ 置换反应
D . BaCO3+2HCl=BaCl2+H2O+CO2↑ 复分解反应
SiC+2CO↑ 置换反应
D . BaCO3+2HCl=BaCl2+H2O+CO2↑ 复分解反应
 2Fe2O3 化合反应
B . Cu+2AgCl=2Ag+CuCl2 置换反应
C . SiO2+3C
2Fe2O3 化合反应
B . Cu+2AgCl=2Ag+CuCl2 置换反应
C . SiO2+3C  SiC+2CO↑ 置换反应
D . BaCO3+2HCl=BaCl2+H2O+CO2↑ 复分解反应
SiC+2CO↑ 置换反应
D . BaCO3+2HCl=BaCl2+H2O+CO2↑ 复分解反应
物质间反应的规律是继续学习科学的必备知识,在下列物质中按要求选出能相互反应的组合(填物质编号如“①⑥”,如有多种组合,组合间用分号“;”隔开)
①CO2 ②KNO3溶液 ③Ag ④CuSO4溶液 ⑤稀H2SO4 ⑥NaOH溶液 ⑦Fe
-
(1) 常温下能发生置换反应的组合有;
-
(2) 常温下能发生复分解反应的组合有。
通过下列化学反应不能达到目的是( )
A . 制氯化铁:2Fe+3CuCl2=2FeCl3+3Cu
B . 实验室制取氢气:Zn+H2SO4=ZnSO4+H2↑
C . 用硝酸钡溶液区别氢氧化钠溶液和硫酸钾溶液:K2SO4+Ba(NO3)2=BaSO4↓+2KNO3
D . 用氢氧化铝治疗胃酸过多症:Al(OH)3+3HCl=AlCl3+3H2O
我国著名制碱专家侯德榜通过长期的研究,改良了索尔维制碱法,提高了制碱效率。在侯式制碱的原理中,有一条反应是:NH4HCO3+NaCl=NH4Cl+ NaHCO3↓。这反应属于( )
A . 复分解反应
B . 分解反应
C . 化合反应
D . 置换反应
电闪雷鸣的雨天,空气中发生的雷电固氮反应如下:①N2+O2═2NO②2NO+O2═2NO2 ③3NO2+H2O═2HNO3+NO,有关判断正确的是( )
A . NO气体由一个N原子和一个0原子构成
B . HNO3属于酸
C . 这些化合物中N元素化合价最高为+4价
D . 反应③属于复分解反应
有关专家提出了“以废治废”的治理污染新思路,并且起到了一定的成效。如冶炼钢铁时,为减少煤中硫燃烧生成的二氧化硫所造成的污染,一般是在煤燃烧时添加生石灰或石灰石进行固硫(主要是利用氧化钙与二氧化硫反应生成亚硫酸钙)。 根据这一原理,有人将造纸厂回收的碱白泥(主要成分:CaCO3和NaOH)掺进煤中进行固硫。用碱白泥固硫时,可能发生了下列化学反应①S+O2  SO2②CaCO3
SO2②CaCO3  CaO+CO2↑③SO2+2NaOH==Na2SO3+H2O④CaCO3+2NaOH=Na2CO3+Ca(OH)2⑤SO2+CaO
CaO+CO2↑③SO2+2NaOH==Na2SO3+H2O④CaCO3+2NaOH=Na2CO3+Ca(OH)2⑤SO2+CaO  CaSO3
CaSO3
 SO2②CaCO3
SO2②CaCO3  CaO+CO2↑③SO2+2NaOH==Na2SO3+H2O④CaCO3+2NaOH=Na2CO3+Ca(OH)2⑤SO2+CaO
CaO+CO2↑③SO2+2NaOH==Na2SO3+H2O④CaCO3+2NaOH=Na2CO3+Ca(OH)2⑤SO2+CaO  CaSO3
CaSO3下列说法不正确的是( )
A . ①是氧化反应,也是化合反应
B . 生成物都是含氧化合物
C . ③属于复分解反应
D . 确定能发生的化学反应有①②③⑤
比较归纳是科学学习中的常用方法。若以下的物质转化都由一步反应完成:①Zn→ZnCl2②Zn(OH)2→ZnCl2 ③ZnCO3→ZnCl2。则( )
A . 三种转化发生的都是复分解反应
B . 三种转化都必须加入盐酸才能进行
C . 只有②发生了中和反应
D . 三种转化的生成物中都有水
某兴趣小组为了探究稀硫酸的化学性质,做了以下实验,请回答问题:

-
(1) 试管A中的现象是:;反应后试管B中一定有的阳离子是(写离子名称)。
-
(2) 实验发现试管C中出现蓝色溶液,固体全部溶解;试管D中出现沉淀。接着往试管D中逐渐加入氢氧化钠溶液,产生沉淀的质量与加入氢氧化钠溶液的质量关系如图,则试管C中的溶质成分是(用化学式表示)。
下列物质混合后,不能发生复分解反应的一组是( )
A . K2SO4溶液和Ba(OH)2溶液混合
B . KCl溶液和Cu(NO3)2溶液混合
C . CuSO4溶液和NaOH溶液混合
D . CaCO3和HCl溶液
如图是包含物质A、B、C、D和盐酸的“化学拼图”卡片,相邻两张卡片所标的物质(或其溶液)间能发生反应

-
(1) 盐酸与D反应的实质是。
-
(2) C与D之间的反应属于(填化学反应基本类型)
-
(1) 同学们根据复分解反应发生的条件,总结出得到CaCl2的不同途径,如:
①Ca(OH)2+YCln=CaCl2+Z↓,那么Z可能是(填一种物质的化学式即可);
②CaX2+2YCln=CaCl2+H2O,则“YCln”属于类的质。
-
(2) 同学们又用类比的方法对CaCl2可能具有的化学性质进行了探究,总结出其能与下列物质中的发生反应(填编号)。
①HNO3 ②AgNO3 ③Na2CO3 ④Fe(OH)2 ⑤Mg ⑥BaCO3
我国古代典籍中有”银针验毒”的记载,“银针验毒”的反应原理之一是4Ag+2H2S+O2=2X+2H2O。下列有关该反应的说法正确的是( )
A . 反应属于复分解反应
B . X的化学式是Ag2S
C . 反应前后分子的种类不变
D . 该反应前后元素的化合价不变
下面是四种制取ZnSO4的化学反应:
①Zn+ H2SO4=ZnSO4+H2↑ ②ZnO+H2SO4=ZnSO4+H2O
③Zn(OH)2+H2SO4=ZnSO4+2H2O ④ZnCO3+H2SO4=ZnSO4+ H2O+CO2↑
对这四个化学反应,错误的是( )
A . 反应①中锌元素由游离态变为化合态
B . 反应②中锌元素的化合价不变
C . 反应③实质是Zn2+和SO42-的反应
D . ③④都是复分解反应
最近更新



