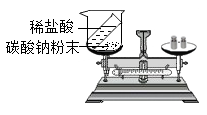
化学实验方案设计与评价 知识点题库
-
(1) 请填写下表中的实验结论:
实验过程
实验现象
实验结论
向盛有少量Fe2O3的试管中加入NaCl溶液振荡
固体不溶解
-
(2) 是否需要做“向Fe2O3中加入水”的对比实验?为什么?
选项 | 实验目的 | 实验操作 |
A | 除去CO2中的CO | 通入澄清石灰水中 |
B | 除去铜粉中的铁粉 | 滴加适量稀盐酸 |
C | 鉴别纯水和矿泉水 | 滴加适量肥皂水 |
D | 鉴别真黄金和假黄金(铜锌合金) | 滴加稀盐酸 |
查阅资料:吹不灭的蜡烛是在蜡烛芯上包裹一层打火石的粉末,打火石是由某种金属掺入少量稀土元素制成的合金,它的着火点只有150℃.
老师告诉同学们,蜡烛芯内打火石中的金属可能是镁、铁或铜中的一种,为确定该金属的成分,大家设计了以下实验方案,请你填空和回答有关问题(注:不考虑打火石中稀土元素对探究金属性质的影响).
-
(1) 完成下列表格
实验序号
操 作 步 骤
实 验 现 象
实 验 结 论
1
切开蜡烛,取出打火石,用砂纸打磨
打火石的颜色为
①
该金属一定不是铜
2
取少量打磨后的打火石于试管中,滴加②
③
该金属一定不是铁,而是镁
-
(2) 反思交流:
(i)实验2中反应的化学方程式为④;
(ii)蜡烛吹不灭的原因是⑤
(iii)小天认为只做实验2便能确定该金属不是铜,理由是⑥.
选项 | 实验目的 | 所用试剂或方法 |
① | 检验生石灰中是否含有杂质碳酸钙 | 稀盐酸 |
② | 除去CO2中含有的杂质CO | 通过灼热的氧化铜 |
③ | 鉴别氢氧化钠溶液和饱和石灰水 | 升高温度 |
④ | 分离C和CuO的固体混合物 | 加水溶解后过滤 |
选项 | 实验操作 | 现象与结论 |
A | 用黄铜片在铜片上刻画 | 铜片上有划痕说明黄铜的硬度比铜大 |
B | 用小木棍蘸少量浓硫酸 | 木棍变黑说明浓硫酸有吸水性 |
C | 向某溶液中滴入无色酚酞试液 | 无色酚酞试液不变色说明无色溶液一定是酸 |
D | 向某固体中滴入稀盐酸 | 有气泡产生说明该物质中一定含CO32﹣ |
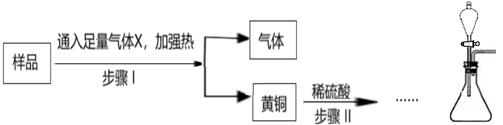
-
(1) 气体X是 ,步骤I的目的是: 。
-
(2) 步骤II中,若通过测定铜的质量来确定黄铜中铜、锌的质量比,简述从黄铜中分离出铜的实验操作。
-
(3) 步骤II中,若不测定铜的质量,某同学认为,结合上图提供的装置进行实验,即使装置气密性不良,也能达到实验目的,写出实验过程中需要测量的数据。

-
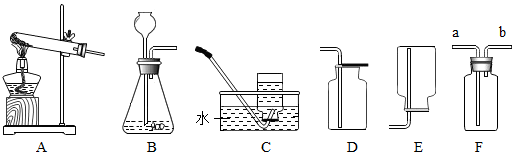
(1) 标号①、②的仪器名称:①,②;
-
(2) 实验室制取二氧化碳可以选择的发生装置是(填写装置序号),写出用大理石和盐酸制取二氧化碳的文字表达式;若要收集较干燥的二氧化碳,可选用的收集装置是(填写装置序号)。
-
(3) 在学习二氧化碳性质时,做了如图G所示的实验:向烧杯中倾倒二氧化碳,下层蜡烛先熄灭,上层蜡烛后熄灭。说明二氧化碳气体具有的性质是。
-
(4) 一氧化氮是大气污染物,但少量一氧化氮在人体内具有扩张血管、增强记忆的功能。实验室收集一氧化氮只能用排水集气法。据此我们推测出一氧化氮具有的性质是(答出一点即可,但不可回答一氧化氮是一种气体)。
-
(5) 实验室用稀硫酸与锌粒反应制取氢气时,装置B、C均可用作发生装置,相对于装置B来说,装置C具有的优点,图中可供选用的收集装置有(填序号)。
-
(1) 若选用A装置用高锰酸钾制取氧气,则有一处需要改进,其目的是;反应的文字表达式为;试管口略向下倾斜的原因;收集氧气可用D装置的原因是;若用C装置收集氧气,请简述判断氧气已收集满的方法;采用这种集气法收集的氧气不纯的原因可能是(答出一点即可)。
-
(2) 实验室用分解过氧化氢制氧气的文字表达式为;该方法可选用的发生装置是(填装置序号);如需随时控制反应速率可将B装置中的(填仪器名称)换成(填仪器名称);若选用F装置用于排空气法收集氧气,氧气应从端(选填“a”或“b”,下同)通入;若选用F装置用于排水法收集氧气,瓶中先装满水,则氧气应从端通入。
-
(3) 用C装置收集一瓶氧气用于铁丝燃烧实验,应在集气瓶底预留适量的水,目的;铁丝绕成螺旋状,原因;铁丝下端系一根火柴的作用;该反应的文字表达式为。
-
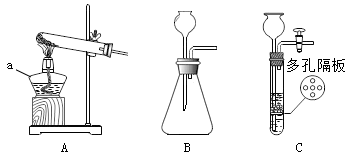
(1) 写出图中仪器的名称:a 。
-
(2) 实验室用大理石和稀盐酸制取二氧化碳,反应的化学万程式是;可用B、C作发生装置,C与B相比的主要优点是。
-
(3) 某小组对KClO3分解反应的催化剂进行研究,在相同的加热条件下,用下图装置完成表中实验:
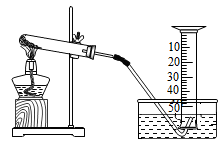
编号
KClO3质量 (g)
催化剂种类
催化剂质量(g)
收集50mLO2所需时间(s)
实验1
5
170
实验2
5
MnO2
0.5
49
实验3
5
Fe2O3
0.5
60
实验4
5
KCl
0.5
152
Ⅰ设置实验1的目的是。
Ⅱ表中催化剂的催化效果最佳的是(填化学式)。
Ⅲ由实验1和实验4可知,KCl(填“有”或“无”)催化作用。维持加热条件不变,用实验1继续收集50mLO2 , 所需时间明显少于170s。解释原因:。
Ⅳ要比较KClO3分解反应中不同催化剂的催化效果,除了测量收集50mLO2所需时间外,还可以测量。

-
(1) (活动一)探究人体呼出气体中是否含有CO2
向装有呼出气体的集气瓶中滴加少量澄清石灰水,振荡后观察到,结论:人体呼出气体中含有CO2。
-
(2) (活动二)探究人体呼出气体中CO2的体积分数
兴趣小组同学用图1所示装置进行实验。(锥形瓶内充满人体呼出的气体)实验前注射器内液体体积为50mL,向锥形瓶内注入少量液体后,注射器内的液体开始被自动吸入锥形瓶,充分反应后,注射器内NaOH溶液的体积为30mL。
小亮同学提出疑问:锥形瓶内CO2是否反应完?
同学们展开了激烈的讨论,设计实验并证明锥形瓶内无色溶液中确实含有NaOH,得出锥形瓶内CO2已反应完。
实验步骤
实验现象
实验结论
①取少量锥形瓶内无色溶液于试管中,加入
②过滤,向滤液中滴加几滴酚酞溶液
③
④
无色溶液中含有NaOH
结论:人体呼出气体中CO2的体积分数为。
-
(3) (活动三)探究人体呼出气体中O2的体积分数兴趣小组同学用图2所示装置进行实验。

(注射器及玻璃管内充满人体呼出的气体)
①实验中需反复推拉注射器的目的是;
②在操作中如何判断装置中的O2是否反应完?。
结论:人体呼出气体中O2的体积分数为16%。
(实验反思)活动三所用方法与教科书上“测定空气里O2的含量”的方法相比,其优点是:(答一点即可)。

-
(1) 图2与图1的实验相比,其优点是什么?
-
(2) 烧杯B中的实验现象是什么?图2中的实验现象是什么?
-
(3) 两组实验的结论均是什么?

-
(1) 实验一中所用红磷必须过量的目的是;
-
(2) 实验二中能体现 CO2的物理性质是;
-
(3) 实验三可得出燃烧的条件之一是;
-
(4) 实验四中(填“左”或“右”)边试管发烫。
-
(1) Ⅰ.探究温度和浓度对Na2CO3溶液去油污效果的影响
(进行实验)室温下,取8个大小相同涂有0.5g植物油的玻璃片,分别浸泡在100g试剂中15分钟,取出干燥后观察实验现象。实验结果如下:
第1组
第2组
第3组
实验编号
①
②
③
④
⑤
⑥
⑦
⑧
温度
20℃
20℃
20℃
20℃
30℃
30℃
40℃
40℃
试剂
水
1% Na2CO3溶液
5% Na2CO3溶液
10% Na2CO3溶液
水
10% Na2CO3溶液
水
10% Na2CO3溶液
去油污效果
5%
16%
20%
27%
60%
90%
75%
97%
已知:去油污效果=去除油脂质量/初始油脂质量
(解释与结论)
配制100g 10% Na2CO3溶液,需要称量Na2CO3固体g。
-
(2) 设计实验①的目的是。
-
(3) 欲探究“浓度对Na2CO3溶液去油污效果的影响”需对比的实验是(填实验编号)。
-
(4) 对比实验④⑥⑧可得到的结论是。
-
(5) Ⅱ.探究温度和浓度对Na2CO3溶液碱性的影响
(查阅资料)相同温度下,溶液的pH越大,碱性越强。
(进行实验)
实验⑨:20℃时,用pH传感器测定不同浓度Na2CO3溶液的pH(结果如图1)。
实验⑩:用pH传感器和温度传感器测定不同温度下10% Na2CO3溶液的pH(结果如图2)。
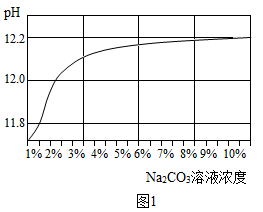
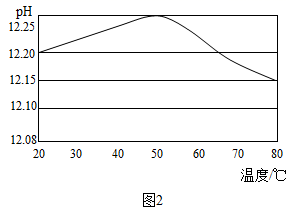
(解释与结论)
结合第1组实验和图1数据分析,欲得出“溶液的碱性越强,Na2CO3溶液去油污效果越好”的依据是。
-
(6) 由图2可知,10% Na2CO3溶液的pH与温度的关系是。
-
(7) (反思与评价)
(查阅资料)相同浓度下,Na2CO3溶液的温度越高,碱性越强
综合以上实验分析,下列说法正确的是(填字母序号)。
A 热Na2CO3溶液去油污效果更好可能与“温度升高,水的去油污能力增强”有关
B 热Na2CO3溶液去油污效果更好可能与“温度升高,溶液碱性增强”有关
C 10% Na2CO3溶液在不同温度时,pH可能相同
D 溶液碱性增强,pH一定增大
-
(1) (查阅资料)84消毒液的有效成分是次氯酸钠,化学式为(NaClO)
(实验1)取少量84消毒液于试管中,滴加 H2O2溶液,发现有大量气泡产生,然后,(填写实验操作和现象),证明产生的气体是氧气。
-
(2) (提出问题)在上述反应中,NaClO的作用是什么?
(作出猜想)猜想一:做反应物,NaClO 与 H2O2溶液发生化学反应;
猜想二:作,类似分解 H2O2溶液制氧气时二氧化锰的作用。
-
(3) (实验2)
①按如图所示,组装实验装置,并。
②向锥形瓶中加入30mL84 消毒液,注射器中吸入 30mLH2O2溶液
③将注射器中的H2O2溶液平均分6次推入锥形瓶中;每次推入H2O2溶液,待不再产生气泡后,记录收集气体的总体积(忽略其他因素对测量结果造成的影响),见下表。
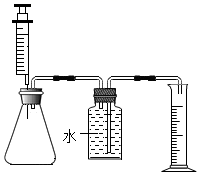
实验编号
第一次
第二次
第三次
第四次
第五次
第六次
收集气体体积/mL
103
206
257
262
267
X
-
(4) (分析讨论)
①X的值为。分析表中数据得出“”正确(填“猜想一或猜想二”),
②次氯酸钠与 H2O2溶液反应,除生成氧气外,还生成氯化钠和水,该反应的化学方程式为 。
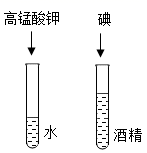 探究影响溶解性的因素
B .
探究影响溶解性的因素
B . 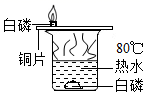 证明可燃物燃烧需要氧气
C .
证明可燃物燃烧需要氧气
C . 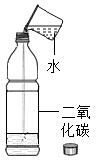 证明二氧化碳能溶于水
D .
证明二氧化碳能溶于水
D . 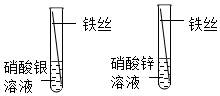 比较Fe、Ag、Zn的金属活动性
比较Fe、Ag、Zn的金属活动性
-
(1) 实验室有两瓶没有贴标签的无色溶液,只知道是氢氧化钙溶液和氢氧化钠溶液的各一种,小雪同学想利用化学试剂,用化学方法确定各是哪种物质。
①小雪所选的鉴别试剂最好是下列选项中的(填选项序号之一)。
A 无色酚酞 B 碳酸钾溶液 C 硫酸铜溶液 D 氯化钡溶液
②取两种无色溶液各少许,分别放在两只试管中,各倒入适量所选鉴别试剂,观察到一个试管中有沉淀生成,可证明这个试管中放入的是(写化学式)溶液。
-
(2) 现欲探究一固体混合物A的成分,已知其中可能含有NaCl、Na2CO3、NH4Cl、NH4NO3四种物质中的两种或多种。按图所示进行实验,出现的现象如图中所示(设过程中所有发生的反应都恰好完全反应)。
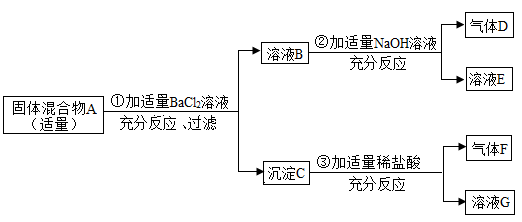
试根据实验过程和出现的现象做出判断,填写以下空白:
①固体混合物A中,一定存在的物质是(写化学式)。
②若将气体F通入紫色石蕊试液中,试液显色。
③溶液G中,一定存在的酸根离子是(写离子符号)。
④写出一个实验过程②中可能发生的一个反应的化学方程式:。
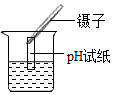 B . 验证空气中氧气的含量
B . 验证空气中氧气的含量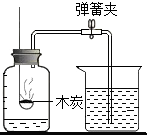 C . 证明CO2的密度比空气大
C . 证明CO2的密度比空气大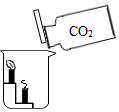 D . 验证质量守恒定律
D . 验证质量守恒定律