碳及其化合物 知识点题库
下列事实能用同一原理进行解释的是( )
A . 金和铝在空气中都不易被腐蚀
B . 实验室收集CO2和O2都能用向上排空气法
C . 实验室和工业上都可用石灰石制二氧化碳
D . 在滴有酚酞的NaOH溶液中滴加稀盐酸和投入活性炭都能使溶液褪色
根据下图装置,回答下列有关问题:
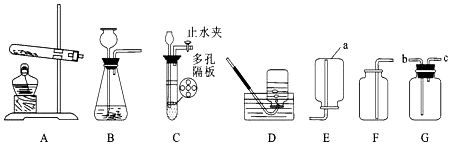
-
(1) 装置图中仪器a的名称为.
-
(2) 写出以混合物为原料用装置A制氧气的化学方程式;该装置中试管口略向下倾斜的原因是.
-
(3) 若用G装置采用排空法收集氢气,氢气应从进(选“b”或“c”).
-
(4) 制取二氧化碳最好选用的发生装置是(填字母).
利用下图实验装置进行实验,根据实验现象不能得出的结论是( )

A . CO 有还原性
B . CO 有毒性
C . CO 有可燃性
D . 产物有 CO2
下图装置可以做CO还原Fe2O3的实验并检验该反应的气体生成物。已知由一氧化碳发生装置得到的CO中混有杂质CO2和H2O。

-
(1) 写出B装置玻璃管内反应的化学方程式。
-
(2) 从环保角度考虑,请写出一种尾气处理方法。
-
(3) 若没有A装置,则该实验不能达到检验气体生成物的目的,请说明原因。
为了制取氧气,实验室提供了以下药品和仪器装置。
【药品】①二氧化锰②氯酸钾③过氧化氢溶液④高锰酸钾
【装置】

-
(1) 写出标号仪器的名称:①;②;
-
(2) 实验室用高锰酸钾制取氧气,装置C还需做的一点改动是,请写出该反应的符号表达式:。
-
(3) 实验室用过氧化氢溶液制取氧气,可用的发生装置是,请写出反应的符号表达式:。
-
(4) 实验室用加热氯化铵和氢氧化钙固体混合物的方法制取氨气(注:同温同压下,氨气的密度接近于空气密度的60%,且极易溶于水),应选用的制取装置为 (填装置编号),收集装置为 (填装置编号)。
下列物质的用途与性质对应关系错误的是( )

A . A
B . B
C . C
D . D
水是一种宝贵的自然资源,它有许多性质和用途,请回答下列问题:
-
(1) 除去水中的不溶性物质,常用的方法是。
-
(2) 用水可除去某些混合气体中的性杂质(选填“难溶“或“易溶“);
-
(3) 自然界中的水在一定程度上可以缓解二氧化碳对地球造成的。
-
(4) 用肥皂水来区分软硬水时,出现较多泡沫的为。
-
(5) 水是常见的溶剂,下列溶液是以水为溶剂的是________A . 抚顺白酒 B . 碘酒 C . 稀盐酸 D . 生理盐水
下列是初中部分常见物质的转换关系,已知,固体F是银白色的金属。C、D、G、H、J属于氧化物。请做出合理推断并完成下面的问题。

-
(1) 写出固体F的化学式,属于纯净物中的类别。
-
(2) 操作E名称为,黑色固体C在反应②中的作用是。
-
(3) 反应③的基本反应类型是。
-
(4) 写出反应⑦的化学反应方程式是,该反应体现了气体G具有。
-
(5) 反应①和反应②都可用于实验室制取无色气体B,同学们讨论后认为较好的方法是②,你觉得同学们的理由是:。(写2条理由)
推理是一种重要的学习方法。下列推理得出的相关结论正确的是( )
A . 含碳元素的物质充分燃烧会生成 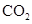 ,所以燃烧能生成
,所以燃烧能生成 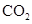 的物质一定含碳元素
B . 铁丝在氧气中能够燃烧,空气中有氧气,所以铁丝在空气中一定能够燃烧
C . 二氧化碳能使燃着木条熄灭,所以能使燃着木条熄灭的气体一定是二氧化碳
D . 水与过氧化氢都是由氢、氧元素组成的化合物,所以它们的性质完全相同
的物质一定含碳元素
B . 铁丝在氧气中能够燃烧,空气中有氧气,所以铁丝在空气中一定能够燃烧
C . 二氧化碳能使燃着木条熄灭,所以能使燃着木条熄灭的气体一定是二氧化碳
D . 水与过氧化氢都是由氢、氧元素组成的化合物,所以它们的性质完全相同
根据下图回答问题。

-
(1) 写出上图中标注仪器的名称:①②
-
(2) 实验室用过氧化氢溶液和二氧化锰来制取较纯净的氧气,选用的发生和收集装置为,开始收集的最佳时机是
-
(3) 实验室制取二氧化碳的化学方程式为 若用F装置收集,则二氧化碳应从管口通入,验满的方法是 ,若将收集的气体通入紫色石蕊试液中现象是
-
(4) 实验室可以用无水醋酸钠固体与碱石灰固体加热制取甲烷,应选用的发生装置是 ,收集装置可以选用 或 或
通过下列实验装置探究碳及其化合物的性质。

①装置 A 中反应的化学方程式为。
②装置 B 中氢氧化钠溶液的作用是。
③装置 C 中黑色固体变红色,其化学方程式为。
④下列对该实验的分析正确的是(选填编号)。
I.给装置 A 中通入 0.1mol 二氧化碳,装置 C 中可生成 0.2mol 铜
II.装置 C 中固体减少的质量与装置 D 中增加的质量相等
III.实验结束时应先熄灭 C 处酒精灯
IV.反应结束后继续通入二氧化碳的目的是防止铜被氧化
请结合下图回答问题:
图1 
图2 
-
(1) 仪器名称:①,②。
-
(2) 用氯酸钾制取氧气,可选用的发生装置是(选填序号),该反应的化学方程式为。用D装置收集氧气完毕后,应先(选填“从水中取出导管”或“熄灭酒精灯”)。
-
(3) 实验室制取CO2 , 反应的化学方程式为,为方便控制反应的发生和停止,应选择的发生装置是(选填序号),可用C装置收集CO2的理由是。
-
(4) 如图是某学生设计的一种由洗气、除杂、检验等用途的装置,当用排水法收集氢气时,瓶内先装满水,气体从(选填“a”或“b”),用该装置还可以检验CO2 , 写出发生反应的化学方程式。
请根据下列装置,回答问题:

-
(1) 标号①、②的仪器名称:①,②;
-
(2) 实验室制取二氧化碳可以选择的发生装置是(填写装置序号),写出用大理石和盐酸制取二氧化碳的化学方程式;若要收集较干燥的二氧化碳,可选用的收集装置是(填写装置序号)。
-
(3) 在学习二氧化碳性质时,做了如图G所示的实验:向烧杯中倾倒二氧化碳,下层蜡烛先熄灭,上层蜡烛后熄灭。说明二氧化碳气体具有的性质是。
-
(4) 一氧化氮是大气污染物,但少量一氧化氮在人体内具有扩张血管、增强记忆的功能。实验室收集一氧化氮只能用排水集气法。据此我们推测出一氧化氮具有的性质是(答出一点即可,但不可回答一氧化氮是一种气体)。
-
(5) 实验室用稀硫酸与锌粒反应制取氢气时,装置B、C均可用作发生装置,相对于装置B来说,装置C具有的优点,图中可供选用的收集装置有(填序号)。
根据下面的实验装置回答问题; 

-
(1) 实验室用高锰酸钾制取较纯净的O2时可选择的装置组合是(填装置序号)发生反应的化学方程式为
-
(2) 将装置F用于收集O2时的验满方法是
-
(3) 装置C用于实验室制取CO2时装置内发生的化学方程式为,该装置的优点是。
学习化学,提高学科核心素养,学会从化学的角度分析问题。下列说法错误的是( )
A . 二氧化碳是植物光合作用的基本原料,可用于温室的气体肥料
B . 氮气化学性质不活泼,可用于填充灯泡
C . 氧气具有可燃性,可用作火箭燃料
D . 稀有气体在通电时发出不同颜色的光,可制造多种电光源
人类的生产生活离不开水。
-
(1) 下列净化水的措施中,相对净化程度较高的是_____(填字母)。A . 静置沉淀 B . 吸附沉淀 C . 过滤 D . 蒸馏
-
(2) 与漫灌相比,喷灌和滴灌的优点是。
-
(3) 含有较多可溶性钙、镁化合物的水叫做硬水,检验生活用水是硬水还是软水常用的试剂为。
-
(4) 过滤是实验室分离可溶物和不溶物常用的操作。过滤时用到的玻璃仪器有下列选项中的_____。A . 烧杯 B . 玻璃棒 C . 铁架台 D . 漏斗
-
(5) 铁丝燃烧时盛有氧气的集气瓶底部需放少量水,是因为。
-
(6) 净水器中常用到活性炭,这是利用了活性炭的性。
-
(7) 海水淡化可缓解淡水资源匮乏的问题。下图为太阳能海水淡化装置示意图。海水制备淡水的过程属于(填“物理”或“化学”)变化。

下列实验方案中,不能达到相应实验目的的是( )
A .  验证质量守恒定律
B .
验证质量守恒定律
B .  证明二氧化碳密度比空气大
C .
证明二氧化碳密度比空气大
C .  氧气验满
D .
氧气验满
D .  探究分子运动
探究分子运动
 验证质量守恒定律
B .
验证质量守恒定律
B .  证明二氧化碳密度比空气大
C .
证明二氧化碳密度比空气大
C .  氧气验满
D .
氧气验满
D .  探究分子运动
探究分子运动
请根据下列实验装置图回答问题:

-
(1) 实验室制取二氧化碳的发生装置是(填字母),反应的化学方程式为
-
(2) 实验室用装置A加热高锰酸钾制取氧气的化学方程式为,在试管口放置蓬松的棉花团的目的是。用排空气法收集氧气时,检验是否收集满的操作方法是。
-
(3) 已知通常状况下,二氧化硫气体的密度比空气大,易溶于水,能与水反应生成亚硫酸。实验室常用亚硫酸钠与硫酸在常温下反应制取二氧化硫。
①实验室制取SO2的发生装置可用(填字母),收集SO2的装置可用(填字母)。
②如图所示,把充满SO2的试管倒立在滴有紫色石蕊的水中,可看到的现象是试管内且液体变为红色,其中液体变为红色的原因是液体中产生了(填物质的化学式)。

阅读面科普短文,并回答相关问题
甲醇(CH3OH)是一种重要的化工原料,其中利用催化剂催化H2与CO2反应制备甲醇是获取甲醇的重要途径。传统的使用金属氧化物催化剂制备甲醇通常需要较高的反应温度(大于300℃),且会产生大量副产物CO,而将不同种金属氧化物混合作为催化剂时催化效果会大大改善。如将氧化铜和氧化锌的混合物作为合成甲醇反应的催化剂时,催化效果如图所示。
我国科学家近日开发出一种新型催化剂,该催化剂在180℃时,生成物中甲醇的含量可达94.3%。该催化剂为实现低能耗、高效率的CO2转化利用开辟了新途径。

-
(1) 混合催化剂中CuO的质量分数为时,催化效果最佳。
-
(2) 新型催化剂相比传统金属氧化物催化剂的优点是(写一点)。
-
(3) 新型催化剂可将CO2和H2转化为CH3OH和H2O,反应的化学方程式为
-
(4) 将二氧化碳高效转化为甲醇对于环境的意义为。
A-F是初中化学常见的物质。已知A、B、C、D、E是五种不同类别的物质,A是能使澄清石灰水变浑浊的气体,C常用于改良酸性土壤,E是提取量最大的金属,F可用于制备波尔多液,六种物质之间的反应与转化关系均为初中化学常见的化学反应。图中“-”表示相连的物质能相互反应,“→”表示一种物质转化成另一种物质(部分反应物、生成物及反应条件已略去)。请回答下列问题:

-
(1) B所属的物质类别为。
-
(2) 写出D的一种用途:。
-
(3) B-C反应的化学方程式可能是。
-
(4) E和F发生化学反应的基本反应类型是。
最近更新



