氧族与碳族及其应用 知识点题库
芯片主要成分是( )
A . Cu
B . Al
C . SiO2
D . Si
下列说法中,不正确的是( )
A . 铅笔芯不含铅
B . 陶瓷都不透明
C . 有机玻璃不属于玻璃
D . 纯碱不属于碱
下列关于硫及含硫化合物的叙述正确的是( )
A . 常温下铝遇浓硫酸钝化,因此可用铝槽车储运浓硫酸
B . 硫在空气中燃烧生成大量SO3
C . 浓硫酸可以干燥H2、NH3、CO2等气体
D . SO2的漂白原理与次氯酸相同
下表各组物质在适当条件均可反应,其中气体产物成分可能不唯一的是( )
A . 浓硫酸与铜
B . 浓硝酸与铜
C . 浓盐酸与MnO2
D . 浓氨水与CaO
关于aL bmol/L的浓硫酸的说法正确的是( )
A . 与足量Cu共热,转移的电子为ab mol
B . 常温时加入Al,不会发生化学反应
C . 若加入mg Zn片,Zn片完全溶解,可收集到的标准状况下气体体积为22.4m/65 L
D . 蔗糖与浓硫酸混合,只体现浓硫酸的脱水性
根据硝酸和硫酸所具有的性质,选择适当的字母按要求填空.
A.吸水性B.脱水性C.强氧化性D.强氧化性和酸性
-
(1) 浓硫酸常用作干燥剂,说明浓硫酸具有;
-
(2) 用玻璃棒蘸浓硫酸滴在纸上,发现变黑,说明浓硫酸具有;
-
(3) 冷的浓硫酸和浓硝酸都常用铁制容器装是利用浓硫酸和浓硝酸的.
光导纤维是高纯度二氧化硅。描述SiO2错误的是( )
A . 熔点高
B . 原子晶体
C . 存在极性键
D . 极性分子
下列有关硫酸的说法中不正确的是( )
A . 常温下浓硫酸与铜反应,浓硫酸体现氧化性和酸性
B . 浓硫酸与木炭粉加热发生反应时,浓硫酸只作氧化剂
C . 浓硫酸具有吸水性,可用来干燥二氧化硫
D . 蔗糖与浓硫酸的作用中,浓硫酸体现脱水性和氧化性
工业制硫酸铜的方法很多:
-
(1) 方法一:用浓硫酸和铜制取硫酸铜。该反应的化学方程式是。
-
(2) 方法二:实验证明,铜不能在低温下与O2反应,也不能与稀H2SO4共热发生反应,但工业上却是将废铜屑倒入热的稀H2SO4中并通入空气来制备CuSO4溶液的。铜屑在此状态下被溶解的化学方程式为。
-
(3) 以上两种方法(填“前”或“后”)者好,原因是。
-
(4) 方法三:用稀硫酸、铜和氧化铁制取硫酸铜,生产的主要过程如下图所示:

稀硫酸和氧化铁反应的离子方程式是(反应①);铜和上述反应(反应①)得到的物质反应的离子方程式是;向混合溶液中通入热空气的目的是;分离蓝色滤液和红褐色沉淀的实验操作是。
下列“化学与生活”的说法不正确是( )
A . 硫酸钡可用作白色颜料
B . 石膏可用来调节水泥的凝固时间
C . 胆矾可用于检验酒精中是否有水
D . 硫酸可用来制药
下列图示的实验操作正确的是( )
A . 过滤 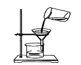 B . 称取氯化钠
B . 称取氯化钠 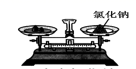 C . 稀释浓硫酸
C . 稀释浓硫酸 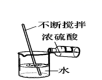 D . 氧气的验满
D . 氧气的验满 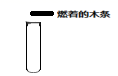
 B . 称取氯化钠
B . 称取氯化钠  C . 稀释浓硫酸
C . 稀释浓硫酸  D . 氧气的验满
D . 氧气的验满 
硅在地壳中的含量较高,硅及其化合物的开发由来已久。高纯硅是现代信息、半导体和光伏发电等产业都需要的基础材料。工业上提纯硅有多种路线,其中一种工艺流程示意图及主要反应如下:

-
(1) 工业上用石英砂和焦炭在电弧炉中高温加热到1600℃-1800℃生成粗硅的化学方程式为。
-
(2) 在流化床反应的产物中,SiHCl3大约占85%,还有SiCl4、SiH2Cl2、SiH3Cl 等,粗硅生成SiHCl3的化学反应方程式_。
-
(3) 有关物质的熔沸点数据如下表,提纯SiHCl3的主要工艺操作依次是沉降、冷凝和_;
SiHCl3极易水解且生成某种可燃性气体,其完全水解的产物为_。
物质
Si
SiCl4
SiHCl3
SiH2Cl2
SiH3Cl
HCl
SiH4
熔点/℃
1410
-70.4
-126.5
-122
-118
-114.2
-185
沸点/℃
2355
57.6
31.8
8.2
-30.4
-84.9
-111.9
-
(4) 还原炉中发生的化学反应为: 。.
-
(5) 上述工艺生产中循环使用的物质除Si、SiHCl3外, 还有_。
保护环境是公民的责任和义务。下列说法正确的是( )
A . 禁止使用“氟利昂”作为制冷剂的目的是为了减少酸雨
B . 采用原煤脱硫技术,可减少燃煤产生的二氧化硫
C . 大量开采地下水,矿产资源,以满足社会经济发展的需求
D . 废旧电池应集中回收,并填埋处理
2018年世界环境日中国主题是“美丽中国,我是行动者”。下列行为符合该主题的是( )
A . 尽量乘坐公共交通工具
B . 大量使用农药
C . 大力开采化石燃料
D . 推广使用一次性塑料餐具
化学与生活、生产、科技密切相关。下列说法错误的是( )
A . 葡萄酒中添加二氧化硫用于杀菌、抗氧化
B . 中国天眼传输信息用的光纤材料是硅
C . 研发新能源汽车,减少化石燃料的使用,与“绿水青山就是金山银山”的绿色发展理念一致
D . 氧化铝是冶炼金属铝的原料,也是较好的耐火材料
Na2S2O3用于照相业定影剂、鞣革时重铬酸盐的还原剂等.
-
(1) Na2S2O3溶液与稀硫酸的反应可探究外界条件对化学反应速率的影响.Na2S2O3溶液与稀硫酸反应的离子方程式为;表格中H2O的体积x=,其中探究温度对化学反应速率的影响的实验是(填序号).
实验
反应温度/℃
Na2S2O溶液
稀H2SO4
H2O
V/mL
c/mol·L-1
V/mL
c/mol·L-1
V/mL
Ⅰ
20
10
0.1
10
0.1
0
Ⅱ
20
5
0.2
10
0.2
x
Ⅲ
40
10
0.1
10
0.1
0
-
(2) 工业上可用反应
 制取Na2S2O3.实验室模拟该工业过程制取Na2S2O3的装置如图所示.
制取Na2S2O3.实验室模拟该工业过程制取Na2S2O3的装置如图所示.
①试管a中的化学方程式为.
②反应结束后,将试管b中溶液水浴加热浓缩,,经过滤、乙醇洗涤晶体、干燥,得到
 。用乙醇而不用水洗涤晶体的原因.
。用乙醇而不用水洗涤晶体的原因.③测定产品纯度:准确称取mg晶体,用适量蒸馏水溶解,以淀粉作指示剂,用0.1000mol·L-1碘的标准溶液滴定,反应原理为:
 。若消耗碘的标准液体积为20.00mL,产品的质量分数为(设
。若消耗碘的标准液体积为20.00mL,产品的质量分数为(设 相对分子质量为M)(写出计算表达式)
相对分子质量为M)(写出计算表达式)
化学与生产、生活密切相关。下列与化学相关的说法合理的是( )
A . 分子筛、青花瓷、黏土、玛瑙、硅石的主要成分都是硅酸盐
B . 碳氢化合物与氮氧化物经紫外线照射发生反应形成的有毒烟雾,称为光化学烟雾
C . 硅酸钠俗称水玻璃,可用作木材防火剂
D . 二氧化硫有毒,严禁将其添加到任何食品和饮料中
下列关于物质应用错误的是( )
A . 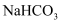 用作烘焙糕点膨松剂
B .
用作烘焙糕点膨松剂
B .  用作食品添加剂
C .
用作食品添加剂
C . 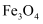 用作磁性材料
D .
用作磁性材料
D .  做光导纤维
做光导纤维
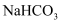 用作烘焙糕点膨松剂
B .
用作烘焙糕点膨松剂
B .  用作食品添加剂
C .
用作食品添加剂
C . 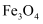 用作磁性材料
D .
用作磁性材料
D .  做光导纤维
做光导纤维
硅与碳属于同族元素,有一类由 Si 和 H 形成的有机硅化合物称“硅烷”,硅烷的组成、 结构与相应的烷烃相似。下列叙述中错误的是( )
A . 甲硅烷(SiH4)沸点比甲烷(CH4)低
B . 甲硅烷热稳定性小于甲烷
C . 硅烷的通式为SinH 2n+2 (n≥1)
D . 乙硅烷(SiH3SiH3)的二氯代物有两种同分异构体
下列关于物质的用途叙述错误的是( )
A .  可用于漂白纸浆、毛、丝等,也可用于杀菌消毒
B . 氨气易液化,液化时会吸收大量的热
C . 二氧化硅可以用来生产通信容量大、抗干扰性能好的光导纤维
D . 氮化硅陶瓷具有耐高温、抗氧化、耐腐蚀等性能,是制造火箭发动机的理想材料
可用于漂白纸浆、毛、丝等,也可用于杀菌消毒
B . 氨气易液化,液化时会吸收大量的热
C . 二氧化硅可以用来生产通信容量大、抗干扰性能好的光导纤维
D . 氮化硅陶瓷具有耐高温、抗氧化、耐腐蚀等性能,是制造火箭发动机的理想材料
 可用于漂白纸浆、毛、丝等,也可用于杀菌消毒
B . 氨气易液化,液化时会吸收大量的热
C . 二氧化硅可以用来生产通信容量大、抗干扰性能好的光导纤维
D . 氮化硅陶瓷具有耐高温、抗氧化、耐腐蚀等性能,是制造火箭发动机的理想材料
可用于漂白纸浆、毛、丝等,也可用于杀菌消毒
B . 氨气易液化,液化时会吸收大量的热
C . 二氧化硅可以用来生产通信容量大、抗干扰性能好的光导纤维
D . 氮化硅陶瓷具有耐高温、抗氧化、耐腐蚀等性能,是制造火箭发动机的理想材料
最近更新



