活化能及其对化学反应速率的影响 知识点题库
1918年,Lewis提出反应速率的碰撞理论:反应物分子间的相互碰撞是反应进行的必要条件,但并不是每次碰撞都能引起反应,只有少数碰撞才能发生化学反应.能引发化学反应的碰撞称之为有效碰撞.

-
(1) 图I是HI分解反应中HI分子之间的几种碰撞示意图,其中属于有效碰撞的是 (选填“A”、“B”或“C”);
-
(2) 20世纪30年代,Eyring和Pelzer在碰撞理论的基础上提出化学反应的过渡态理论:化学反应并不是通过简单的碰撞就能完成的,而是在反应物到生成物的过程中经过一个高能量的过渡态.图Ⅱ是NO2和CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式: ;
-
(3) 过渡态理论认为,催化剂改变反应速率的原因是改变了反应的途径,对大多数反应而言主要是通过改变过渡态而导致有效碰撞所需要的能量发生变化.请在图Ⅱ中作出NO2和CO反应时使用催化剂而使反应速率加快的能量变化示意图;
-
(4) 进一步研究表明,化学反应的能量变化(△H)与反应物和生成物的键能有关.键能可以简单的理解为断开1 mol 化学键时所需吸收的能量.下表是部分化学键的键能数据:
化学键
P﹣P
P﹣O
O=O
P=O
键能/kJ•mol﹣1
197
360
499
X
已知白磷的燃烧热为2378.0kJ/mol(1mol可燃物完全燃烧生成稳定的氧化物所放出的热量为燃烧热),白磷完全燃烧的产物结构如图Ⅲ所示,则上表中X= .
①升高温度 ②加入催化剂 ③增大体系压强 ④增大反应物浓度.

反应过程
-
(1) 该反应是(填“吸热”或“放热”)反应。
-
(2) 该反应的热化学方程式为。
-
(3) 改变下列条件都可使该反应的反应速率改变,其中通过降低活化能加快反应速率的是。
a.浓度 b.压强 c.温度 d.催化剂
-
(4) 反应体系中加入催化剂对反应热是否有影响?(填“是”或“否”),原因是。

前体物之一,还可产生光化学烟雾和硝酸型酸雨,严重危害人类生命健康和破坏生态环境。回答下列问题:
-
(1) 一种脱硝方法是利用臭氧将NOx氧化为高价态氮氧化物N2O5 , 然后溶解在液相中。
氧化反应如下:
Ⅰ.NO(g)+O3(g)
 NO2(g)+O2(g) △H1=- 200.9 kJ·mol-1
NO2(g)+O2(g) △H1=- 200.9 kJ·mol-1Ⅱ.2NO2(g)+O3(g)
 N2O5(g)+O2(g) △OH2
N2O5(g)+O2(g) △OH2①在298K,101kPa时,反应I的活化能为10.7kJ·mol-1 , 则其逆反应的活化能为kJ·mol-1
②在2L密闭容器中充入2molNO2和1molO3 , 在不同温度下,平衡时NO2的物质的量分数
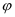 (NO2)随温度变化的曲线如图甲所示。
(NO2)随温度变化的曲线如图甲所示。
ⅰ.反应Ⅱ的△H20(填“大于”“小于”或“等于”,下同),a点的V正b点的v正 , a点的v正 v逆。
ⅱ.图甲中,T2℃时,若考患2NO2(g)
 N2O4(g),平衡后,O2和N2O4的平衡分压相同,则反应Ⅱ以物质的量分数表示的平衡常数Kx=(保留两位小数,不考虑反应Ⅰ的影响)。
N2O4(g),平衡后,O2和N2O4的平衡分压相同,则反应Ⅱ以物质的量分数表示的平衡常数Kx=(保留两位小数,不考虑反应Ⅰ的影响)。ⅲ.对反应体系无限加压,得平衡时a(O3)与压强的关系如图乙所示。压强增大至p1MPa之后,O3的平衡转化率a(O3)不再增大的原因是
-
(2) 一种Ce-Ti固溶体催化剂选择性催化还原NOx的原理如下。

①反应的化学方程式为。
②反应的催化剂为(填标号)。
-
(1) Ⅰ.减少
 的排放,常采取的措施有:
的排放,常采取的措施有:将煤转化为清洁气体燃料。已知:




则焦炭与水蒸气反应生成
 和
和 的热化学方程式为。
的热化学方程式为。 -
(2) 洗涤含
 的烟气,以下物质可作洗涤剂的是(填序号)。
的烟气,以下物质可作洗涤剂的是(填序号)。a.
 b.
b.  c.
c. 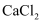 d.
d. 
-
(3) Ⅱ.利用
 的还原性可以消除氮氧化物的污染。
的还原性可以消除氮氧化物的污染。氮氧化物间的相互转化,已知
 的反应历程分两步:
的反应历程分两步:第一步
 (快反应)
(快反应)第二步
 (慢反应)
(慢反应)①总反应的速率由决定(填“第一步或第二步”)。
②用
 表示的速率方程为
表示的速率方程为 ;
; 表示的速率方程为
表示的速率方程为 ,
, 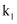 与
与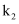 分别表示速率常数,则
分别表示速率常数,则 (填数值)。
(填数值)。③下列关于反应
 的说法正确的是(填序号)。
的说法正确的是(填序号)。A.反应的总活化能等于第一步和第二步反应的活化能之和
B.使压强增大,反应速率常数一定增大
C.第一步反应的活化能小于第二步反应的活化能
-
(4) 已知

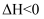 , 某研究小组将
, 某研究小组将 、
、 和一定量的
和一定量的 充入
充入 密闭容器中,在
密闭容器中,在 催化剂表面发生上述反应,
催化剂表面发生上述反应, 的转化率随温度变化的情况如图所示:
的转化率随温度变化的情况如图所示:
①在有氧条件下,温度
 之后
之后 生成
生成 的转化率降低的原因可能是。
的转化率降低的原因可能是。②在温度为
 时,有氧条件下
时,有氧条件下 生成
生成 的转化率明显高于无氧条件的原因可能是。
的转化率明显高于无氧条件的原因可能是。③有氧条件下,在
 内,温度从
内,温度从 升高到
升高到 , 此时段内
, 此时段内 的平均反应速率
的平均反应速率 。
。
 CaO(s)+CO2(g) ΔH>0 能否自发进行与温度有关
D . 常温下,反应C(s) +CO2(g) =2CO(g)不能自发进行,则该反应的ΔH>0
CaO(s)+CO2(g) ΔH>0 能否自发进行与温度有关
D . 常温下,反应C(s) +CO2(g) =2CO(g)不能自发进行,则该反应的ΔH>0

 )是制造染料的甲基化试剂。我国科学家利用计算机模拟技术,分别研究反应
)是制造染料的甲基化试剂。我国科学家利用计算机模拟技术,分别研究反应 在无水和有水条件下的反应历程,如图所示。下列说法正确的是( )
在无水和有水条件下的反应历程,如图所示。下列说法正确的是( )
 的能量高于
的能量高于 的能量,因此该反应的
的能量,因此该反应的 B . 无水条件下逆反应的活化能为34.76 Ev
C . 水改变了该反应的
B . 无水条件下逆反应的活化能为34.76 Ev
C . 水改变了该反应的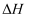 D . 反应过程中
D . 反应过程中 中的C—H键均未发生断裂
中的C—H键均未发生断裂
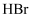 加成过程及能量变化如下图, 下列说法正确的是( )
加成过程及能量变化如下图, 下列说法正确的是( )





