几组未知物的检验 知识点题库
-
(1) 取少量固体于试管中,滴加稀盐酸,有气泡产生,由此可知该NaOH固体已变质.写出氢氧化钠在空气中变质的化学方程式
-
(2)
该同学为进一步探究固体中是否还含有NaOH,设计了如下实验方案:

①滴加足量的CaCl2溶液目的是 ,生成沉淀的化学方程式为
②取少量溶液B于试管中,滴加少量 试液,现象为 ,其结论是固体样品中 (填“存在”或“不存在”)氢氧化钠.
-
(1) 某同学通过分析,认为无需检验就可判断其中必有的两种物质是 和 (填化学式).
-
(2) 为了确定X,现将(1)中的两种物质记为A和B,含X的物质记C,当C与B的溶液混合时,产生红褐色沉淀和无色无味气体;当C与A的溶液混合时也产生红褐色沉淀,向该沉淀中滴入稀硝酸沉淀部分溶解,最后留有白色沉淀不再溶解.则X为 .
A.SO32﹣B.SO42﹣C.CH3COO﹣D.SiO32﹣
-
(3) B的水溶液显 性,原因为 .(用离子方程式表示)
-
(4) 将0.02molA与0.01molC同时溶解在足量的蒸馏水中,充分反应后,最终所得沉淀的物质的量为 (保留一位小数)
-
(5) 将Cu投入到装有D溶液的试管中,Cu不溶解;再滴加稀H2SO4 , Cu逐渐溶解,管口附近有红棕色气体出现.则物质D一定含有上述离子中的 (填相应的离子符号).有关反应的离子方程式为:
-
(6) 利用上述已经确定的物质,可以检验出D、E中的阳离子.请简述实验操作步骤、现象及结论
①取少许固体溶于水,得到无色透明溶液;
②往此溶液中滴加氯化钡溶液,有白色沉淀生成;
③过滤,往沉淀中加入足量的稀硝酸,发现沉淀没有全部溶解且有无色无味的气体生成.
④往滤液中加入足量的新制的氯水,再加入少许汽油,振荡,静置,上层液体呈紫红色.
-
(1) 试判断:固体混合物中肯定含有,一定没有,可能含有.
-
(2) 对可能含有的物质,如何进行实验以进一步检验.
-
(3) 实验④中发生的化学反应属于反应(填反应类型),主要实验操作名称叫.
①将固体溶于水,搅拌后得到无色透明溶液;
②往此溶液中滴加硝酸钡溶液,有白色沉淀生成;
③过滤,将沉淀置于稀硝酸中,发现沉淀全部溶解.
-
(1) 试判断:固体混合物中肯定含有,肯定没有,可能含有.
-
(2) 对可能有的物质,可采用往滤液中滴加(填试剂名称)来检验,如果含有该物质,其现象是.
根据上述实验现象,完成下列各题:
-
(1) 原白色粉末中肯定含有的物质为,可能含有的物质为.
-
(2) 写出步骤①中发生反应的化学方程式.
-
(3) 写出步骤②中发生反应的离子方程式为.
-
(4) 写出步骤③中发生反应的离子方程式.

-
(1) 依次写出D、E、G三种微粒符号、、;
-
(2) a、d的比值为;
-
(3) 复盐的化学式为.(写出计算步骤)
实验步骤 | 实验现象 |
①取少量该溶液,测定溶液pH | pH=0 |
②取少量该溶液加热浓缩,加Cu片和浓 H2SO4 , 加热 | 有无色气体产生,气体遇空气变成红棕色 |
③取少量该溶液,加少量BaCl2溶液 | 有白色沉淀 |
④取③中上层清液,加足量AgNO3溶液 | 有白色沉淀,且不溶于稀HNO3 |
⑤取少量该溶液,加NaOH溶液 | 有白色沉淀,NaOH过量时沉淀部分溶解 |
由此判断:
-
(1) 溶液中肯定不存在的离子有,
溶液中肯定存在的离子是.
-
(2) 请设计实验验证其中可能存在的阴离子的方法(写明操作、现象、结论)
-
(3) Ⅱ.已知一定量的铁粉与某浓度的硝酸反应,其离子方程式如下:
aFe+bH++cNO3﹣═dFe2++eFe3++fNO+gN2O4+hN2O+iH2O
试确定以下关系
①a、d、e的关系;
②c、f、g、h的关系;
③b、c、d、e的关系;
④d、e、f、g、h的关系;
⑤b、f、g、h的关系.
①将固体混合物溶于水,搅拌后得无色透明溶液;
②往此溶液中滴加BaCl2溶液,有白色沉淀生成;
③过滤,将沉淀物置于足量稀硝酸中,发现沉淀全部溶解.
试判断:
-
(1) 固体混合物中肯定有,肯定没有,可能有.
-
(2) 写出有关的离子方程式:实验②;实验③.
|
序号 |
操作及现象 |
|
实验1 |
取放置一段时间后依然无色的0.1mol/LKI溶液,加入淀粉溶液,溶液不变蓝;向溶液中继续加入2滴6mol/L的稀硫酸,溶液立即变蓝 |
|
实验2 |
取新制的0.1mol/LKI溶液,加入淀粉溶液,溶液不变蓝;向溶液中继续加入2滴6mol/L的稀硫酸,溶液10s后微弱变蓝 |
-
(1) 溶液变蓝,说明溶液中含有 。结合实验1和实验2,该小组同学认为酸化能够加快I-氧化反应的速率。
-
(2) 同学甲对滴加稀硫酸后溶液变蓝速率不同的原因提出猜想:放置一段时间后的0.1mol/LKI溶液成分与新制0.1mol/LKI溶液可能存在差异,并继续进行探究。
实验3:取新制0.1mol/LKI溶液在空气中放置,测得pH如下:
时间
5分钟
1天
3天
10天
pH
7.2
7.4
7.8
8.7
资料:
ⅰ.pH<11.7时,I-能被O2氧化为I。
ⅱ.一定碱性条件下,I2容易发生歧化,产物中氧化产物与还原产物的物质的量之比为1∶5。
①用化学用语,解释0.1mol/LKI溶液放置初期pH升高的原因:。
②对比实验1和实验2,结合化学用语和必要的文字,分析实验1中加稀硫酸后“溶液立即变蓝”的主要原因可能是。
-
(3) 同学甲进一步设计实验验证分析的合理性。
序号
操作
现象
实验4
重复实验2操作后,继续向溶液中加入 。
溶液立即变蓝
-
(4) 该组同学想进一步探究pH对I2发生歧化反应的影响,进行了如下实验。
实验5:用20mL 4种不同浓度的KOH溶液与2mL淀粉溶液进行混合,测量混合液的pH后,向其中加入2滴饱和碘水,观察现象。记录如下:
实验组
A
B
C
D
pH
11.4
10.6
9.5
8.4
现象
无颜色变化
产生蓝色后瞬间消失
产生蓝色,30s后蓝色消失
从实验5可以看出pH越大,歧化反应速率越(填“快”或“慢”)。
解释pH=8.4时,“产生蓝色,30s后蓝色消失”的原因:。


下列说法中,错误的是( )
 、
、 、
、 和
和 . 取少量样品进行如下实验:
. 取少量样品进行如下实验:①溶于水,得到无色透明溶液
②向①的溶液中滴加过量稀盐酸,溶液变浑浊,有刺激性气体逸出.离心分离.
③取②的上层清液,向其中滴加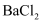 溶液有沉淀生成.
溶液有沉淀生成.
该样品中确定存在的是( )
 B .
B .  C .
C .  D .
D . 
目的 | 操作 | |
A | 降低液溴的贮存与使用风险 | 稀H2SO4酸化n(KBrO3):n(KBr)=1:5的混合液替代溴水 |
B | 除去Fe(OH)3胶体中的Fe3+、Cl- | 用滤纸将待提纯的Fe(OH)3胶体包好,放入盛有蒸馏水的烧杯中,更换蒸馏水,重复几次 |
C | 除去NO中的NO2 | 先后通过盛有蒸馏水、浓硫酸的洗气瓶 |
D | 验证浓H2SO4具有脱水性 | 将胆矾晶体悬挂于盛有浓H2SO4的密闭试管中,蓝色晶体逐渐变为白色 |



