化学实验方案的评价 知识点题库
选项 | 实验事实 | 结论 |
A | H2可在Cl2中燃烧 | 燃烧不一定有氧气参加 |
B | 铝箔在酒精灯火焰上加热熔化但不滴落 | 氧化铝熔点高于铝 |
C | 将SO2通入含HClO的溶液中,生成H2SO4 | HClO酸性比H2SO4强 |
D | 向FeCl2溶液中滴入KSCN溶液,在液面出现微红色 | Fe2+在空气中被氧化 |
选项 | 实验目的 | 实验图示 | 实验分析 |
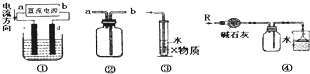
A | 实验室用酸性高锰酸钾溶液滴定草酸溶液 |
| 摇瓶时,使溶液向一个方向做圆周运动,勿使瓶口接触滴定管,溶液也不得溅出。 |
B | 石油分馏时接收馏出物 |
| 为收集到不同沸点范围的馏出物,需要不断更换锥形瓶。 |
C | 测定锌与稀硫酸反应生成氢气的速率 |
| 实验中,需测定的物理量是反应时间和生成氢气的体积。 |
D | 用四氯化碳萃取碘水中的碘 |
| 充分振荡后静置,待溶液分层后,先把上层液体从上口倒出,再让下层液体从下口流出。 |
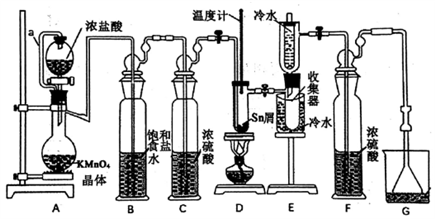
已知:① SnCl2、SnCl4有关物理性质如下表
|
物质 |
颜色、状态 |
熔点/℃ |
沸点/℃ |
|
SnCl2 |
无色晶体 |
246 |
652 |
|
SnCl4 |
无色液体 |
-33 |
114 |
② SnCl4极易和水反应生成SnO2·xH2O。
回答下列问题:
-
(1) 已知Sn的原子序数为50,则在Sn元素周期表中的位置为,画出Sn的原子结构示意图。
-
(2) 导管a的作用是,装置A中发生反应的离子方程式为。
-
(3) 当观察到装置F液面上方时才开始点燃D处的酒精灯,待锡熔化后适当增大氯气流量,继续加热。此时继续加热的目的是、。
-
(4) 若上述装置中缺少装置C(其它均相同),则D处具支试管中发生的主要副反应化学方程式为 。
-
(5) 若制得产品中含有少量Cl2 , 则可采用下列___________(填字母)措施加以除去。A . 加入NaOH萃取分液 B . 加入足量锡再加热蒸馏 C . 加入碘化钾冷凝过滤 D . 加入饱和食盐水萃取
| 选项 | 实验操作和现象 | 结论 |
| A | 向苯酚钠溶液中滴入少量醋酸,溶液变浑浊 | 酸性:醋酸>苯酚 |
| B | 向两支均盛有1mL蛋白质溶液的试管中分别加入乙酸铅、饱和 (NH4)2SO4溶液,均产生沉淀 | 蛋白质均发生了变性 |
| C | 向试管中加入少量麦芽糖,再加入2mL水溶解,片刻后再加入银氨溶液,水浴加热,管壁产生银镜 | 麦芽糖己水解且产物中含有葡萄糖 |
| D | 取卤代烃RX少许与NaOH溶液混合共热,冷却后加入足量HNO3 , 再滴加AgNO3溶液,产生白色沉淀 | X为Cl原子 |
编号 | 实验目的 | 实验过程 |
A | 配制0.1mol/L的FeCl3溶液 | 称取16.25 gFeCl3固体加入少量蒸馏水溶解,转移至1000mL容量瓶中定容 |
B | 探究H2O2的氧化性 | 向盛有2mL酸性KMnO4溶液的试管中滴入H2O2的溶液,观察溶液颜色变化 |
C | 制备纯净的SO2 | 向Na2SO3中加入浓硝酸,产生的气体通过浓硫酸 |
D | 制备Fe(OH)3胶体 | 将饱和的FeCl3溶液滴入沸水中,继续加热至液体变为红褐色 |
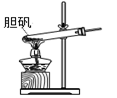 可用于胆矾分解
B .
可用于胆矾分解
B . 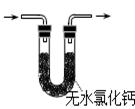 可用于检验产物是否含H2O
C .
可用于检验产物是否含H2O
C . 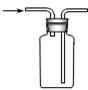 可用于收集SO2
D .
可用于收集SO2
D . 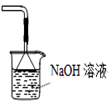 可用于吸收胆矾分解的SO2
可用于吸收胆矾分解的SO2
| 实验操作及现象 | 实验结论 | |
| A | 用石墨作电极电解CuSO4溶液,某电极附近有蓝色沉淀生成 | 该电极为阳极 |
| B | 向2 mL 0.1 mol·L-1 NaOH溶液中滴加3滴0.1 mol·L-1MgCl2溶液,出现白色沉淀后,再滴加3滴 0.1 mol·L-1FeCl3溶液,出现红褐色沉淀 | 溶解度:Mg(OH)2>Fe(OH)3 |
| C | 分别向2 mL 0.1 mol·L-1 CH3COOH溶液和2 mL 0.1 mol·L-1 H3BO3溶液中滴加等浓度的NaHCO3溶液, 前者有气泡产生,后者无明显现象 | 酸性:CH3COOH>H2CO3>H3BO3 |
| D | 向2 mL 5%的双氧水中分别滴加2滴0.1 mol/L Fe2(SO4)3和0.1 mol/L CuSO4溶液,前者产生气泡较快 | 对双氧水分解催化效果:Fe3+>Cu2+ |
-
(1) 汽车尾气中的 NO(g)和CO(g)在一定温度和催化剂条件下可发生如下反应:
2NO(g)+2CO(g)
 N2(g)+2CO2(g) ΔH
N2(g)+2CO2(g) ΔH已知:CO燃烧热的ΔH1=-283.0kJ/mo1
N2(g)+O2(g)=2NO(g) ΔH2=+180.5kJ/mo1,则ΔH= 。
-
(2) 某研究小组对反应 NO2+SO2
 SO3+NO ΔH <0进行相关实验探究。在固定体积的密闭容器中,使用某种催化剂,改变原料气配比[n(NO2):n(SO2)]进行多组实验(各次实验的温度可能相同,也可能不同),测定 NO2 的平衡转化率 [α(NO2)],部分实验结果如图1所示。
SO3+NO ΔH <0进行相关实验探究。在固定体积的密闭容器中,使用某种催化剂,改变原料气配比[n(NO2):n(SO2)]进行多组实验(各次实验的温度可能相同,也可能不同),测定 NO2 的平衡转化率 [α(NO2)],部分实验结果如图1所示。 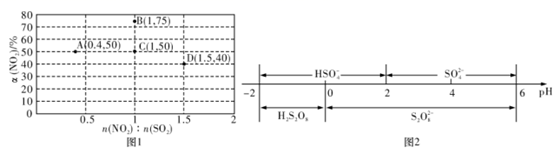
①如果将图中B点的平衡状态改变为C点的平衡状态,应采取的措施是。
②图中B、D两点对应的实验温度分别为TB和TD , 通过计算判断:TBTD(填“>”“=”或“<”)。
-
(3) 工业废气也是产生雾霾的重要原因,某厂采用湿法 K2S2O8氧化脱硝综合处理燃煤锅炉烟气,提高了烟气处理效率。
①K2S2O8水解时生成 H2O2和 KHSO4 , 写出该反应的化学方程式:。
②过二硫酸钾可通过电解 KHSO4溶液的方法制得。电解液中含硫微粒主要存在形式与pH 的关系如图2所示。
已知在阳极放电的离子主要是 HSO
 ,阳极区电解质溶液的pH 范围为 ;阳极的电极反应式为。
,阳极区电解质溶液的pH 范围为 ;阳极的电极反应式为。
-
(1) 氯气与水反应产生的HClO可去除废水中含有的NH3。
已知:NH3(aq)+HClO(aq)=NH2Cl(aq)+H2O(l) ΔH=a kJ·mol-1
2NH2Cl(aq)+HClO(aq)=N2(g)+H2O(l)+3H+(aq)+3Cl-(aq) ΔH=b kJ·mol-1
则反应2NH3(aq)+3HClO(aq)=N2(g)+3H2O(l)+3H+(aq)+3Cl-(aq)的ΔH=kJ·mol-1。
-
(2) 在酸性废水中加入NaCl进行电解,阳极产生的HClO可氧化氨氮。电解过程中,废水中初始Cl-浓度对氨氮去除速率及能耗(处理一定量氨氮消耗的电能)的影响如图所示。

①写出电解时阳极的电极反应式:。
②当Cl-浓度减小时,氨氮去除速率下降,能耗却增加的原因是。
③保持加入NaCl的量不变,当废水的pH低于4时,氨氮去除速率也会降低的原因是。
-
(3) 高铁酸钾(K2FeO4)是一种高效氧化剂,可用于氨氮处理。K2FeO4在干燥空气中和强碱性溶液中能稳定存在。氧化剂的氧化性受溶液中的H+浓度影响较大。
①碱性条件下K2FeO4可将水中的NH3转化为N2除去,该反应的离子方程式为。
②用K2FeO4氧化含氨氮废水,其他条件相同时,废水pH对氧化氨氮去除率及氧化时间的影响如图所示。当pH小于9时,随着pH的增大,氨氮去除率增大、氧化时间明显增长的原因是。


根据设计要求回答:
-
(1) 装置E的名称是,D装置中使用球形干燥管的作用。
-
(2) 写出CH4与Cl2生成一氯代物的化学反应方程式,该反应的类型是
-
(3) B装置有三种功能:①控制气体流速;②干燥气体;③。
-
(4) 若D装置中盛有AgNO3溶液,现象是有白色沉淀产生。此现象并不能说明该有机反应的类型。为了证明该反应有HCl生成,将装置进行改进:
①在A、B装置间增加一个盛有的洗气瓶;②。
-
(5) 在C装置中,经过一段时间的强光照射,发现硬质玻璃管内壁有黑色小颗粒产生,写出置换出黑色小颗粒的化学方程式:
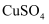 溶液,甲瓶为100mL 1.0mol/L
溶液,甲瓶为100mL 1.0mol/L 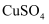 溶液,乙瓶为100g 15%
溶液,乙瓶为100g 15% 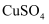 溶液。
溶液。
-
(1) 若将乙瓶溶液的浓度转化为物质的量浓度,还需要的物理量是。
-
(2) 实验室用
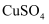 固体配制两种溶液,配制甲瓶溶液比配制乙瓶溶液多出的仪器是。
固体配制两种溶液,配制甲瓶溶液比配制乙瓶溶液多出的仪器是。
-
(3) 配制过程中需要“摇匀”,写出配制甲瓶溶液“摇匀”的具体操作。
-
(4) 配制甲瓶溶液时,未经冷却,直接转移到容量瓶中,所配溶液的浓度将 (填“偏大”“偏小”或“不变”)
-
(5) 实验室制取硫酸铜有以下两种方案:
方案一:
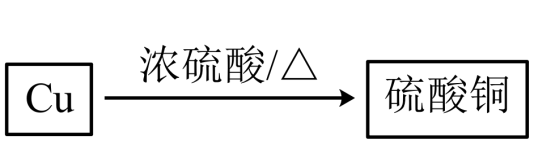
方案二:

上述两种方案中(填“方案一”或“方案二”)更优,理由是。
选项 | 操作 | 现象 | 结论 |
A | 将CH3CH2Br与NaOH溶液共热,冷却后,取出上层水溶液加入AgNO3溶液 | 产生淡黄色沉淀 | CH3CH2Br中含有溴原子 |
B | 向2 mL10%的NaOH溶液中滴入2%的CuSO4溶 液4至6滴,得到新制的Cu(OH)2悬浊液,然后加入乙醛溶液0.5 mL,振荡后加热 | 产生砖红色沉淀 | 醛基具有还原性 |
C | 将乙醇与浓硫酸共热至170℃所得气体直接通入酸性KMnO4溶液中 | KMnO4溶液褪色 | 乙醇发生消去反应的产物为乙烯 |
D | 向苯酚钠溶液中通入一定量CO2 | 溶液变浑浊 | 碳酸的酸性比苯酚的酸性强 |
实验目的 | 玻璃仪器 | 试剂 | |
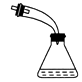
A | 检验 | 试管、胶头滴管、酒精灯 |
|
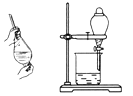
B | 制备无水乙醇 | 蒸馏烧瓶、牛角管、酒精灯、冷凝管、锥形瓶 |
|
C | 实验室制备乙烯 | 酒精灯、圆底烧瓶、温度计、导气管、胶头滴管 | 浓硫酸、乙醇碎瓷片 |
D | 除去苯中少量的苯酚 | 普通漏斗、烧杯、玻璃棒 | 浓溴水 |
实验目的 | 实验方案 | 现象和结论 | |
A | 探究乙醇消去反应的产物 | C2H5OH与浓硫酸(体积比约为1:3)的混合液,放入几块碎瓷片,170℃共热,将产生的气体通入酸性KMnO4溶液中 | 若酸性KMnO4溶液褪色,则乙醇消去反应的产物为乙烯 |
B | 探究乙酰水杨酸( 样品中是否含有水杨酸( | 取少量样品,加入3mL蒸馏水和少量乙醇,振荡,再加入1-2滴FeCl3溶液 | 若有紫色沉淀生成,则该样品中含有水杨酸 |
C | 探究麦芽糖是否发生水解 | 取2mL20%的麦芽糖溶液于试管中,加入适量稀H2SO4后水浴加热5min,冷却后先加足量NaOH溶液,再加入适量新制Cu(OH)2悬浊液并加热煮沸 | 若生成砖红色沉淀,则麦芽糖已水解 |
D | 探究KI与FeCl3反应的限度 | 取5mL0.1mol·L-1KI溶液于试管中,加入1mL0.1mol·L-1FeCl3溶液,充分反应后滴入5滴15%KSCN溶液 | 若溶液变血红色,则KI与FeCl3的反应有一定限度 |


 中的溴元素
中的溴元素 溶液、硝酸、
溶液、硝酸、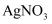 , 溶液
, 溶液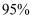 乙醇
乙醇 )
) )
)


