物质发生化学变化时的能量变化 知识点题库
-
(1) 目前,我国一些城市推广使用“乙醇汽油”作汽车燃料:
①乙醇属于化合物(填“有机”或“无机”).
②写出乙醇完全燃烧的化学方程式:.
-
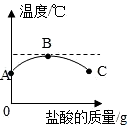
(2) 将稀盐酸慢慢滴入装有氢氧化钠溶液的烧杯中,用温度计测出烧杯中溶液的温度,溶液温度随加入稀盐酸的质量而变化如图所示:
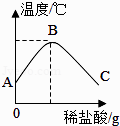
①由图知,稀盐酸与氢氧化钠溶液发生的反应是(填“放热”或“吸热”)反应.
②从A到B过程中,烧杯中溶液的pH逐渐.B点表示的含义是.
-
(3) 小明家菜地里的蔬菜叶子发黄了,妈妈叫他去买化肥碳酸氢铵(NH4HCO3)来施用,当他到化肥商店时,碳酸氢铵刚好缺货,你建议他买 (填“尿素”或“氯化钾”),也能起到与碳酸氢铵相同的作用.
-
(1) 铅蓄电池充电时是将电能转化为(填序号)。
a、机械能 b、热能 c、化学能
-
(2) 铅蓄电池放电过程中,反应的化学方程式为Pb+PbO2+2H2SO4═2PbSO4+2H2O,据此可知,铅蓄电池在放电时,溶液的pH不断(填“增大”、“减小”或“不变”)。
-
(3) 废铅蓄电池可以回收利用。
①从材料分类角度看,外壳塑料属于材料(填写“有机合成”、“复合”或“无机非金属”)。
②废硫酸可以与氟磷灰石[Ca5(PO4)3F]反应,反应的化学方程式为:2Ca5(PO4)3F+7H2SO4═3CaSO4+3Ca(H2PO4)2+2HF,反应产物中可用作化肥的物质是 (填写化学式)。
③下表是一些金属熔点的数据:
金属
锡
铅
铋
镉
熔点∕℃
231.9
327.5
271.3
320.9
日常所用保险丝由铋、铅、锡、镉等金属组成,其熔点约为(填序号)
A.300﹣320℃ B.230﹣250℃ C.60﹣80℃ D.20﹣40℃
④废硫酸直接排放会污染环境,拟选用如表物质中和后再排放:
物质
CaCO3
Ca(OH)2
NH3
NaOH
市场参考价(元/kg)
1.8
2.0
6.5
11.5
已知:2NH3+H2SO4=(NH4)2SO4 , 如果要求花最少的钱来中和等质量、等浓度的废硫酸,则应选择(填序号)。
A、CaCO3 B、Ca(OH)2 C、NH3 D、NaOH
-
(1) 油罐车的尾部经常有一条铁链拖到地面上,利用了铁的(填铁的一种性质)
-
(2) 可用碘酒来检验大米、面粉等食物中是否含有 (填名称)
-
(3) 生活中降低水的硬度可采用的方法是 ;
-
(4) 手机应用比较广泛,其中手机电池的原理是将能转化为电能。
【提出问题】氢氧化钠溶液与稀盐酸混合是否发生了化学反应?
【猜想与假设】
a.二者混合发生了化学反应
b.二者混合没有发生化学反应
【设计并实验】
实验操作 | 实验现象 | |
甲同学 | 在盛有10mL一定浓度的氢氧化钠溶液的烧杯中,用胶头滴管慢慢滴入1﹣2滴稀硫酸,振荡,同时测定溶液的pH | 溶液pH减小但仍大于7 |
乙同学 | 在盛有10 mL一定浓度的氢氧化钠溶液的烧杯中,先滴入几滴无色酚酞溶液,然后再加入稀硫酸 | 溶液由红色变为无色 |
【得出结论】氢氧化钠与稀硫酸发生了化学反应
-
(1) 乙同学认为甲的设计不合理,原因是,改进的方法是,根据改进的实验现象说明二者混合后发生了化学变化,写出氢氧化钠与稀硫酸反应的化学方程式.
-
(2) 探究稀硫酸与氢氧化钠溶液是否恰好完全反应.
乙同学在做完稀硫酸与氢氧化钠溶液反应得到实验后,为探究稀硫酸与氢氧化钠是否恰好完全反应,设计了实验方案二
【思考与交流】
实验步骤
实验现象
结论
取少量碳酸钠固体于试管中滴加乙同学上述反应后的溶液于试管中
若
稀硫酸(“过量”或“不过量”)
若没有明显现象
稀硫酸与氢氧化钠溶液恰好完全反应
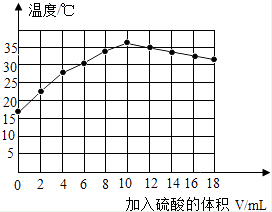
丙同学在绝热装置中,向分别盛有10 mL10%氢氧化钠溶液加入不同体积某浓度的稀硫酸,充分混合后溶液的温度变化曲线如图(最高温度18℃).
-
(3) 根据图示分析,稀硫酸和氢氧化钠的反应是(填“吸热”或“放热”)反应,加入稀硫酸mL时,二者恰好完全反应.

-
(1) 你认为苏-25的起落架应具有的性质是;
A.强度大 B.密度小 C.制造成本低
-
(2) 苏-25所用的燃料当中有一种是CH3(CH2)8CH3 , 该燃料燃烧的生成物为,化学反应前后氧元素的化合价分别是;
-
(3) 该飞机在行驶过程中的能量转化过程是:。
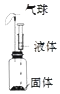
A. | B. | C. | D. | |
固体 | 氯化钠 | 生石灰 | 双氧水 | 铁粉 |
液体 | 水 | 水 | 二氧化锰 | 稀硫酸 |
 也能使紫色的石蕊试液变红,所以
也能使紫色的石蕊试液变红,所以  是酸
C . 置换反应的生成物是单质和化合物,有单质和化合物生成的反应一定是置换反应
D . 镁粉与盐酸反应放出热量,证明化学反应不仅生成新物质还伴随能量的变化
是酸
C . 置换反应的生成物是单质和化合物,有单质和化合物生成的反应一定是置换反应
D . 镁粉与盐酸反应放出热量,证明化学反应不仅生成新物质还伴随能量的变化

-
(1) 黑龙江盛产优质水稻,其加工得到的大米中含有丰富的淀粉,淀粉的化学式为;淀粉属于糖类,糖类在人体内经氧化放出能量,为机体活动和提供能量。
-
(2) 水稻生长期间需要施加氨肥,氮肥有促进植物;叶色浓绿,提高植物蛋白质含量的作用。请写出一种施用后在土壤中不残留有害物质的铵态氮肥(填化学式)。
-
(3) 有了科技的翅膀,粮仓变得越来越稳定。经过 40年的发展,黑龙江省农业机械化水平实现了质的飞跃。某种收割机的燃料为柴油,则在其收割水稻的过程中,发生的能量转化全过程为(用“→”表示转化)。
-
(1) 下列能源不属于新能源的是______(填字母)。A . 氢能 B . 核能 C . 石油 D . 风能
-
(2) 电池的能量转换方式是能转化为电能。
-
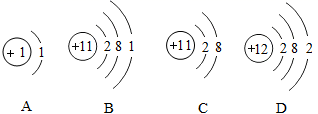
(3) 锂电池可为新能源汽车提供动力,下列结构示意图表示的粒子与锂原子的化学性质最为相似的是(填字母)。
-
(4) 锂(Li)的金属活动性强于铝,它与稀硫酸反应的化学方程式为,新能源汽车除了节约化石能源外,其主要优点是。
-
(1) 下列成语的原意与燃烧不相关的是____(填字母序号)。A . 卧薪尝胆 B . 釜底抽薪 C . 火上浇油 D . 煽风点火
-
(2) 古籍《天工开物》就有“煤饼烧石成灰”的记载。“烧石成灰”是指在高温条件下将石灰石(主要成分是碳酸钙)转化为生石灰。
① “烧石成灰”的过程中,能量转化的主要方式是将能转化为能 。
②“石”转化为“灰”的反应属于(填基本反应类型)。
③“灰”遇水成浆,该反应的化学方程式为。
-
(3) 室内起火时,如果急于打开门窗,火反而会烧得更旺。原因是。

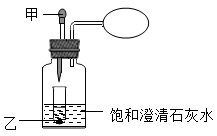
选项 | 锥形瓶内固体 | 胶头滴管内液体 |
A | 生石灰 | 水 |
B | 氢氧化钠 | 水 |
C | 硝酸铵 | 水 |
D | 大理石 | 稀盐酸 |
-
(1) 写出该反应的化学方程式。
-
(2) 稀盐酸与氢氧化钠溶液发生的中和反应是(填“吸热”“放热”或“无热量变化”)反应。

可供选择的药品见表:
|
组别 |
药品 |
||||
|
铁粉/g |
碳粉/g |
水/滴 |
食盐/g |
其他 |
|
|
一 |
5.0 |
0.1 |
0 |
0 |
干燥剂 |
|
二 |
5.0 |
0.1 |
10 |
0 |
无 |
|
三 |
5.0 |
0.1 |
10 |
1.0 |
无 |
|
四 |
5.0 |
0.1 |
0 |
1.0 |
无 |
-
(1) 铁在空气中锈蚀生成铁锈。铁锈的主要成分是(填化学式)。
-
(2) 在A、B两只试剂瓶中依次加入第一组和第二组药品进行实验。
①600s内A瓶中O2含量几乎不变,B瓶中不断减少。实验表明,铁在空气中锈蚀是铁和O2、发生了化学反应。
②将第二组药品中的水改为迅速冷却的沸水,且用量增多至足以完全浸没固体混合物。600s内B瓶中O2含量也略有减少,主要原因是。
-
(3) 为探究食盐对钢铁锈蚀速率的影响,应选择的药品组别是(填序号)。
-
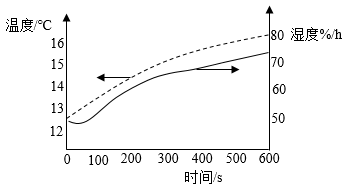
(4) 在两只试剂瓶中均加入第二组药品,分别改用温度和湿度传感器测得结果如图所示。瓶内湿度随时间增大(即水蒸气含量增大),根本原因是。
-
(5) 请提出一种防止钢铁生锈的方法:。



