二氧化碳的实验室制法 知识点题库
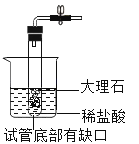
B .
B . 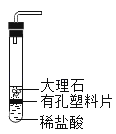
C .
C . 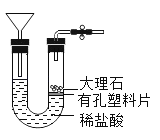
D .
D . 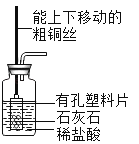
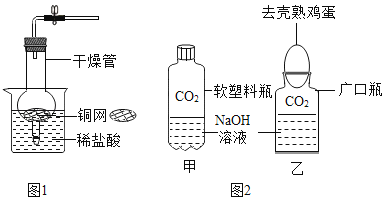
CO2是初中化学重点研究的气体之一.某化学兴趣小组设计了如下实验来探究CO2的制取和性质,为:甲——软塑料瓶变瘪,乙——“瓶吞鸡蛋”.
-
(1) 该兴趣小组用干燥管、烧杯、铜网等设计装配了一个在实验室中制取二氧化碳气体的装置,如图1所示.在干燥管内的铜网上应盛放
-
(2) 该兴趣小组同学将制得的CO2分别通人澄清石灰水和氢氧化钠溶液中,他们观察到前者变浑浊,后者无明显现象.写出石灰水变浑浊的化学方程式:
CO2和NaOH是否发生了化学反应?
①小明设计了甲、乙两个实验来验证CO2与NaOH发生了化学反应,如图2所示.实验现象.小雯同学提出质疑,她认为上述实验还不足以说明CO2和NaOH发生了反应.其理由是
②小虎向甲实验后变瘪塑料瓶的溶液中加入 ,观察到 现象,从而证明CO2与NaOH已经发生了反应.
写出塑料瓶中先后发生的两个化学方程式
①生成二氧化碳的质量.
②样品中碳酸钙的质量分数.
③所用稀盐酸中溶质的质量分数.
-
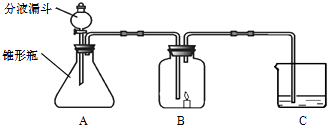
(1) 小明在分液漏斗、锥形瓶和C中分别加了药品,并使之混合,再盖上B的塞子,连接成如图所示,发现B中的蜡烛熄灭,C中的溶液变浑浊,写出C中反应的化学方程式.
-
(2) 小白也在分液漏斗、锥形瓶和C中分别加了药品,并使之混合,再盖上B的塞子,连接成如图所示,发现B中的蜡烛燃烧的更旺,C中的溶液也变浑浊,写出A中发生反应的方程式.小白说C中的现象证明蜡烛中含有碳元素,你认为小白说的对吗?.请简述理由.
-
(3) 小白想进一步探讨C中白色浑浊物的成分,把C中的白色浑浊物从水溶液中分离出来了,她用的方法是.
-
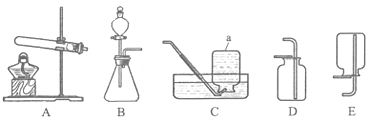
(1) 仪器a的名称是;组装A装置时,酒精灯应在固定试管之(填“前”或“后”)放置.
-
(2) 实验室用高锰酸钾制取氧气,反应的化学方程式:,宜选用的发生装置是(填装置标号,下同),不宜选用的收集装置是
-
(3) 实验室制取二氧化碳的研究中,在其他条件相同的情况下,进行如下实验:
实验标号
药品
甲
乙
丙
丁
大理石(m0g)
块状
块状
粉末状
粉末状
盐酸(过量)
稀盐酸
浓盐酸
稀盐酸
浓盐酸
①实验室制取二氧化碳的化学方程式:.
②若要研究盐酸浓度大小对反应快慢的影响,可选择实验甲与(填实验编号)对照.
③除盐酸的浓度外,上述实验研究的另一个影响反应快慢的因素是.
④研究发现盐酸的浓度越大,产生气体越快.与甲比较,下列对丁分析正确的是(填标号)
A.反应更剧烈 B.产生的二氧化碳的质量更大 C.参加反应的大理石更多
-
(4) 请从实验原理、原料、发生装置、操作等方面,阐述下列实验中可以产生较平稳气体的主要原因.
实验目的
原料
发生装置
主要原因
制取氧气
粉末状二氧化锰和稀过氧化氢溶液
B

-
(1) 写出仪器a、b的名称:a是,b是.
-
(2) 用B装置制取氧气的化学方程式是,可选用的收集装置是(填序号).装药品前应首先进行.当实验结束时,甲同学先移去了酒精灯,忘记将导管从水槽中取出,在水未进入试管之前,可采取的补救措施有:①②.
-
(3) 实验室制取二氧化碳气体应选用的发生装置是(填序号),收集装置是(填序号),小雨同学选用该装置收集二氧化碳,并用燃着的小木条放在瓶口验证二氧化碳是否收集满,结果发现小木条始终不灭,说明该瓶气体没有集满.出现上述情况的原因可能是①,②,③(写出其中3条),将该气体通入澄清的石灰水中发生反应的化学方程式为.
-
(4) 将一瓶二氧化碳气体正立于烧杯中(装置见图2),敞口一会儿,集气瓶外壁上湿润的蓝色石蕊试纸自上面而下变红色,该现象说明分子具有的性质,还说明二氧化碳气体.
-
(5) 在实验室里制取氢气,发生装置与制二氧化碳的相同,收集方法可采用(填“向上”或“向下”)排空气法.若用如图3所示装置采用“排空气法”收集氢气,请在图中将导管补画完整.
-
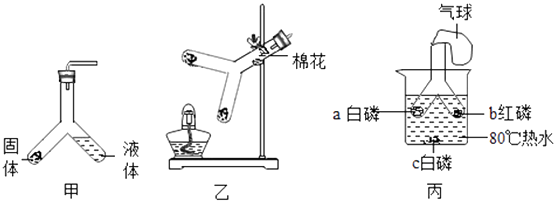
(1) 实验室利用装置甲制备少量二氧化碳:Y形管中盛放的固体物质是(填名称,下同),液体物质是.
-
(2) 实验室利用装置乙制备少量氧气:实验室,酒精灯应加热Y形管内(填“a”或“b”)处的高锰酸钾,反应的化学方程式为.
-
(3) 利用装置丙探究燃烧的条件(白磷着火点为40℃;红磷的着火点为240℃)
①通过比较装置丙内(填标号)处的实验现象,可推导出燃烧条件之一是温度达到可燃物的着火点.
A、a和b B、b和c C、a和c
②图2中能正确反映气球内气压(P)随反应时间(t)而发生变化的是(填标号).
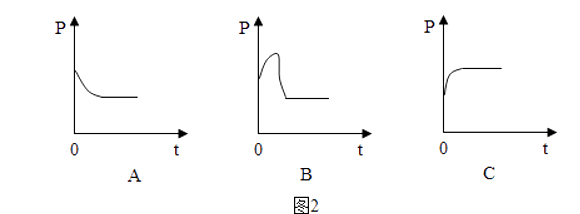
-
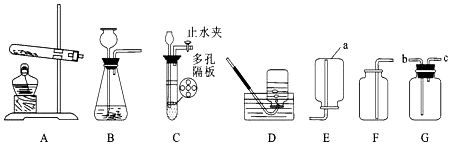
(1) 装置图中仪器a的名称为.
-
(2) 写出以混合物为原料用装置A制氧气的化学方程式;该装置中试管口略向下倾斜的原因是.
-
(3) 若用G装置采用排空法收集氢气,氢气应从进(选“b”或“c”).
-
(4) 制取二氧化碳最好选用的发生装置是(填字母).
①实验室用石灰石和稀硫酸制备二氧化碳时,收满二氧化碳的集气瓶应正立在桌面上
②实验室用锌和稀硫酸制备氢气时,收满氢气的集气瓶应倒立在桌面上
③点燃任何可燃性气体前,必须先验纯
④制备任何气体时,都要把反应装置中的空气排尽后,再用排水法收集.
-
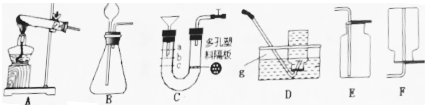
(1) 仪器g的名称是。
-
(2) 若选用A装置作为高锰酸钾制氧气的发生装置,试管口塞一团棉花的目的是。
-
(3) 请写出实验室制取二氧化碳的化学方程式。
-
(4) 甲烷的密度比空气小,难溶于水,实验室可用(填字母)装置收集甲烷。
-
(5) 作为气体发生装置,C装置相比较B,优点是,用C装置制取氢气,向漏斗中添加稀硫酸,应添加到图中(填“a”“b”“c”)处。
-
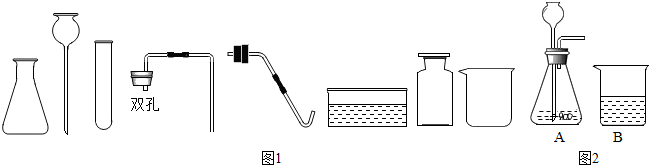
(1) 若补充仪器和(填名称),并利用上述部分仪器和药品可制取一种气体,则发生反应的化学方程式为,制取该气体时,需先检查装置的气密性;连接好仪器,将导管一端浸入水中,用手紧握容器外壁,使容器内温度,压强变,观察到水中导管口有时,说明装置不漏气。
-
(2) 若要制备并检验二氧化碳(如图2所示),需补充一种溶液,该溶液中溶质的俗称有,B中可观察到的实验现象是。
-
(3) 检验二氧化碳气体是否收集满的方法是。
-
(1) 实验室用固体制O2的化学方程式是。
-
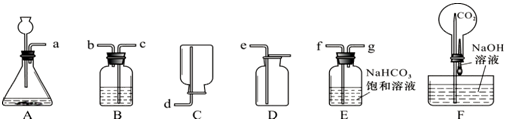
(2) 从如图中选用4个装置来制取较纯净的CO2气体。①正确的接口顺序从左到右依次为:
a接;②所选装置有一处明显的错误是,B中盛放的液体是。
-
(3) 用上图中的 F 装置可以制造十分有趣的“化学喷泉”。将胶头滴管中的 NaOH 溶液挤进圆底烧瓶时,很快看到长导管顶端产生“喷泉”现象。烧瓶中发生反应的化学方程式是。若将烧瓶内的CO2换成下列四种气体中的仍可产生“喷泉”现象(填序号)。
A SO2 B H2 C CO D HCl

-
(1) 仪器a的名称是。
-
(2) 实验室用高锰酸钾来制取氧气,可选择的发生装置为(填序号),其反应的化学方程式为,为了收集较为纯净的氧气,最好选用的收集装置是(填序号)。
-
(3) 实验室用石灰石和稀盐酸反应制取二氧化碳,选用的发生装置是(填序号)。用D装置收集二氧化碳气体时,导管伸至接近集气瓶底部的原因。
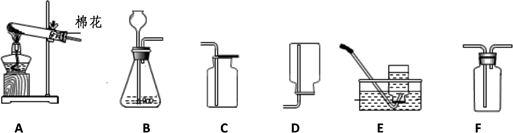
-
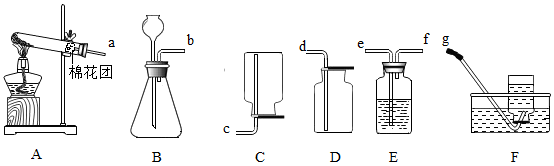
(1) 写出装置A制取氧气的化学方程式.
-
(2) 收集一瓶氧气用于完成铁丝在氧气中燃烧的实验最好用(填序号)装置。
-
(3) 写出实验室制取二氧化碳的化学反应方程式.
-
(4) 若用F装置干燥二氧化碳,瓶中应装.
-
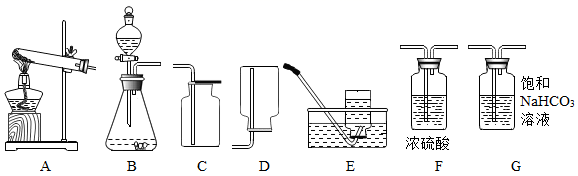
(1) 实验室用B装置制取CO2的化学方程式。
-
(2) 实验室要制取干燥的氢气,可选用如图所示的一些装置,导管口的连接顺序是什么?
-
(1) 写出实验室用过氧化氢溶液和二氧化锰制取氧气的化学方程式。
-
(2) 实验室用石灰石和稀盐酸反应制取二氧化碳时,应选用的发生装置是(填序号,下同),收集装置是。若要检验制得的气体是二氧化碳,请简述实验方案(写出步骤、现象以及结论)
-
(3) 若要除去二氧化碳气体中混有的少量氯化氢和水蒸气,可以将气体依次通过装置→。(填序号)

-
(1) 若要制取二氧化碳还需补充的仪器是(填名称)。
-
(2) 若补充一种用品还能制取氧气,发生反应的化学力程式为。
-
(3) 将制取氧气的装置图补充完整。
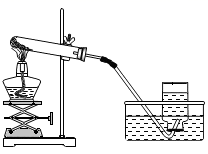
-
(4) 用排水法收集氧气,当观察到导管口有时,开始收集,气体逸出的原因是由于试管内温度升高且,使试管内压强,大于外界大气压,在压强差的作用下,气体逸出。
-
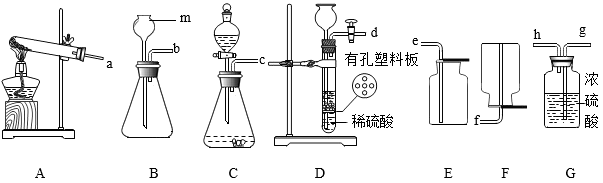
(1) 实验室制取二氧化碳时,可以选用的发生装置有(填仪器序号),反应的化学方程式为。
-
(2) 若用高锰酸钾制取一瓶干燥的氧气,仪器接口的连接顺序是(依次填仪器接口标号):用分解双氧水制氧气,与上述方法相比有的优点。
-
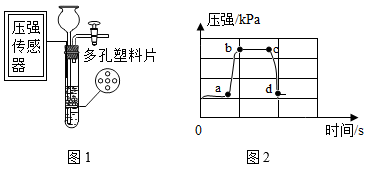
(3) 相比图中的B装置,D装置的优点是可以控制反应的发生或停止,为了解装置具有该优点的原因,在装置D中连接压强传感器(如图1),从而测定实验中试管内气体压强变化的情况(如图2)。ab段试管中液面逐渐(填“上升”或“下降”),c点对应的操作是。



