海洋中的资源 知识点题库
(1)元素资源:海水中含量最高的金属元素是 (填元素符号);从物质在水中溶解的规律和水天然循环的角度看,该元素含量最高的原因是 .
(2)淡水资源:淡化海水可以用(填字母代号);
| A.吸附法 | B.蒸馏法 | C.过滤法 | D.电解法 |
该过程是(填“化学变化”或“物理变化”).
(3)矿产资源:海底蕴藏着大量的“可燃冰”(含甲烷),甲烷燃烧的化学反应方程式为 .
(4)你还知道海洋中有哪些资源?(写一种)

-
(1) 图中①是(填“蒸发池”或“冷却池”)。
-
(2) 析出晶体后的母液是氯化钠的(填“饱和溶液”或“不饱和溶液”)。
-
(3) 实验室除去粗盐中难溶性杂质的主要实验步骤有:
Ⅰ 溶解 Ⅱ(填操作名称) Ⅲ 蒸发
上述三个步骤中,用到的同一种玻璃仪器的名称是,该玻璃仪器在步骤Ⅱ中的作用是。
-
(4) 将粗盐制成精盐后,现要配制
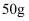 溶质质量分数为
溶质质量分数为 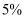 的氯化钠溶液,最取蒸馏水的量筒规格应选择 (填字母)。
A .
的氯化钠溶液,最取蒸馏水的量筒规格应选择 (填字母)。
A .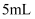 B .
B . 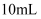 C .
C . 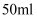 D .
D . 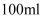
-
(5) 已知某粗盐样品中的杂质为氯化镁和泥沙。常温下,将
 该粗盐样品溶解于足量水中,过滤得到不足4g泥沙和
该粗盐样品溶解于足量水中,过滤得到不足4g泥沙和  溶液,取出
溶液,取出  溶液进行测定,其中含有镁元素
溶液进行测定,其中含有镁元素  ,氯元素
,氯元素 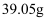 ,则原粗盐中氯化钠的质量分数为。
,则原粗盐中氯化钠的质量分数为。


三餐的白米饭中可以加点粗粮和番薯
摄入富含蛋白质的食物

搭配新鲜蔬菜和水果
-
(1) 米饭中的淀粉在人体内经酶的催化作用,与水发生一系列反应,最终变成葡萄糖,葡萄糖的化学式为。摄入的蛋白质是由多种构成的极为复杂的化合物。蔬菜和水果中富含的营养素(除水外)可以起到调节新陈代谢、、维持身体健康的重要作用。
-
(2) 葡萄是人们喜欢吃的一种水果。在葡萄生长发育过程中对钾肥的需求量超过其他果树。钾具有保证各种代谢过程的顺利进行,促进植物生长,增强和能力等功能。请写出一种钾肥的化学式。
-
(3) 下图是利用海水提取粗盐的过程

图中A是池,析出晶体后的母液是氯化钠的(填“饱和溶液”或“不饱和溶液”)。

请填写下列空白:
-
(1) B的俗名是;D的化学式;
-
(2) 写出卤水→D的化学方程式;
-
(3) 金属镁的冶炼因为镁金属相对活泼,用常见还原剂达不到目的,因此常用电解的方法,请写出化学方程式。
-
(4) 镁条点燃后产生耀眼的白光,将燃着的镁条插入一瓶纯净的二氧化碳中,发现燃烧继续进行,并没有出现我们初中阶段所认为必然会出现的现象。这说明,我们初中阶段所学的燃烧三要素中的这一条还需要进一步完善。在二氧化碳化学性质中,它能够用于这一条也需要强调某些前提。

-
(1) 提取物质常用转化的方法,就是将杂质转化为沉淀或气体而除去。粗盐中含有氯化镁、硫酸钠、氯化钙等可溶性杂质,通过步骤I,再利用过滤操作进行除杂。步骤I加入下列三种溶液的先后顺序为(填字母序号),而后需要加入(填试剂名称)制得精盐水。
A稍过量的Na2CO3溶液 B稍过量的BaCl2溶液 C稍过量的NaOH溶液
-
(2) 母液中有MgCl2 , 又经历了步骤Ⅳ、V的转化过程,其目的是。
-
(3) 化学变化是改造物质的重要途径。上述流程图中没有涉及基本反应类型是。
-
(1) 如图是利用海水提取粗盐的过程:

①图中M是池。
②根据海水晒盐的原理,下列说法中错误的是(填标号)。
A海水进入贮水池,海水的成分基本不变
B在M中,海水中氯化钠的质量逐渐增加
C在M中,海水中水的质量逐渐减少
D析出晶体后的母液是氯化钠的不饱和溶液
③海水在浓缩过程中,密度与析出盐的种类和质量(g)关系如表:
海水密度(g/mL)
析出盐的种类和质量(g)
CaSO4
NaCl
MgCl2
MgSO4
NaBr
1.13
0.56
1.20
0.91
1.21
0.05
3.26
0.004
0.008
1.22
0.015
9.65
0.01
0.04
1.26
0.01
2.64
0.02
0.02
0.04
1.31
1.4
0.54
0.03
0.06
Ⅰ.分析数据可知,普通海水的密度小于g/mL。
Ⅱ.海水晒盐的过程中,母液的密度应控制在g/mL范围内,原因是。
-
(2) 实验室用氯化钠固体配制100g质量分数为16%的氯化钠溶液。
①实验中除了用到托盘天平(含砝码)、药匙、烧杯、量筒、试剂瓶外,还需用到的玻璃仪器是。
②量取水时,应选用的量筒规格是mL(填“10”“100”或“250”);若仰视读数(其它操作正确),所得溶液的溶质质量分数16%(填“大于”“小于”或“等于”)。
③ 常温下氯化钠的溶解度是36g。农业上常用质量分数为16%的氯化钠溶液来选种,该溶液是溶液(填“饱和”或“不饱和”)。
④ 要将配制好的100g质量分数为16%的氯化钠溶液变成质量分数为24%的氯化钠溶液,需要再加入NaCl的质量是g(计算结果精确到0.1)。

-
(1) 操作A是。
-
(2) 写出生成氢氧化镁的化学方程式。
-
(3) 得到氢氧化镁需要洗净,为证明是否洗净,可取洗涤液少量,向其中加入下列试剂中______。A . 石灰水 B . 硝酸银溶液 C . 碳酸钠溶液 D . 氢氧化钠溶液

-
(1) 海水淡化。
①蒸馏法是常用的海水淡化方法,该方法是利用混合体系中各物质的不同,将物质进行分离。
②下图所示为膜分离法淡化海水,水分子可以通过淡化膜(海水中体积较大的盐的离子和其他分子不能通过)进入左侧的淡水池,从而得到淡水。下列说法中正确的是(填字母序号)。

A.膜分离法的原理与滤纸过滤原理类似
B.膜分离法还可以浓缩海水中的盐类物质
C.该膜分离法的目的是除去海水中的不溶物
-
(2) 海水制镁。步骤①②③是利用母液制镁的流程,该流程中发生中和反应的化学方程式是。步骤①中制取氢氧化镁选择向母液中加入石灰乳,而不是向海水中直接加入石灰乳,原因是。
-
(3) 海水晒盐
①利用盐田法晒盐,盐田通常分为蒸发池和结晶池两部分。下列说法正确的是(填字母序号)。
A.在蒸发池中水蒸发所需能量主要为太阳能和风能
B.在结晶池中主要通过降温结晶使氯化钠析出
C.当氯化钠晶体析出时,结晶池中的溶液为氯化钠的饱和溶液
②粗盐中常含有泥沙等难溶性杂质。在实验室中除去粗盐中的难溶性杂质,可依次通过、过滤、蒸发结晶等操作。蒸发结晶操作中要用到玻璃棒,其作用是。
③通过步骤④除去粗盐溶液中含有的MgCl2、Na2SO4、CaCl2等可溶性杂质,需要依次加入过量的BaCl2溶液、过量的Na2CO3溶液、过量的NaOH溶液,然后过滤,在滤液中加入适量的稀盐酸。其中加入过量的Na2CO3溶液的目的是。
-
(4) 步骤⑥是电解NaCl饱和溶液制取烧碱,该反应中的反应物是。
-
(5) 步骤⑦用烧碱低温制取次氯酸钠的反应原理为:
 ,则X的化学式是。
,则X的化学式是。



