海洋中的资源 知识点题库
-
(1) 海水中含有的氧、钠、镁、钾、硫、钙、溴、碳、锶和氟等化学元素占海水中溶解物质总量的99.8%以上.以上元素中,属于非金属元素的共种;
-
(2) 我国海滨砂矿资源包括金刚石等.金刚石坚硬且不导电,石墨质软且能导电,两者性质存在巨大差异的原因是;
-
(3) 油气资源中的“油”主要指石油,由石油获得航空煤油的方法是;“气”主要指天然气(主要成分为甲烷),它已逐渐成为家庭常用燃料,写出甲烷完全燃烧的化学方程式:.
-
(1) 海水中含有的阴离子包括Cl-、SO42-及(写出一种微粒符号即可)等;
-
(2) 苦卤中的溶质主要有:氯化镁、金属溴化物和(写出一种物质);
-
(3) 工业上把苦卤除钙后,再加入碱性沉淀剂可以制备氢氧化镁。若海水中钙离子含量太高,氢氧化钙会存在于氢氧化镁颗粒中,从而影响氢氧化镁的纯净度。某研究小组在控制反应温度是20~25℃和浓海水质量为1109g不变的条件下,进行下述对比实验,数据如下:
实验
碳酸钠加入量/g
搅拌速度 r/min
反应时间/h
钙除去率/%
a
1.78
200
3
44.8
b
2.32
200
3
60.2
c
2.32
125
4
55.1
d
2.32
200
4
64.6
①该对比实验中发生反应的化学方程式是;
②进行实验a和b的目的是。
③该实验显示(填实验因素)对钙的除去率的影响很小;
④搅拌速率越快,反应时间越长则消耗能源越多。为了节约能源,获得较高的钙除去率,进一步优化“搅拌速率”和“反应时间”的反应条件。在其他实验条件不变情况下,设计对比实验,你应选择的反应条件是(填选项)。
A.200r/min,3.5h B.200r/min,4.5h
C.175r/min,4h D.225r/min,4h
-
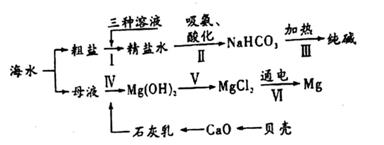
(1) 提纯物质常用转化的方法,就是将杂质转化为沉淀或气体而除去。粗盐中含有氯化镁、硫酸钠氯化钙等可溶性杂质,通过步骤Ⅰ,再利用过滤操作进行除杂。步骤加入下列三种溶液的先后顺序为(填字母序号)。
a.稍过量的Na2CO3溶液
b.稍过量的BaCl2溶液
c.稍过量的NaOH溶液
-
(2) 母液中有MgCl2 , 却经历了步骤Ⅳ、Ⅴ的转化过程,其目的是。
-
(3) 步骤Ⅱ中先向饱和食盐水中通入氨气,有利于二氧化碳的吸收,这样做的目的是,写出该反应的化学方程式。
-
(1) 食用海鱼、海虾等海鲜可为人体提供的营养素主要是________(填序号)。A . 糖类 B . 蛋白质 C . 维生素
-
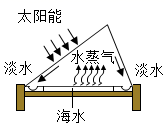
(2) 如图所示,是利用太阳能将海水淡化的过程。由海水变成淡水的过程属于(填物理或化学)变化。
-
(3) 从海水中获取粗盐的方法是采用蒸发结晶,而不是降温结晶,理由是。
-
(4) 海水提取粗盐后剩余的母液叫苦卤,利用苦卤制取金属镁的主要流程如下:
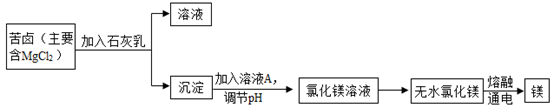
①流程中,溶液A为。
②测定氯化镁溶液的pH:用玻璃棒蘸取氯化镁溶液滴在上,然后再与对照,得出氯化镁溶液的pH。
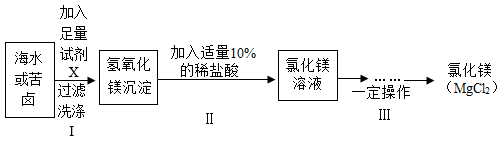
(信息)(一)海水和苦卤中都含有NaCl、Na2SO4、MgCl2、CaCl2、KCl等。
(二)苦卤是海水晒盐后剩余的溶液。
-
(1) 海水和苦卤都可以作为制取氯化镁的原料,甲同学提出选择苦卤更好,小组同学一致同意他的观点,理由是。
-
(2) 该方案制取氯化镁时,要经历步骤I和步骤II两步转化,其主要目的是。
-
(3) 小组同学按上述方案进行了实验,并制得19.0g干燥纯净的氯化镁固体。若步骤II中溶质质量分数为10%的稀盐酸与氢氧化镁恰好完全反应,且步骤Ⅲ中氯化镁没有损失,求步骤II中消耗稀盐酸的质量。(写岀计算步骤)。
-
(1) 海水晒盐。利用盐田法晒盐,盐田通常分为蒸发池和结晶池两部分。下列说法正确的是_____(填字母序号)。A . 在蒸发池中水蒸发所需能量主要为太阳能和风能 B . 在结晶池中主要通过降温结晶使氯化钠析出 C . 当氯化钠晶体析出时,结晶池中的溶液为氯化钠的饱和溶液 D . 湿度大、气温高有利于海水“晒盐”
-
(2) 粗盐的纯化。为了除去NaCl溶液中含有的少量MgCl2、CaCl2和Na2SO4杂质,某小组同学选用Na2CO3溶液、稀盐酸、Ba(OH)2溶液三种试剂,按一定顺序进行如图所示的实验。回答下列问题:
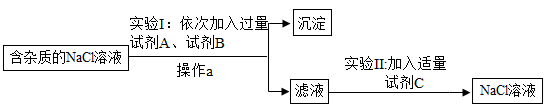
①操作a的名称是。
②实验I中加入的试剂B是。(填序号)
a、稀盐酸b、碳酸钠溶液c、氢氧化钡溶液
③实验Ⅱ中发生中和反应的化学方程式是。
-
(3) 海水制镁。工业以海水为原料提取镁的过程如下,回答下列问题:
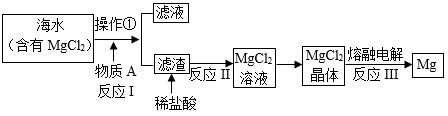
①为了使海水中含量较低的氯化镁富集,工业生产中通常向海水中加入物质A是(写化学式)使海水中的氯化镁转化为沉淀,该反应的化学方程式是,此过程富集氯化镁的同时也达到了的目的。
②反应Ⅲ的基本反应类型为。
-
(4) 海水制碱。氨碱法制纯碱使碳酸氢钠结晶析出的化学方程式是,将碳酸氢钠固体加热分解即得到纯碱。向滤出碳酸氢钠晶体后的NH4Cl溶液中加入熟石灰,可以回收氨气以循环使用,反应的化学方程式是。
-
(1) 《汉代古火井碑序》记载:“诸葛丞相躬莅视察,改进技法,刳斑竹以导气(气指沼气),引井火以煮盐”,请写出文中涉及到的化学反应的化学方程式:。

-
(2) 通过晾晒海水可以得到粗盐和卤水,上图为海水提取粗盐的过程,在结晶池中,继续风吹日晒,海水会变成食盐的溶液(填“饱和”或“不饱和”)。析出粗盐后,母液中氯化钠的溶质质量分数(填“变大”、“变小”或“不变”)。
-
(3) 氯化钠和硝酸钾在不同温度下的溶解度如下表所示。请根据下表回答:
温度/℃
20
30
40
50
60
70
80
溶解度/g
NaCl
36.0
36.3
36.6
37.0
37.3
37.8
38.4
KNO3
31.6
45.5
63.9
85.5
110
138
169
①60℃将100gKNO3溶解在100g水中,然后降温到40℃,降温后析出固体的质量是g。
②KNO3和NaCl溶解度相等的温度范围是。
③如下图所示,要使试管中有晶体析出,加入的试剂A是。

A.生石灰 B.氢氧化钠 C.硝酸铵固体 D.氯化钠固体
-
(1) 任务一:调查海水利用概况
【查阅资料】我国海水利用主要有海水直接利用、海水淡化、海水化学资源利用等。
【分析交流】两所学校的同学们共同获悉,海水里的化学资源有(写1种)。
-
(2) 任务二:咨询海水处理技术
【咨询专家】同学们通过数字化平台,向海洋专家进行了咨询,专家介绍, 海水淡化使用了反渗透膜淡化技术,其工作原理如图所示。

【小组讨论】同学们对以下两个问题,进行了网上交流并达成共识。
①海水通过反渗透膜,发生改变的是。
②淡化后的海水可用于(写1种)。
-
(3) 任务三:探究海水提取车间废水成分
沿海学校的同学获得一瓶海水提取车间的废水,在“云端”共同完成了如下探究。
【教师指导】①提取车间未经处理的废水含有酸性物质。②BaSO4为难溶于水的白色沉淀。
【猜想假设】该强腐蚀性废水中可能含有硫酸和盐酸。
【进行实验】设计实验方案,探究废水成分。
项目
实验步骤
实验现象
实验结论
方案
①取少量废水于试管中,滴入几滴紫色石蕊溶液。
废水中含有硫酸和盐酸
②另取少量废水于试管中,滴加过量Ba(NO3)2溶液,静置。
产生白色沉淀
③取步骤②的上层清液于试管中,滴加几滴。
产生白色沉淀
-
(4) 【反思评价】
①废水中不含碳酸根离子的原因是。
②步骤③中发生反应的化学方程式为。
-
(5) 任务四:展望海水发展前景
【小组交流】同学们了解到随着海水农业技术的创新和推广,富含碘、硒等微量元素的海水食物将为人类健康提供必要的保障,他们一致认为,经常食用可预防的疾病是(写1种)。
【成果分享】通过“云端”合作,同学们知道了海洋作为人类重要的资源宝库,不仅可以提供丰富的自然资源,还可以通过科技手段推动再生资源的开发和利用。



