常见金属的特性及其应用 知识点
铜:导电性好,呈红色,作装饰品、电线等
银、金:具有金属光泽,作手饰等
汞:常温为液态,作温度计
钨:高熔点性,作灯丝
常见金属的特性及其应用 知识点题库
铜是人类最早利用的金属之一.
(1)下列铜制品中,利用金属导热性的是 (填字母序号).

(2)“湿法炼铜”的原理是硫酸铜溶液与铁反应,该反应的化学方程式为 .
(3)利用废旧电池铜帽(含Cu、Zn)制取海绵铜(Cu),并得到硫酸锌溶液,主要流程如下(反应条件已略去):
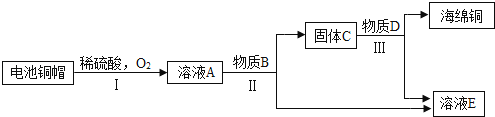
已知:2Cu+2H2SO4+O2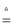 2CuSO4+2H2O
2CuSO4+2H2O
①过程Ⅱ中分离操作的名称是 .
②过程Ⅲ中有气体产生,反应的化学方程式为 .
③A~E中含铜、锌两种元素的物质有 (填字母序号).
①用砂纸打磨后的镁带是色的,硬度较,
②用夹持镁带放在酒精灯上加热,当镁带开始燃烧时再移到上方,可以观察到的现象是:abc
③将打磨后的镁带放入食醋中,观察到的现象是ab
④以上实验说明金属镁具有的化学性质是ab
⑤烟花、照明弹中都含有镁粉,其原因是

 铜制作导线
B .
铜制作导线
B .  不锈钢做锅
C .
不锈钢做锅
C .  钛做人造骨
D .
钛做人造骨
D . -
(1) 下列生活用品,属于金属材料制品的是(填序号)。
A 塑料水杯
B 大理石砖
C 不锈钢水盆
-
(2) 工业上用赤铁矿(主要成分Fe2O3)冶炼生铁的化学方程式为。
-
(3) 铁制品锈蚀的过程,实际上是铁与等物质 发生化学反应的过程。防止铁制栏杆生锈的方法之一是。
-
(4) 路边的太阳能路灯灯柱为铝合金材质,因为铝合金的要比铝大。

-
(1) 米中富含的营养素是。
-
(2) 发热包中的生石灰(CaO)能与水反应放出大量的热,该反应的化学方程式为。
-
(3) 锅是铝制的,铝能压成薄片制成铝锅,说明铝具有良好的(填序号)。
A导热性 B导电性 C延展性
-
(1) Cu和Al都能用作导线,因为Cu和Al具有良好的性。
-
(2) 分析反应:
 ,
, 
①Mn、Fe、Mg三种金属在溶液中的活动性,由强到弱的顺序是。
②将金属Mn放入硫酸铜溶液中,如果能反应,写出反应方程式。如果不能反应,说明理由。
-
(3) 如图是实验室探究铁生锈条件的一组对比实验,a和c两只试管对比,验证影响铁生锈的因素是。
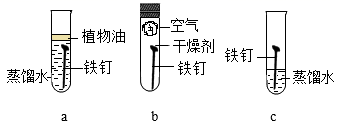
-
(1) 生活中使用铜丝来做导线,利用了金属良好的。
-
(2) 体温计中填充的银白色物质是(填化学符号)。
-
(3) 84消毒液主要成分为次氯酸钠(NaClO),写出次氯酸钠中阴离子的离子符号。
-
(4) 抗击“新型冠状病毒肺炎”疫情的战斗中,我们需要用75%的医用酒精进行室内消毒,酒精的化学式是。
-
(5) 加碘盐是在食盐中加入碘酸钾(KIO3),KIO3中碘元素的化合价为。
-
(1) 6个一氧化碳分子。
-
(2) 画出镁离子的结构示意图。
-
(3) 4个硫原子。
-
(4) 目前世界年产量最高的金属是。
-
(5) 过氧化钠(Na2O2)中氧元素的化合价是价。
玻璃在现代生活中占据着重要地位,玻璃杯、玻璃窗等随处可见。
玻璃的主要成分为硅酸盐和其他氧化物。我们以沙子(主要成分为 SiO2)为原料制作玻璃,向多次洗涤后的沙子中加入碳酸钠,升温至 2200℃,待固体呈现熔融状后冷却,就得到了粗制玻璃。
现如今,除了常规的玻璃外,还有很多功能独特的玻璃。
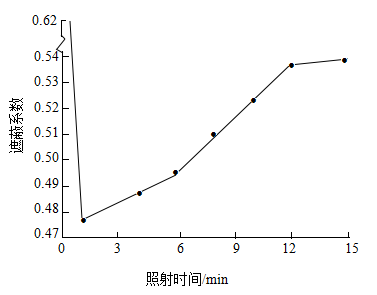
变色玻璃:在光照、温度等条件下能够改变颜色,当施加条件消失后又能自动恢复到初始状态的玻璃。如图为光照强度相同时,某种变色玻璃的遮蔽系数与太阳光照射时长的关系图。
防盗玻璃:在玻璃中间嵌有极细的金属丝,玻璃被击碎时,会立即发出报警信号。
高硼硅玻璃:比普通玻璃强度高,抗酸碱,无毒副作用,常用来制作玻璃餐具。
现今玻璃制造技术不断发展,日常生活和高科技领域,都不可缺少玻璃。
依据文章内容回答下列问题。
-
(1) 高温下,沙子中的 SiO2与碳酸钠反应,生成硅酸钠(Na2SiO3)和物质 X,物质 X 中一定含有的元素为和氧元素。
-
(2) 与普通玻璃相比,高硼硅玻璃的优点是(写出一条即可)。
-
(3) 判断下列说法是否正确(填“对”或“错”)。
①玻璃属于纯净物。
②防盗玻璃能报警体现了金属的导电性。
-
(4) 由图 1 可知,照射时间与遮蔽系数的关系是。



