жә¶и§ЈеәҰзҡ„еҪұе“Қеӣ зҙ зҹҘиҜҶзӮ№
еӣәдҪ“жә¶и§ЈеәҰзҡ„еҪұе“Қеӣ зҙ дё»иҰҒжҳҜжҢҮжё©еәҰгҖӮ
жіЁж„ҸдәӢйЎ№пјҡ
1гҖҒеӨ§йғЁеҲҶеӣәдҪ“йҡҸжё©еәҰеҚҮй«ҳжә¶и§ЈеәҰеўһеӨ§пјҢеҰӮзЎқй…ёй’ҫпјӣе°‘йғЁеҲҶеӣәдҪ“жә¶и§ЈеәҰеҸ—жё©еәҰеҪұе“ҚдёҚеӨ§пјҢеҰӮйЈҹзӣҗпјҲж°ҜеҢ–й’ пјүпјӣжһҒе°‘ж•°зү©иҙЁжә¶и§ЈеәҰйҡҸжё©еәҰеҚҮй«ҳеҸҚиҖҢеҮҸе°ҸпјҢеҰӮзҶҹзҹізҒ°гҖӮ
2гҖҒж°”дҪ“жә¶и§ЈеәҰзҡ„еҪұе“Қеӣ зҙ дё»иҰҒжҳҜжҢҮжё©еәҰе’ҢеҺӢејәгҖӮе…·дҪ“зҡ„еҸҳеҢ–规еҫӢжҳҜпјҡ
ж°”дҪ“зҡ„жә¶и§ЈеәҰйҡҸжё©еәҰзҡ„еҚҮй«ҳиҖҢеҮҸе°ҸпјҲйҡҸжё©еәҰзҡ„йҷҚдҪҺиҖҢеўһеӨ§пјүпјҢйҡҸеҺӢејәзҡ„еўһеӨ§иҖҢеўһеӨ§пјҲйҡҸеҺӢејәзҡ„еҮҸе°ҸиҖҢеҮҸе°ҸпјүгҖӮеҸҜд»Ҙз®Җи®°дёә 4 дёӘеӯ—пјҢеҚі“жё©еҸҚеҺӢжӯЈ”пјӣе…¶еҗ«д№үжҳҜж°”дҪ“зҡ„жә¶и§ЈеәҰдёҺжё©еәҰжҲҗеҸҚжҜ”е…ізі»пјҢдёҺеҺӢејәжҲҗжӯЈжҜ”е…ізі»гҖӮ
жә¶и§ЈеәҰзҡ„еҪұе“Қеӣ зҙ зҹҘиҜҶзӮ№йўҳеә“
еҰӮеӣҫжҳҜaгҖҒbгҖҒcдёүз§ҚеӣәдҪ“зү©иҙЁзҡ„жә¶и§ЈеәҰжӣІзәҝпјҢиҜ·еӣһзӯ”дёӢеҲ—й—®йўҳпјҡ
пјҲ1пјүиӢҘдҪҝaгҖҒcзҡ„йҘұе’Ңжә¶ж¶ІеҗҢж—¶жһҗеҮәжҷ¶дҪ“пјҢж–№жі•жҳҜ пјҺ
пјҲ2пјү в„ғж—¶пјҢaгҖҒcдёӨзү©иҙЁзҡ„жә¶и§ЈеәҰзӣёзӯүпјҺж°”дҪ“зҡ„жә¶и§ЈеәҰйҡҸжё©еәҰзҡ„еҸҳеҢ–规еҫӢдёҺгҖҖ пјҲеЎ«вҖңaвҖқгҖҒвҖңbвҖқжҲ–вҖңcвҖқпјүзӣёдјјпјҺ
пјҲ3пјүеңЁt2в„ғж—¶пјҢaгҖҒbгҖҒcдёүз§ҚйҘұе’Ңжә¶ж¶ІйҷҚжё©иҮіt1в„ғж—¶жә¶иҙЁзҡ„иҙЁйҮҸеҲҶж•°з”ұеӨ§еҲ°е°Ҹзҡ„йЎәеәҸжҳҜгҖҖ пјҢжһҗеҮәжҷ¶дҪ“жңҖеӨҡзҡ„жҳҜ пјҲеЎ«вҖңaвҖқгҖҒвҖңbвҖқжҲ–вҖңж— жі•зЎ®е®ҡвҖқпјүпјҺ
пјҲ4пјүеңЁt2в„ғж—¶пјҢе°Ҷ150е…Ӣaзҡ„йҘұе’Ңжә¶ж¶ІзЁҖйҮҠжҲҗиҙЁйҮҸеҲҶж•°дёә20%зҡ„жә¶ж¶ІйңҖеҠ ж°ҙ е…ӢпјҺ

-
пјҲ1пјү еҰӮиЎЁжҳҜKNO3гҖҒNaClеңЁдёҚеҗҢжё©еәҰдёӢзҡ„жә¶и§ЈеәҰпјҲеҚ•дҪҚпјҡg/100gж°ҙпјү
жё©еәҰпјҲв„ғпјү
0
10
20
30
40
50
60
70
80
90
100
KNO3
13.3
20.9
32
45.8
64
85.5
110
138
169
202
246
NaCl
35.7
35.8
36
36.3
36.6
37
37.3
37.8
38.4
39
39.8
в… .20в„ғж—¶пјҢNaClзҡ„жә¶и§ЈеәҰжҳҜ gпјҺ
в…Ў.30в„ғж—¶пјҢKNO3жә¶ж¶Ізҡ„жңҖеӨ§жө“еәҰпјҲжә¶иҙЁиҙЁйҮҸеҲҶж•°пјүдёәгҖҖ гҖҖпјҲеҸӘеҲ—и®Ўз®—ејҸпјҢдёҚйңҖиҰҒи®Ўз®—з»“жһңпјүпјҺ
в…ўпјҺKNO3 дёӯеҗ«е°‘йҮҸж°ҜеҢ–й’ ж—¶пјҢжҸҗзәҜзЎқй…ёй’ҫзҡ„дёҖиҲ¬ж–№жі•жҳҜ пјҺ
в…ЈпјҺж №жҚ®иЎЁеҶ…ж•°жҚ®еҸҜзҹҘпјҢKNO3е’ҢNaClеңЁжҹҗдёҖжё©еәҰж—¶е…·жңүзӣёеҗҢзҡ„жә¶и§ЈеәҰXпјҢеҲҷXзҡ„еҸ–еҖјиҢғеӣҙжҳҜгҖҖ пјҺ
-
пјҲ2пјү еҰӮеӣҫжҳҜеҜ№20в„ғдёҖе®ҡиҙЁйҮҸзҡ„з”Ізҡ„жә¶ж¶ІиҝӣиЎҢжҒ’жё©и’ёеҸ‘з»“жҷ¶зҡ„е®һйӘҢиҝҮзЁӢпјҢиҜ·еӣһзӯ”пјҺ

в… пјҺи’ёеҸ‘еүҚеҺҹжә¶ж¶ІжҳҜпјҲеЎ«вҖңйҘұе’ҢвҖқжҲ–вҖңдёҚйҘұе’ҢвҖқпјүжә¶ж¶ІпјҺnзҡ„ж•°еҖјжҳҜгҖҖ пјҺ
в…ЎпјҺдҫқжҚ®дёҠиҝ°е®һйӘҢпјҢдҪ и®Өдёәз”Ізҡ„жә¶и§ЈеәҰйҡҸжё©еәҰеҸҳеҢ–зҡ„и¶ӢеҠҝжҳҜ пјҲеЎ«еӯ—жҜҚпјүпјҺ
AпјҺйҡҸжё©еәҰеҚҮй«ҳиҖҢеўһеӨ§ BпјҺйҡҸжё©еәҰеҚҮй«ҳиҖҢеҮҸе°Ҹ CпјҺж— жі•еҲӨж–ӯпјҺ
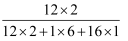 Г—100%
Г—100%
жё©еәҰ/в„ғ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | |
жә¶и§ЈеәҰ/g | NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 |
KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | |
-
пјҲ1пјү 10в„ғж—¶пјҢж°ҜеҢ–й’ зҡ„жә¶и§ЈеәҰжҳҜВ g
-
пјҲ2пјү зЎқй…ёй’ҫзҡ„жә¶и§ЈеәҰйҡҸжё©еәҰзҡ„еҚҮй«ҳиҖҢпјҢдёҺзЎқй…ёй’ҫзӣёжҜ”иҫғпјҢж°ҜеҢ–й’ зҡ„жә¶и§ЈеәҰеҸ—жё©еәҰеҸҳеҢ–еҪұе“ҚпјҲеЎ«вҖңиҫғеӨ§вҖңжҲ–вҖңиҫғе°ҸвҖңпјү
-
пјҲ3пјү 20в„ғж—¶пјҢеҗ‘100gж°ҙдёӯеҠ е…Ҙ40gзЎқй…ёй’ҫпјҢе……еҲҶжҗ…жӢҢеҗҺпјҢжүҖеҫ—жә¶ж¶ІжҳҜпјҲеЎ«вҖңйҘұе’Ңжә¶ж¶ІвҖқжҲ–вҖңдёҚйҘұе’Ңжә¶ж¶ІвҖқпјүпјҺ
-
пјҲ4пјү жҸҗзәҜж··жңүе°‘йҮҸж°ҜеҢ–й’ зҡ„зЎқй…ёй’ҫеӣәдҪ“пјҢжңҖеҘҪзҡ„ж–№жі•жҳҜпјҺ
 第дёҖз»„ |  第дәҢз»„ |  第дёүз»„ | ||||
е®һйӘҢжё©еәҰ | В 20в„ғ | 80в„ғ | 20в„ғ | 20в„ғ | В 20в„ғ | 20в„ғ |
В жә¶иҙЁз§Қзұ» | В еҶ°зі–зІүжң« | В еҶ°зі–зІүжң« | В еҶ°зі–зІүжң« | В еқ—зҠ¶зІүжң« | В еҶ°зі–зІүжң« | В йЈҹзӣҗзІүжң« |
В жә¶иҙЁиҙЁйҮҸ | В 10g | 10g | 10g | В 10g | В 10g | В 10g |
В жә¶еүӮз§Қзұ» | В ж°ҙ | жӨҚзү©жІ№ | ж°ҙ | ж°ҙ | ж°ҙ | ж°ҙ |
В жә¶еүӮиҙЁйҮҸ | В 10g | В 10g | 10g | В 10g | В 10g | В 10g |
иҜ·еӣһзӯ”дёӢеҲ—й—®йўҳпјҺ
-
пјҲ1пјү иҜҘе®һйӘҢдёӯжүҖз ”з©¶зҡ„вҖңеҪұе“Қзү©иҙЁжә¶и§ЈжҖ§зҡ„еӣ зҙ вҖқеҢ…жӢ¬пјҡгҖҒгҖҒгҖҒпјҢе…¶дёӯдёҚдјҡеҪұе“Қзү©иҙЁжә¶и§ЈжҖ§зҡ„еӣ зҙ жҳҜпјҺ
-
пјҲ2пјү иҜҘе®һйӘҢжүҖйҮҮз”Ёзҡ„з ”з©¶ж–№жі•жҳҜпјҢе…¶дёӯ第组е®һйӘҢи®ҫи®ЎдёҚеҗҲзҗҶпјҢзҗҶз”ұжҳҜпјҢиӢҘе°ҶиҜҘи®ҫи®Ўдёӯзҡ„ж”№дёәеҗҺеҶҚиҝӣиЎҢе®һйӘҢпјҢеҸҜеҫ—еҮәзҡ„з»“и®әжҳҜпјҺ
-
пјҲ3пјү и§ӮеҜҹ第дёүз»„е®һйӘҢеҸ‘зҺ°пјҡеҶ°зі–е…ЁйғЁжә¶и§ЈпјҢйЈҹзӣҗжңүйғЁеҲҶеү©дҪҷпјҢз”ұжӯӨеҸҜеҫ—еҮәзҡ„з»“и®әжҳҜпјҺ
-
пјҲ1пјү йұјиҷҫжҳҜдәә们е–ңзҲұзҡ„йЈҹзү©пјҢе®ғ们еҗ«жңүдё°еҜҢзҡ„пјҺпјҲйҖүеЎ«вҖңиӣӢзҷҪиҙЁвҖқгҖҒвҖңзі–зұ»вҖқгҖҒвҖңжІ№и„ӮвҖқжҲ–вҖңз»ҙз”ҹзҙ вҖқпјү
-
пјҲ2пјү й—·зғӯзҡ„еӨ©ж°”пјҢжұ еЎҳйҮҢзҡ„йұјиҷҫеӣ зјәж°§иҖҢжҺҘиҝ‘ж°ҙйқўжёёеҠЁпјҢи§ЈйҮҠе…¶зјәж°§зҡ„еҺҹеӣ 并жҸҗеҮәдёҖжқЎж”№е–„йұјиҷҫзјәж°§зҡ„еҗҲзҗҶеҒҡжі•пјҺ
-
пјҲ3пјү дёәдәҶи§Јжұ еЎҳдёӯж°ҙзҡ„й…ёзўұеәҰжҳҜеҗҰйҖӮеҗҲйұјиҷҫз”ҹй•ҝпјҢйңҖжөӢе®ҡжұ еЎҳдёӯж°ҙзҡ„pHпјҺиҜ·з®Җиҝ°е®һйӘҢж“ҚдҪңиҝҮзЁӢпјҺ
-
пјҲ4пјү жұ еЎҳдёӯж°ҙзҡ„й…ёжҖ§иҫғејәпјҢдёҚеҲ©дәҺйұјиҷҫзҡ„з”ҹй•ҝпјҢеңЁжҠ•ж”ҫйұјиҷҫиӢ—д№ӢеүҚпјҢиҜ·дҪ з»ҷе…»ж®–жҲ·жҸҗдёҖжқЎж”№иүҜж°ҙиҙЁй…ёжҖ§зҡ„е»әи®®пјҺ
-
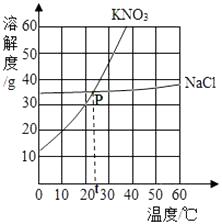
пјҲ1пјү PзӮ№иЎЁзӨәзҡ„еҗ«д№үжҳҜпјӣ
-
пјҲ2пјү 20в„ғж—¶еҗ‘50gж°ҙдёӯеҠ е…Ҙ25gзЎқй…ёй’ҫпјҢе……еҲҶжә¶и§ЈеҗҺжүҖеҫ—жә¶ж¶Ідёәжә¶ж¶І(еЎ«вҖңйҘұе’ҢвҖқжҲ–вҖңдёҚйҘұе’ҢвҖқ)пјӣиҜ·и®Ўз®—жӯӨж—¶жә¶ж¶Ізҡ„жә¶иҙЁзҡ„иҙЁйҮҸеҲҶж•°пјҢ(еҶҷеҮәи®Ўз®—иҝҮзЁӢпјҢз»“жһңдҝқз•ҷ1дҪҚе°Ҹж•°)пјӣ
-
пјҲ3пјү е°ҶйҘұе’Ңзҡ„KNO3жә¶ж¶ІеҖ’е…Ҙе°ҸиҜ•з®ЎдёӯпјҢ然еҗҺж”ҫе…Ҙзӣӣж°ҙзҡ„зғ§жқҜдёӯпјҢеҪ“еҗ‘ж°ҙдёӯеҠ е…Ҙжҹҗзү©иҙЁеҗҺпјҢиҜ•з®Ўдёӯжңүжҷ¶дҪ“жһҗеҮәпјҲеҰӮеӣҫпјүгҖӮеҠ е…Ҙзҡ„зү©иҙЁеҸҜиғҪжҳҜдёӢеҲ—дёӯзҡ„пјҲеЎ«еӯ—жҜҚеәҸеҸ·пјүгҖӮ
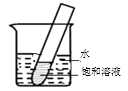
A.ж°ўж°§еҢ–й’ еӣәдҪ“ B.з”ҹзҹізҒ°еӣәдҪ“ C.еҶ°еқ—
D.зЎқй…ёй“өеӣәдҪ“ E.жө“зЎ«й…ё
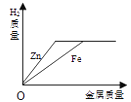 еҗ‘зӯүиҙЁйҮҸгҖҒзӯүжө“еәҰзҡ„зЁҖзЎ«й…ёдёӯеҲҶеҲ«еҠ е…ҘиҝҮйҮҸзҡ„Znе’ҢFe
B .
еҗ‘зӯүиҙЁйҮҸгҖҒзӯүжө“еәҰзҡ„зЁҖзЎ«й…ёдёӯеҲҶеҲ«еҠ е…ҘиҝҮйҮҸзҡ„Znе’ҢFe
B .  еҗ‘еҗ«жңүе°‘йҮҸNaOHзҡ„Na2CO3жә¶ж¶ІдёӯйҖҗж»ҙеҠ е…ҘзЁҖзӣҗй…ё
C .
еҗ‘еҗ«жңүе°‘йҮҸNaOHзҡ„Na2CO3жә¶ж¶ІдёӯйҖҗж»ҙеҠ е…ҘзЁҖзӣҗй…ё
C .  з”ЁзӯүиҙЁйҮҸгҖҒзӯүжө“еәҰзҡ„иҝҮж°§еҢ–ж°ўжә¶ж¶ІеңЁжңүгҖҒж— еӮ¬еҢ–еүӮжқЎд»¶дёӢеҲ¶еҸ–ж°§ж°”
D .
з”ЁзӯүиҙЁйҮҸгҖҒзӯүжө“еәҰзҡ„иҝҮж°§еҢ–ж°ўжә¶ж¶ІеңЁжңүгҖҒж— еӮ¬еҢ–еүӮжқЎд»¶дёӢеҲ¶еҸ–ж°§ж°”
D .  дёҖе®ҡжё©еәҰж—¶пјҢеҗ‘дёҖе®ҡйҮҸзҡ„йҘұе’ҢзҹізҒ°ж°ҙдёӯеҠ е…Ҙз”ҹзҹізҒ°
дёҖе®ҡжё©еәҰж—¶пјҢеҗ‘дёҖе®ҡйҮҸзҡ„йҘұе’ҢзҹізҒ°ж°ҙдёӯеҠ е…Ҙз”ҹзҹізҒ°
A.жҺўз©¶з©әж°”дёӯж°§ж°”зҡ„еҗ«йҮҸ | B. жҺўз©¶еҢ–еӯҰеҸҚеә”жҳҜеҗҰйҒөеҫӘиҙЁйҮҸе®ҲжҒ’е®ҡеҫӢ | C. жҺўз©¶еҸҜзҮғзү©зҮғзғ§жқЎд»¶ | D.жҺўз©¶еҪұе“Қзү©иҙЁжә¶и§ЈжҖ§зҡ„еӣ зҙ |
|
|
|
|

-
пјҲ1пјү йҡҸжё©еәҰеҚҮй«ҳпјҢжә¶и§ЈеәҰеҮҸе°Ҹзҡ„зү©иҙЁжҳҜгҖӮ
-
пјҲ2пјү з”Іе’Ңд№ҷзҡ„жә¶и§ЈеәҰзӣёеҗҢж—¶пјҢжё©еәҰжҳҜгҖӮ
-
пјҲ3пјү еҲҶеҲ«е°Ҷз”ІгҖҒд№ҷгҖҒдёҷдёүз§Қзү©иҙЁзҡ„йҘұе’Ңжә¶ж¶Ід»Һt2в„ғйҷҚеҲ°t2в„ғпјҢйҷҚжё©еҗҺз”ІгҖҒд№ҷгҖҒдёҷдёүз§Қжә¶ж¶Ізҡ„жә¶иҙЁиҙЁйҮҸеҲҶж•°з”ұеӨ§еҲ°е°Ҹзҡ„йЎәеәҸжҳҜгҖӮ
-
пјҲ4пјү е°Ҷ150gз”Ізҡ„йҘұе’Ңжә¶ж¶Ід»Һt3в„ғйҷҚеҲ°t2в„ғеҗҺпјҢеҗ‘е…¶дёӯеҠ е…Ҙ50gж°ҙпјҢжӯӨж—¶жүҖеҫ—жә¶ж¶Ізҡ„жә¶иҙЁиҙЁйҮҸеҲҶж•°жҳҜпјҲи®Ўз®—з»“жһңзІҫзЎ®еҲ°0.1%пјүгҖӮ


-
пјҲ1пјү дёҷзү©иҙЁзҡ„жә¶и§ЈеәҰйҡҸжё©еәҰзҡ„еҚҮй«ҳиҖҢ(еЎ«вҖңеўһеӨ§вҖқжҲ–вҖңеҮҸе°ҸвҖқ)пјҺ
-
пјҲ2пјү иӢҘиҰҒд»Һд№ҷзү©иҙЁзҡ„йҘұе’Ңжә¶ж¶Ідёӯеҫ—еҲ°д№ҷеӣәдҪ“пјҢеҸҜз”Ёз»“жҷ¶ж–№жі•пјҺ
-
пјҲ3пјү t1в„ғж—¶пјҢе°Ҷз”Ізү©иҙЁзҡ„йҘұе’Ңжә¶ж¶ІеҚҮжё©еҲ°t3в„ғжүҖеҫ—жә¶ж¶Ідёӯжә¶иҙЁзҡ„иҙЁйҮҸеҲҶж•°(еЎ«вҖңеҸҳеӨ§вҖқгҖҒвҖңеҸҳе°ҸвҖқжҲ–вҖңдёҚеҸҳвҖқ)пјҺ
-
пјҲ4пјү t2в„ғе°Ҷ100gж°ҙеҠ е…ҘеҲ°зӣӣжңү30gз”Ізү©иҙЁзҡ„зғ§жқҜдёӯпјҢе……еҲҶжә¶и§ЈеҗҺеҫ—еҲ°дёҚйҘұе’Ңжә¶ж¶ІпјҢиӢҘжғідҪҝжә¶ж¶ІжҒ°еҘҪйҘұе’ҢпјҢеҸҜйҮҮз”Ёзҡ„ж–№жі•жҳҜпјҡпјҺ
-
пјҲ5пјү t3в„ғж—¶пјҢз”ІгҖҒд№ҷгҖҒдёҷдёүз§Қзү©иҙЁзҡ„жә¶и§ЈеәҰзҡ„з”ұеӨ§еҲ°е°Ҹзҡ„йЎәеәҸжҳҜпјҺ
 ж°”дҪ“зү©иҙЁзҡ„жә¶и§ЈеәҰдёҺжё©еәҰе’ҢеҺӢејәзҡ„е…ізі»
B .
ж°”дҪ“зү©иҙЁзҡ„жә¶и§ЈеәҰдёҺжё©еәҰе’ҢеҺӢејәзҡ„е…ізі»
B .  еҗ‘зӯүиҙЁйҮҸзҡ„ж°§еҢ–й”Ңе’Ңж°ўж°§еҢ–й”ҢдёӯеҲҶеҲ«еҠ е…ҘзӣёеҗҢжө“еәҰзҡ„зЁҖзӣҗй…ёиҮіиҝҮйҮҸ
C .
еҗ‘зӯүиҙЁйҮҸзҡ„ж°§еҢ–й”Ңе’Ңж°ўж°§еҢ–й”ҢдёӯеҲҶеҲ«еҠ е…ҘзӣёеҗҢжө“еәҰзҡ„зЁҖзӣҗй…ёиҮіиҝҮйҮҸ
C .  еҠ зғӯдёҖе®ҡиҙЁйҮҸзҡ„ж°Ҝй…ёй’ҫе’ҢдәҢж°§еҢ–й”°зҡ„ж··еҗҲзү©
D .
еҠ зғӯдёҖе®ҡиҙЁйҮҸзҡ„ж°Ҝй…ёй’ҫе’ҢдәҢж°§еҢ–й”°зҡ„ж··еҗҲзү©
D .  еҗ‘дёҖе®ҡйҮҸзҡ„зӣҗй…ёе’ҢзЎ«й…ёй’ҫж··еҗҲжә¶ж¶ІдёӯдёҚж–ӯж»ҙеҠ ж°ўж°§еҢ–й’Ўжә¶ж¶І
еҗ‘дёҖе®ҡйҮҸзҡ„зӣҗй…ёе’ҢзЎ«й…ёй’ҫж··еҗҲжә¶ж¶ІдёӯдёҚж–ӯж»ҙеҠ ж°ўж°§еҢ–й’Ўжә¶ж¶І
| жё©еәҰв„ғ | t1 | t2 |
| KNO3зҡ„жә¶и§ЈеәҰпјҲg/100gж°ҙпјү | 60 | 90 |
в‘ дәәдҪ“жүҖйңҖзҡ„еҫ®йҮҸе…ғзҙ еҢ…жӢ¬й’ҷгҖҒй“ҒгҖҒй”ҢгҖҒзЎ’зӯү
в‘Ўе–қе…ҘеӨ§йҮҸеҸҜд№җеҗҺдјҡжү“е—қпјҢиҜҙжҳҺж°”дҪ“зҡ„жә¶и§ЈеәҰйҡҸеҺӢејәзҡ„еҮҸе°ҸиҖҢеҮҸе°Ҹ
в‘ўж°ҜеҢ–й’ гҖҒзўій…ёй’ҷзӯүзӣҗдёӯйғҪеҗ«йҮ‘еұһе…ғзҙ пјҢжүҖд»ҘзӣҗдёӯдёҖе®ҡйғҪеҗ«йҮ‘еұһе…ғзҙ
в‘ЈжҹҗеҗҢеӯҰеҗ‘жҹҗж— иүІжә¶ж¶Ідёӯж»ҙе…ҘдәҶеҮ ж»ҙй…ҡй…һпјҢжә¶ж¶ІжҳҫзәўиүІпјҢеҲҷиҜҘжә¶ж¶ІдёҖе®ҡдёәзўұгҖӮ
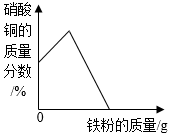
в‘Өеҗ‘дёҖе®ҡйҮҸзҡ„зЎқ酸银е’ҢзЎқй…ёй“ңзҡ„ж··еҗҲжә¶ж¶ІдёӯеҠ е…Ҙй“ҒзІүиҮіиҝҮйҮҸпјҡеҠ е…Ҙй“ҒзІүиҙЁйҮҸдёҺзЎқй…ёй“ңзҡ„иҙЁйҮҸеҲҶж•°е…ізі»еҰӮеӣҫпјҡ
-
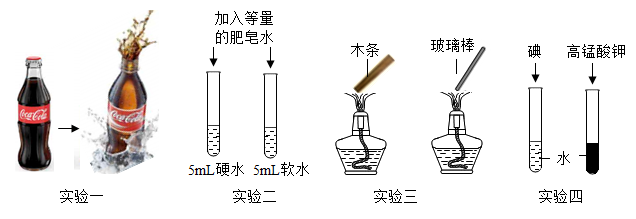
пјҲ1пјү е®һйӘҢдёҖдёӯејҖеҸҜд№җзҡ„瓶зӣ–пјҢи§ӮеҜҹеҲ°еӨ§йҮҸж°”жіЎеҶ’еҮәпјҢиҜҙжҳҺж°”дҪ“зҡ„жә¶и§ЈеәҰдёҺжңүе…ігҖӮ
-
пјҲ2пјү е®һйӘҢдәҢдёӯдә§з”ҹжө®жёЈжӣҙеӨҡзҡ„жҳҜпјҲеЎ«вҖңзЎ¬ж°ҙвҖқжҲ–вҖңиҪҜж°ҙвҖқпјүгҖӮ
-
пјҲ3пјү е®һйӘҢдёүдёӯи§ӮеҜҹеҲ°жңЁжқЎзҮғзғ§пјҢзҺ»з’ғжЈ’дёҚзҮғзғ§пјҢиҜҙжҳҺзҮғзғ§еә”е…·еӨҮзҡ„жқЎд»¶жҳҜгҖӮ
-
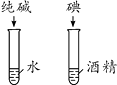
пјҲ4пјү е®һйӘҢеӣӣдёӯи§ӮеҜҹеҲ°й«ҳй”°й…ёй’ҫжә¶дәҺж°ҙеҪўжҲҗзҙ«зәўиүІжә¶ж¶ІпјҢиҖҢзўҳеҮ д№ҺдёҚжә¶дәҺж°ҙпјҢиҜҙжҳҺзү©иҙЁзҡ„жә¶и§ЈжҖ§дёҺжңүе…ігҖӮ