除杂 知识点题库
材料一
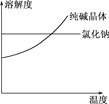
材料二
物质 | 熔点/℃ | 沸点/℃ | 密度/g·cm-3 | 溶解性 |
乙二醇 | -11.5 | 198 | 1.11 | 易溶于水和乙醇 |
丙三醇 | 17.9 | 290 | 1.26 | 能跟水、酒精以任意比互溶 |
回答下列问题(填写序号):
A.蒸馏法
B.萃取法
C.“溶解、结晶、过滤”的方法
D.分液法
-
(1) 将纯碱从氯化钠和纯碱的混合物中分离出来,最好应用.
-
(2) 将乙二醇和丙三醇相互分离的最佳方法是.
实验 | 除杂试剂 | 实验目的 | |
① | 电石与水反应 | CuSO4溶液 | 用KMnO4酸性溶液检验乙炔的还原性 |
② | CH3CH2Br与NaOH溶液共热 | HNO3溶液 | 用AgNO3溶液检验CH3CH2Br中的Br |
③ | 淀粉与稀H2SO4水浴共热 | NaOH溶液 | 用银氨溶液检验水解产物的还原性 |
④ | C2H5OH与浓H2SO4加热至170℃ | NaOH溶液 | 用Br2的CCl4溶液证明该反应为消去反应 |
 等离子,可以通过化学沉淀法除去.如:可以通过加入Ba(NO3)2的方法除去其中的SO
等离子,可以通过化学沉淀法除去.如:可以通过加入Ba(NO3)2的方法除去其中的SO  D . 从海带中提取碘单质时,可以将其灼烧后加水溶解过滤,在滤液中加适量氯水将碘元素氧化为I2 , 最后用乙醇萃取出单质碘
D . 从海带中提取碘单质时,可以将其灼烧后加水溶解过滤,在滤液中加适量氯水将碘元素氧化为I2 , 最后用乙醇萃取出单质碘
-
(1) 除去该混合物中的碳酸氢钠可采取的方法是.
-
(2) 若将该混合物加热至质量不再变化时,剩余固体质量为2.62g.计算原混合物中碳酸钠的质量分数.
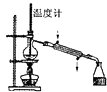 制蒸馏水
C .
制蒸馏水
C . 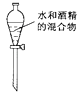 分离水和酒精
D .
分离水和酒精
D . 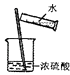 稀释浓硫酸
稀释浓硫酸
![]()
-
(1) 判断BaCl2已过量的方法是。
-
(2) 第⑥步中,相关的离子方程式是。
-
(3) 为检验精盐纯度,需配制230mL0.2mol/L NaCl(精盐)溶液,则需用托盘天平称取精盐固体的质量为,需要的玻璃仪器有量筒、 。
-
(4) 配制NaCl(精盐)溶液时,若出现下列操作,造成结果偏低的是。
A.称量时NaCl已潮解 B.天平的砝码已锈蚀
C.定容摇匀时,液面下降又加水 D.定容时仰视刻度线
选项 | A | B | C | D |
实验 目的 | 鉴别盐酸、NaCl溶液、Ca(OH)2溶液 | 鉴别CaCO3和K2CO3粉末 | 除去氯化钠溶液中的少量盐酸 | 除去CaO中的少量CaCO3 |
方案1 | 滴加碳酸钠溶液 | 滴加盐酸 | 滴加适量Na2CO3溶液 | 加足量的水 |
方案2 | 分别测定溶液的pH | 加水 | 滴加适量Ca(OH)2溶液 | 滴加适量盐酸 |
| 选项 | 目的 | 实验 |
| A | 制取较高浓度的次氯酸溶液 | 将Cl2通入碳酸钠溶液中 |
| B | 加快氧气的生成速率 | 在过氧化氢溶液中加入少量MnO2 |
| C | 除去乙酸乙酯中的少量乙酸 | 加入饱和碳酸钠溶液洗涤、分液 |
| D | 制备少量二氧化硫气体 | 向饱和亚硫酸钠溶液中滴加浓硫酸 |
| 选项 | 物质 | 使用的试剂 | 主要操作 |
| A | 乙醇(水) | 金属钠 | 蒸馏 |
| B | 乙酸乙酯(乙酸) | 饱和碳酸钠溶液 | 分液 |
| C | FeCl2(FeCl3)溶液 | 过量铜粉 | 过滤 |
| D | 乙烯(SO2) | 酸性高锰酸钾溶液 | 洗气 |
-
(1) Fe粉(Al粉):试剂离子方程式;
-
(2) FeCl2溶液(FeCl3):试剂离子方程式;
-
(3) Na2CO3固体(NaHCO3):化学方程式。
![]() +HNO3
+HNO3 
![]() +H2O
+H2O
![]() +3H2
+3H2 
![]() +2H2O
+2H2O
| 物质 | 沸点/℃ | 密度/(g*cm3) | 部分性质 |
| 苯 | 80 | 0.88 | 无色油状液体,难溶于水 |
| 硝基苯 | 210.9 | 1.23 | 无色或淡黄色油状液体,不溶于水,易溶于乙醇、乙醚 |
| 苯胺 | 184.4. | 1.02 | 无色油状液体,微溶于水,易溶于乙醇、乙醚:还原性强,易被氧化 |
实验步骤:
-
(1) I.制取硝基苯
实验室采用如图所示装置制取硝基苯,A中装有一定量的苯,三颈烧瓶装有一定比例的浓硫酸和浓硝酸混合物。请回答下列问题:
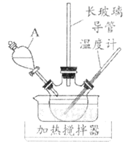
仪器A的名称是。
-
(2) 配制浓硫酸和浓硝酸的混合物时,应将逐滴加入到中,并及时搅拌和冷却。
-
(3) 实验装置中长玻璃导管的作用是。
-
(4) 粗硝基苯用5% NaOH溶液洗涤的目的是。
-
(5) II.制取苯胺
①组装好实验装置(如图,夹持仪器已略去),并检查气密性。②先向三颈烧瓶中加入沸石及硝基苯,再取下恒压分液漏斗,换上温度计。③打开活塞K,通入H2一段时间。④利用油浴加热,使反应液温度维持在140℃进行反应。⑤反应结束后,关闭活塞K,向三颈烧瓶中加入生石灰。⑥调整好温度计的位置,继续加热,收集182~186℃馏分,得到较纯苯胺。

回答下列问题:
操作①中加入沸石的作用,冷凝装置中的冷凝水应该从(填“a”或者“b”)口进入。
-
(6) 若实验中步骤③和④的顺序颠倒,则实验中可能产生的不良后果是。
-
(7) 蒸馏前,步骤⑤中加入生石灰的作用是。
-
(8) 若实验中硝基苯用量为5 mL,最后得到苯胺2.79 g,苯胺的产率为。
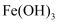 胶体在生活中有重要应用,利用
胶体在生活中有重要应用,利用  和沸水反应制备的
和沸水反应制备的 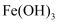 胶体中常混有
胶体中常混有  和HCl。已知胶体不能透过半透膜,而小分子和离子可以透过半透膜。试回答下列有关问题:
和HCl。已知胶体不能透过半透膜,而小分子和离子可以透过半透膜。试回答下列有关问题:
-
(1) 制取
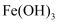 胶体的实验操作是。用的方法除去胶体中的浑浊物;用(填方法或现象)证明胶体已经制成。
胶体的实验操作是。用的方法除去胶体中的浑浊物;用(填方法或现象)证明胶体已经制成。
-
(2)
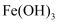 胶体区别于
胶体区别于  溶液的本质特征是。
溶液的本质特征是。
-
(3) 除去胶体中混有的
 和HCl的实验操作名称是。
和HCl的实验操作名称是。
-
(4) 取半透膜外最后一次的溶液少许于试管中,,则证明胶体和
 已经完全分离。
已经完全分离。

-
(1) “沉淀1”的化学式是,“碱溶”后溶液的pH=12,“沉淀1”中不含Ca(OH)2则溶液中的c(CO
 )>mol•L-1。(Ksp(Ca(OH)2=6×10-6 , Ksp(CaCO3)=3×10-9)
)>mol•L-1。(Ksp(Ca(OH)2=6×10-6 , Ksp(CaCO3)=3×10-9)
-
(2) “沉降”时温度控制在40℃左右,主要原因是,“沉降”的离子方程式是。
-
(3) “洗涤”的目的是,实验室检验该洗涤已干净的操作是。
-
(4) 若要使聚合氧化[Al2(OH)aCl6-a]n中a=3,“酸化”时除控制温度外,理论上还需控制投料比n[Al(OH)3:n(HCl)=,为了达到上述目的,实际生产中可以采用控制的条件是。
序号 | 物质 | 杂质 | 试剂 | 方法 |
A |
|
|
| 蒸馏 |
B |
|
|
| 加热 |
C |
|
| NaOH溶液 | 洗气 |
D |
|
| 饱和 | 洗气 |


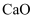


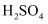



 溶液
溶液


