铁的化学性质 知识点题库
类比推理是化学中常用的思维方法.下列推理正确的是( )
A . CO2是直线型分子,推测CS2也是直线型分子
B . SiH4的沸点高于CH4 , 推测H2Se的沸点高于H2S
C . Fe与Cl2反应生成FeCl3 , 推测Fe与I2反应生成FeI3
D . NaCl与浓H2SO4加热可制HCl,推测NaBr与浓H2SO4加热可制HBr
将铁屑溶于过量的稀盐酸后,再加入下列物质,会有Fe3+生成的是( )
A . 溴水
B . 硫酸锌
C . 硝酸钠
D . 氯化铜
下列物质不能通过化合反应得到的物质是( )
A . CuCl2
B . FeCl2
C . FeS
D . CuS
下列反应中,最终能生成+3价铁的化合物的是( )
①铁粉和稀盐酸②过量铁和稀硝酸③过量铁和FeCl3④氯水和FeCl2⑤FeO和稀硝酸⑥铁粉和足量稀硝酸 ⑦铁片投入CuSO4溶液⑧铁在Cl2中燃烧.
A . ②③④⑥
B . ④⑤⑥⑧
C . ③④⑥⑧
D . ②③⑤⑥
下列物质间的转化,能经过一步化合反应直接转化的是( )
A . SiO2→H2SiO3
B . Na2O2→Na2CO3
C . Fe→Fe(OH)3
D . Al2O3→Al(OH)3
下列反应中,不能产生氢气的是( )
A . 红热的铁与水蒸气
B . 钠与水
C . 铝和NaOH溶液反应
D . 铁与稀硝酸反应
铝和铁是生活中非常常见的金属,运用所学知识回答:
-
(1) 金属铝是活泼的金属,但在生活中的应用仍很广泛,原因是.
-
(2) 在一个瘪了的铝制易拉罐加入适量的NaOH溶液,并密封,易拉罐会慢慢复原,原因是(用化学方程式表示).
-
(3) 写出还原铁粉与水蒸气反应的化学方程式.
下列实验现象描述正确的是( )
A . 二氧化碳气体通入无色酚酞溶液,溶液变红色
B . 细铁丝在氧气里剧烈燃烧,火星四射
C . 点燃棉线闻到一股烧焦的羽毛味
D . 打开浓盐酸试剂瓶的瓶塞,瓶口上方出现大量白烟
现向一支装有FeCl2溶液的试管中滴加氢氧化钠溶液,可观察到的现象是,有关的化学方程为.
下列有关铁及其化合物的说法中正确的是( )
A . 赤铁矿的主要成分是Fe3O4
B . 铁与水蒸气在高温下的反应产物为Fe2O3和H2
C . 除去FeCl2溶液中的FeCl3杂质可以向溶液中加入铁粉,然后过滤
D . Fe3+与KSCN产生血红色沉淀
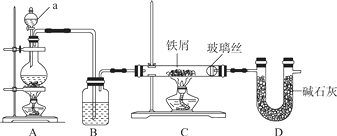
工业上,向500℃左右的铁屑中通入Cl2生产无水氯化铁,其制备过程中均要确保无水。现模拟该过程用图示装置进行实验:
-
(1) 仪器a的名称为,装置A的圆底烧瓶中发生反应的化学方程式为,为保持装置C为无水环境,装置B中加入的试剂是。
-
(2) 实验步骤:如图连接装置后,先(填实验操作),再装药品,然后点燃(填“A”或“C”)处酒精灯,当(填实验现象)时,再点燃(填“A”或“C”)处酒精灯。
-
(3) 装置D的作用是,。
-
(4) 甲同学认为进入装置C的气体中混有HCl,应在装置B前增加装有(填试剂名称)的洗气装置除去;乙同学认为不需要除去HCl,理由为。
推理是化学学习中常用的思维方法,下列推理正确的是( )
A . 在同一化合物中,金属元素显正价,所以非金属元素一定显负价
B . 混合物都不是电解质,所以冰水混合物也不是电解质
C . 通入CO2后的紫色石蕊溶液变红,所以CO2是酸
D . Cu2+的氧化性比H+强,所以CuCl2和稀盐酸的混合溶液中加入少量铁屑时,可能没有气泡冒出。
在给定条件下,下列选项所示的物质间转化均能实现的是( )
A . Fe  FeCl2
FeCl2  Fe(OH)2
B . S
Fe(OH)2
B . S  SO3
SO3  H2SO4
C . CaCO3
H2SO4
C . CaCO3  CaO
CaO  CaSiO3
D . NH3
CaSiO3
D . NH3 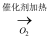 NO
NO  HNO3
HNO3
 FeCl2
FeCl2  Fe(OH)2
B . S
Fe(OH)2
B . S  SO3
SO3  H2SO4
C . CaCO3
H2SO4
C . CaCO3  CaO
CaO  CaSiO3
D . NH3
CaSiO3
D . NH3 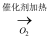 NO
NO  HNO3
HNO3
用如图所示装置进行Fe与水蒸气反应的实验,下列有关说法正确的是( )
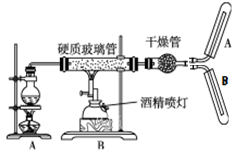
A . 实验时,先点燃酒精喷灯再点燃酒精灯
B . 装置B中H2O作氧化剂,发生的化学方程式为 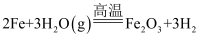 C . 干燥管中加入的固体干燥剂可以是无水硫酸铜
D . 收集反应产生的气体选用装置A
C . 干燥管中加入的固体干燥剂可以是无水硫酸铜
D . 收集反应产生的气体选用装置A
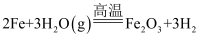 C . 干燥管中加入的固体干燥剂可以是无水硫酸铜
D . 收集反应产生的气体选用装置A
C . 干燥管中加入的固体干燥剂可以是无水硫酸铜
D . 收集反应产生的气体选用装置A
某稀硫酸和稀硝酸的混合溶液200 mL,平均分成两份。向其中一份中逐渐加入铜粉,最多能溶解19.2 g(已知硝酸只被还原为NO气体)。向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示。下列分析或结果错误的是( )

A . 混合酸中HNO3物质的量浓度为2 mol/L
B . OA段产生的是NO,BC段产生氢气
C . 第二份溶液中最终溶质为FeSO4
D . 原混合酸中H2SO4物质的量为0.4 mol
铁是当前应用量最大的金属元素。下列说法错误的是( )
A . 生铁与普通钢都是以铁为主的含碳合金
B . 与铜质水龙头连接处的铁水管不容易发生腐蚀
C . 红色涂料中的“铁红”,其主要化学成分是  D . 食用富含维生素C的食物有助于人体对铁元素的吸收
D . 食用富含维生素C的食物有助于人体对铁元素的吸收
 D . 食用富含维生素C的食物有助于人体对铁元素的吸收
D . 食用富含维生素C的食物有助于人体对铁元素的吸收
用如图所示装置进行Fe与水蒸气反应的实验,下列有关说法正确的是( )
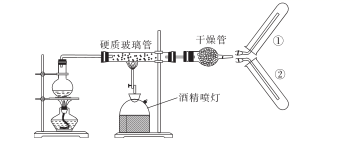
A . 实验时,先点燃酒精喷灯再点燃酒精灯
B . 反应中H2O作氧化剂,发生反应的化学方程式为 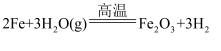 C . 干燥管中加入的固体干燥剂可以是无水氯化钙
D . 收集反应产生的气体选用装置②
C . 干燥管中加入的固体干燥剂可以是无水氯化钙
D . 收集反应产生的气体选用装置②
 C . 干燥管中加入的固体干燥剂可以是无水氯化钙
D . 收集反应产生的气体选用装置②
C . 干燥管中加入的固体干燥剂可以是无水氯化钙
D . 收集反应产生的气体选用装置②
铁及其化合物在生活中的应用广泛,其中氯化铁主要用于金属蚀刻、污水处理。
-
(1) I.以废铁屑(Fe和Fe2O3的混合物)为原料获得FeCl3的流程如图。

电解氯化钠水溶液的离子方程式为。 -
(2) Y在Z中燃烧得到W,反应现象是;W溶液“溶解废铁屑”时,氧化铁溶解的离子方程式为。
-
(3) “氧化”时发生反应的离子方程式为;若“氧化”时由电解
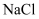 水溶液得到的Z恰好完全反应,得到
水溶液得到的Z恰好完全反应,得到 , 则发生电解的
, 则发生电解的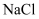 的物质的量为(用含a的代数式表示)
的物质的量为(用含a的代数式表示) 。
。
-
(4) II.电子工业常用
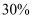 的
的 溶液作为腐蚀液覆在绝缘板的铜箔上,制造印刷电路板。
溶液作为腐蚀液覆在绝缘板的铜箔上,制造印刷电路板。
某化学兴趣小组测得含有
 的腐蚀废液中
的腐蚀废液中 的物质的量之比为
的物质的量之比为 , 向其中加入适量铁粉,充分反应后,测得溶液中
, 向其中加入适量铁粉,充分反应后,测得溶液中 的物质的量之比变为
的物质的量之比变为 。则参加反应的铁粉与原溶液中
。则参加反应的铁粉与原溶液中 的物质的量之比为。
的物质的量之比为。
贫血是一种常见的疾病,其中缺铁性贫血是贫血中最常见的类型,通常补铁剂会与维生素C同服。下列有关叙述中错误的是( )
A . 补铁剂中的铁以Fe3+形式存在
B . 铁是人体必需的微量元素
C . 补铁剂搭配的维生素C具有还原性
D . Fe2+具有还原性,能被氧化成Fe3+
某研究性学习小组利用如图所示的装置制备无水氯化铁。

-
(1) 装置Ⅰ中仪器A的名称是,写出装置Ⅰ中制备氯气的离子方程式。
-
(2) 装置Ⅱ的作用是,装置Ⅲ的溶液是。
-
(3) 写出在装置Ⅳ中发生的反应的化学方程式。
-
(4) 实验结束后将装置Ⅳ中的固体加水溶解并过滤,往滤液中滴加KSCN溶液,观察到,即可证明滤液中含有
 。
。
-
(5) 另一组同学发现,在装置Ⅳ和装置Ⅴ之间还需要增加一个装置才能制得无水氯化铁。为了达到这一实验目的,你认为还需在装置Ⅳ和装置Ⅴ之间添加下图中的装置(填序号)。

最近更新



