铁的氧化物和氢氧化物 知识点题库
铁及其化合物在生活、生产中有广泛应用.请回答下列问题:
(1)黄铁矿(FeS2)是生产硫酸和冶炼钢铁的重要原料.其中一个反应为3FeS2+8O2 6SO2+Fe3O4 , 氧化产物为 ,若有3mol FeS2参加反应,转移 mol电子.
6SO2+Fe3O4 , 氧化产物为 ,若有3mol FeS2参加反应,转移 mol电子.
(2)与明矾相似,硫酸铁也可用作净水剂,其原理为 (用离子方程表示)
(3)FeCl3与氢碘酸反应时可生成棕色物质,该反应的离子方程式为 .
(4)在热的稀硫酸溶液中溶解一定量的FeSO4后,再加入足量的KNO3溶液,可使其中的Fe2+全部转化成Fe3+ , 并有气体逸出,请配平该化学方程式:
FeSO4+ KNO3+ H2SO4═ K2SO4+ Fe2(SO4)3+ NO↑+ H2O;其中氧化剂为 .
(5)铁红是一种红色颜料,其成分是Fe2O3将一定量的铁红溶于160mL 5mol•L﹣1盐酸中,在加入一定量铁粉恰好溶解,收集到2.24L(标准状况),经检测,溶夜中无Fe3+ , 则参加反应的铁粉的质量为 g .
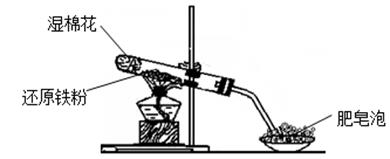
回答下列问题:
-
(1) 硬质试管中发生反应的化学方程式为 ;
-
(2) 该同学欲确定反应后硬质试管中固体物质的成分,设计了如下实验方案:
①待硬质试管冷却后,取少许其中的固体物质溶于稀硫酸得溶液B;
②取少量溶液B滴加KSCN溶液,若溶液变红色则说明硬质试管中固体物质的成分一定有,若溶液未变红色则说明硬质试管中固体物质的成分一定有;原因是:(用离子方程式表示);
-
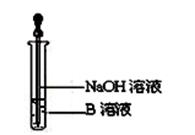
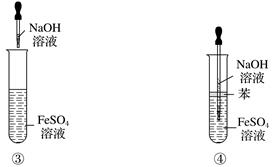
(3) 发现溶液未变红该同学马上另取少量溶液B,使其跟NaOH溶液反应。若按下图所示的操作,可观察到生成白色沉淀,迅速变成灰绿色,最后变成红褐色的现象,请写出与沉淀发生变化现象的反应的化学方程式:;
-
(4) 一段时间后,该同学发现(2)中未变红的溶液变成红色,说明Fe2+ 具有性;由此可知,实验室中FeSO4溶液要临时配制并加少量。

 C . “自古书契多编以竹简,其用缣帛(丝织品)者谓之为纸”,文中“纸”的主要成分为蛋白质
D . “司南之杓(勺),投之于地,其柢(勺柄)指南”中的“杓”含
C . “自古书契多编以竹简,其用缣帛(丝织品)者谓之为纸”,文中“纸”的主要成分为蛋白质
D . “司南之杓(勺),投之于地,其柢(勺柄)指南”中的“杓”含 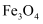

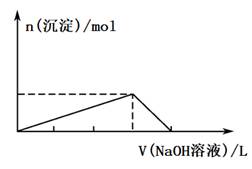
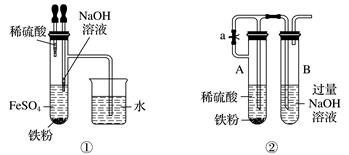
回答下列问题:
-
(1) 已知气体A能使品红溶液褪色,则反应①的离子方程式为。
-
(2) 溶液F中溶质的化学式为,为检验该溶液中的金属阳离子,可向溶液
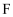 中滴加溶液,预计观察的现象为。
中滴加溶液,预计观察的现象为。
-
(3) 固体B是由两种金属氧化物-CuO和(填化学式)组成的混合物,其中CuO与另一金属氧化物的物质的量之比为。
-
(4) X在足量空气中充分灼烧的化学方程式为。
-
(1) 下列变化中,与氧化还原反应有关的是(填字母)。
a.食物的腐败 b.钢铁的锈蚀 c.钟乳石的形成 d.燃料的燃烧
-
(2) 汽车尾气中的CO和NO在催化剂作用下发生反应,生成CO2和N2。写出化学方程式:。
-
(3) FeSO4、K2FeO4是水处理中常用的物质。
①选择两种属于不同基本反应类型的方法制取FeSO4 , 用离子方程式表示该方法:、。
②依据“性质决定用途”的学科观念,分析K2FeO4的性质,预测K2FeO4在处理含
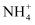 的废水中的作用。简述分析过程:。
的废水中的作用。简述分析过程:。
选项 | 操作或现象 | 解释 |
A | 节日燃放的烟花五彩缤纷 | 活泼金属单质易燃且火焰颜色各异 |
B | 食品包装袋中装有“脱氧剂” | “脱氧剂”为CaO,CaO能吸收 |
C | 广东韶关境内的丹霞山岩石呈红色 | 岩石中含 |
D | 漂白液与含盐酸的洁厕剂不能混合使用 | 两者混合产生沉淀,影响使用效果 |

 ,
, 


