铁的氧化物和氢氧化物 知识点题库
下列物质与其用途完全符合的有多少条( )
①Si﹣光导纤维 ②Na2CO3﹣制玻璃 ③Fe2O3﹣红色油漆或涂料 ④MgO﹣耐火材料 ⑤NaClO﹣消毒剂 ⑥NaCl﹣制纯碱 ⑦SO2﹣食品漂白剂 ⑧Al2O3﹣焊接钢轨 ⑨NH3﹣制冷剂.⑩AgI﹣人工降雨.
A . 6
B . 7
C . 5
D . 4
下列有关物质应用的说法不正确的是( )
A . 氧化铁可用来制造红色油漆和涂料
B . 生铁、普通钢和不锈钢中的含碳量依次减小
C . 硅胶可用作实验室和袋装食品、瓶装药品等的干燥剂
D . 硅是生产光纤制品的基本原料
下列物质的转化在给定条件下能实现的是( )
①NaAlO2(aq)  Al(OH)3
Al(OH)3 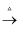 Al2O3(熔融)
Al2O3(熔融)  Al
Al  Fe
Fe
②S  SO3
SO3  H2SO4
H2SO4
③Cu(OH)2CO3  CuCl2(aq)
CuCl2(aq)  Cu
Cu
④Fe2O3  FeCl3
FeCl3 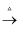 无水FeCl3
无水FeCl3
⑤饱和NaCl(aq)  NaHCO3
NaHCO3 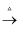 Na2CO3 .
Na2CO3 .
A . ①③⑤
B . ②③④
C . ②④⑤
D . ①④⑤
将铝粉与某铁的氧化物FeO•2Fe2O3粉末配制成铝热剂,分成两等份.一份直接放入足量的烧碱溶液中,充分反应后放出气体在标准状况下的体积为15.68L;另一份在高温下恰好反应完全,反应后的混合物与足量的盐酸反应后,放出的气体在标准状况下的体积为( )
A . 11.20L
B . 15.68L
C . 22.40L
D . 31.36L
为了探究铁及其化合物的氧化性或还原性,某同学设计如下实验方案,其中符合实验
要求且完全正确的是( )
选项 | 实验操作 | 实验现象 | 实验结论 | 离子反应 |
A | 向FeCl2溶液中加入Zn片 | 浅绿色溶液变为无色 | Zn具有还原性 | Fe2++Zn═Zn2++Fe |
B | 向FeCl2溶液中滴新制氯水 | 浅绿色溶液变为棕黄色 | Fe2+具有还原性 | 2Fe2++Cl2═2Fe3++2Cl﹣ |
C | 向FeCl3溶液中加入铁粉 | 棕黄色溶液变为浅绿色 | Fe具有还原性 | Fe+Fe3+═2Fe2+ |
D | 向FeCl3溶液中加入铜粉 | 蓝色溶液变为棕黄色 | Fe3+具有氧化性 | Fe3++Cu═Fe2++Cu2+ |
A . A
B . B
C . C
D . D
将下列固体物质溶于水,再将其溶液加热、蒸发结晶、再灼烧,能得到化学组成与原固体物质相同的是( )
A . FeCl3
B . NaAlO2
C . NaHCO3
D . Na2SO3
下列有关化学物质的俗称错误的是( )
A . 碳酸钠的俗称是纯碱
B . 四氧化三铁的俗称是磁性氧化铁
C . 氧化铁的俗称是铁红
D . 碳酸氢钠的俗称是苏打
化学已经渗透到人类生活的各个方面,下列说法不正确的是( )
A . 卫生间与铁器接触的瓷砖上的斑斑锈迹,可用稀盐酸清洗
B . 治疗红眼病可用95%的酒精冲洗眼睛进行杀菌消毒
C . “地沟油”禁止食用,但可以经过加工处理制肥皂或生物柴油,可以实现厨余废物利用
D . 停车场安装催化光解设施,可将汽车尾气中的CO和NO,反应生成无毒气体
现有金属单质A、B、C和气体甲、乙、丙及物质D、E、F、G、H,它们之间能发生如下反应(图中有些反应的产物和反应的条件没有全部标出)。
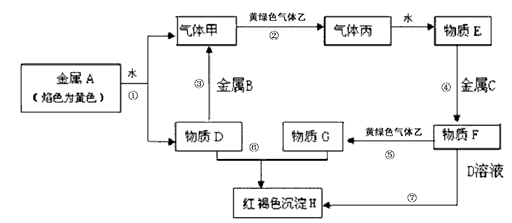
请根据以上信息回答下列问题:
-
(1) 写出下列物质的化学式:A: B: F: 丙:
-
(2) 说出黄绿色气体乙的一种用途:。
-
(3) 若除去F溶液中含有的少量G,需加入,实验室检验G中所含的金属离子时,常在G的溶液中加入溶液。
-
(4) 反应①的离子方程式为。
-
(5) 反应⑦涉及的化学方程式有。
根据下列反应事实写出相应的化学方程式。
-
(1) 双氧水在二氧化锰的催化作用下生成水和氧气:。
-
(2) 在尘埃的作用下,二氧化硫和氧气反应生成三氧化硫(SO3):。
-
(3) Cu和AgNO3溶液反应,生成Cu(NO3)2溶液和Ag:。
-
(4) 少量CuSO4溶液滴入NaOH稀溶液中生成Cu(OH)2沉淀和Na2SO4溶液:。
-
(5) 一氧化碳和四氧化三铁(Fe3O4)在高温下反应,生成铁和二氧化碳:。
有关物质及其用途的描述,正确的是( )
①Al2O3(作耐火坩埚) ②KAl(SO4)2·12H2O(作消毒剂)③Fe2O3(作黄色油漆和涂料) ④NaHCO3(作食用碱) ⑤钠、钾、锶、钡等化合物(作烟花的焰色) ⑥Na2O2(作呼吸面具供氧剂)
A . ①④⑤⑥
B . ①②⑤⑥
C . ①③④⑤
D . 全部
已知有以下物质相互转化:
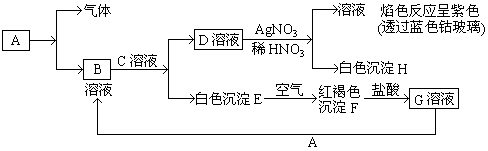
试回答
-
(1) 写出C的化学式;
-
(2) A与水蒸气反应方程式为: ;
-
(3) 写出由E转变成F的化学方程式;
-
(4) 鉴别G溶液中阳离子的方法是:,现象为:;用G溶液可以腐蚀铜印刷电路板,离子反应方程式为;
-
(5) 金属铝与A的氧化物可用来焊接火车铁轨,实验室中该反应所需药品有。
已知A为金属单质,下列物质相互转化如图所示:
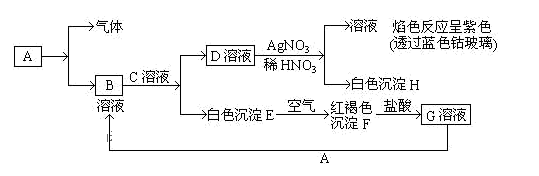
试回答:
-
(1) 写出B的化学式,D的化学式。
-
(2) 写出由E转变成F的化学方程式。
-
(3) 向G溶液加入A的有关离子反应方程式。
-
(4) 某同学取B的溶液酸化后加入碘化钾淀粉溶液,在空气中放置一会儿变为蓝色,写出与上述变化过程相关的离子方程式,。
“灌钢法”是我国古代劳动人民对钢铁冶炼技术的重大贡献,陶弘景在其《本草经集注》中提到“钢铁是杂炼生鍒作刀镰者”。“灌钢法”主要是将生铁和熟铁(含碳量约0.1%)混合加热,生铁熔化灌入熟铁,再锻打成钢。下列说法错误的是( )
A . 钢是以铁为主的含碳合金
B . 钢的含碳量越高,硬度和脆性越大
C . 生铁由于含碳量高,熔点比熟铁高
D . 冶炼铁的原料之一赤铁矿的主要成分为Fe2O3
《墨子·天志》中记载:“书之竹帛,镂之金石”。下列说法错误的是( )
A . 竹简的主要成分纤维素是天然有机高分子化合物
B . 丝帛不宜使用含酶洗涤剂洗涤
C . 饱和氯化铵溶液可以洗去金属表面的锈迹
D . “石”指的是陶瓷、玉石,制作陶瓷过程中只发生物理变化
将某难溶于水的含铁化合物溶于盐酸,滴加KSCN溶液不发生颜色变化,再加入适量的氯水,溶液立即呈红色,该化合物是( )
A . Fe2O3
B . FeCl3
C . FeSO4
D . FeO
下列有关铁及其化合物的叙述正确的是( )
A . Fe3O4可用作红色颜料
B . Cl2可用于除去FeCl2溶液中混有的少量FeCl3
C . 铁与水蒸气高温反应可生成Fe3O4和氢气
D . 饱和FeCl3溶液滴入NaOH溶液中可制得Fe(OH)3胶体
下图所示装置可用来制取Fe(OH)2和观察Fe(OH)2在空气中被氧化时的颜色变化。实验提供的试剂:铁屑、6 mol/L硫酸溶液、NaOH溶液。下列说法不正确的是( )
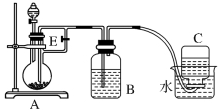
A . B中盛有一定量的NaOH溶液,A中应预先加入的试剂是铁屑
B . 实验开始时应先将活塞E关闭
C . 生成Fe(OH)2的操作为:关闭E,使A中溶液压入B瓶中
D . 取下装置B中的橡皮塞,使空气进入,有关反应的化学方程式为:4Fe(OH)2+O2+2H2O=4Fe(OH)3
下列说法正确的是( )
A . 钠在氧气中燃烧生成过氧化钠,则锂在氧气中燃烧也生成过氧化锂
B .  的分子构型为直线形,则
的分子构型为直线形,则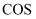 分子构型也为直线形
C . 碳酸钠溶于水放出热量,则碳酸氢钠溶于水也是放出热量
D .
分子构型也为直线形
C . 碳酸钠溶于水放出热量,则碳酸氢钠溶于水也是放出热量
D . 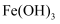 在空气中加热分解生成
在空气中加热分解生成 , 则
, 则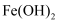 在空气中加热也分解生成
在空气中加热也分解生成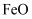
 的分子构型为直线形,则
的分子构型为直线形,则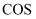 分子构型也为直线形
C . 碳酸钠溶于水放出热量,则碳酸氢钠溶于水也是放出热量
D .
分子构型也为直线形
C . 碳酸钠溶于水放出热量,则碳酸氢钠溶于水也是放出热量
D . 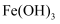 在空气中加热分解生成
在空气中加热分解生成 , 则
, 则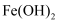 在空气中加热也分解生成
在空气中加热也分解生成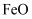
某学习小组为认识铁及其化合物的性质、分散系的性质做了如下一组综合实验,根据实验流程回答相关问题:

-
(1) 请写出Fe2O3与①反应的离子方程式:。
-
(2) 向FeCl2溶液中滴加NaOH溶液最终生成Fe(OH)3浊液,该过程的现象为,此过程中发生的氧化还原反应为(用化学方程式表式)。
-
(3) 将FeCl3饱和溶液滴入沸水中,并继续煮沸至红褐色,制得的分散系③为,把它与FeCl3溶液、Fe(OH)3浊液的区别开来的实验方法是。
最近更新



