探究碳酸钠与碳酸氢钠的性质 知识点题库
下列实验过程中始终无明显现象的是( )
A . 二氧化氮通入硫酸亚铁溶液中
B . 二氧化碳通入氯化钙溶液中
C . 二氧化碳通入饱和的碳酸钠溶液中
D . 氨气通入氯化铝溶液中
过量的NaHCO3和Na2O2混合,在密闭容器中充分混合加热后,最后排出气体,残留的固体是 ( )
A . Na2O
B . Na2CO3
C . Na2O2和Na2CO3
D . Na2O2和Na2O
加热纯碱和小苏打的混合物20克,至质量不再变化为止,冷却后称量其固体质量是13 .8克,则原混合物中纯碱的质量分数是( )
A . 84%
B . 8.4%
C . 1.6%
D . 16%
关于Na2CO3和NaHCO3性质的说法正确的是( )
A . 热稳定性:NaHCO3 <Na2CO3
B . 与Ca(OH)2溶液反应:Na2CO3溶液中有白色沉淀生成,NaHCO3溶液中没有沉淀生成
C . 相同温度时,在水中的溶解性:NaHCO3>Na2CO3
D . 相同物质的量浓度时,溶液的导电能力:NaHCO3>Na2CO3
将9.58 g Na2CO3·10H2O与NaHCO3的混合物溶于水配成100mL溶液,测得c(Na+)=1 mol/L。再取同质量的混合物,充分加热至质量不变时,所得固体的质量为:( )
A . 5.30g
B . 7.78g
C . 6.72g
D . 6g
有关Na2CO3和NaHCO3的性质,下列叙述错误的是( )
A . 相同温度下,等浓度的Na2CO3和NaHCO3溶液的碱性比较,前者更强
B . 常温时水溶性:Na2CO3>NaHCO3
C . 在酒精灯加热的条件下,前者不分解,后者分解
D . 将澄清的石灰水分别加入Na2CO3和NaHCO3溶液中,前者产生沉淀,后者无现象
关于Na2CO3和NaHCO3性质的说法正确的是( )
A . 在水中的溶解性:NaHCO3>Na2CO3
B . 热稳定性:NaHCO3<Na2CO3
C . 与酸反应的速率:NaHCO3<Na2CO3
D . 只可能让NaHCO3转化成Na2CO3
用四种溶液进行实验,下表中“操作及现象“与”溶液“对应关系错误的是( )
选项 | 操作及现象 | 溶液 |
A | 通入二氧化碳,溶液变浑浊 | 饱和碳酸钠溶液 |
B | 通入二氧化碳,溶液变浑浊,继续通二氧化碳至过量,浑浊消失 | 硅酸钠溶液 |
C | 通入二氧化碳,溶液变浑浊,继续通二氧化碳至过量,浑浊消失,再加入足量氢氧化钠溶液,又变浑浊 | 澄清石灰水 |
D | 通入二氧化碳,溶液变浑浊,再加入品红溶液,红色褪色 | 次氯酸钙溶液 |
A . A
B . B
C . C
D . D
下列实验方案中,不能测定Na2CO3和NaHCO3混合物中Na2CO3质量分数的是( )
A . 取a克混合物充分加热,得b克固体
B . 取a克混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得b克固体
C . 取a克混合物与足量Ba(OH)2溶液充分反应,过滤、洗涤、烘干,得b克固体
D . 取a克混合物与足量稀硫酸充分反应,逸出气体用碱石灰吸收,增重b克
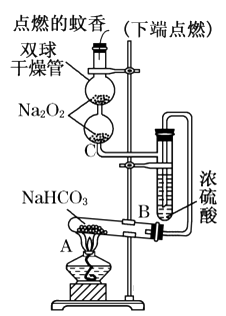
如图实验装置用于验证某些物质的性质.在试管A中装入足量的固体NaHCO3.试回答下列问题:
-
(1) 在A试管内发生反应的化学方程式是.
-
(2) B装置的作用是.
-
(3) 在双球干燥管内发生反应的化学方程式为.
-
(4) 双球干燥管内观察到的实验现象是.上述实验现象说明.
-
(5) 若将干燥管内的Na2O2换成Na2O,则双球干燥管内观察到的实验现象是.
下列有关NaHCO3、Na2CO3的性质比较中,正确的是( )
A . 热稳定性Na2CO3<NaHCO3
B . 常温时水溶性Na2CO3< NaHCO3 ,
C . 可用BaCl2溶液区分NaHCO3固体和Na2CO3固体
D . 等物质的量的NaHCO3和Na2CO3与足量稀盐酸反应,NaHCO3放出的CO2多
下列关于Na2CO3的分类错误的是( )
A . 属于化合物
B . 属于电解质
C . 属于盐
D . 属于碱
现有下列4种物质:①浓H2SO4、②NO2、③NH4Cl、④NaHCO3。其中,可以使蔗糖变黑的是(填序号);与水发生反应由红棕变为无色的是(填序号);加热分解,遇冷又化合的是(填序号);加热分解生产无色无味气体的反应方程式是。
下列溶液分别与碳酸钠溶液混合后不能产生沉淀的是( )
A . 氢氧化钙溶液
B . 氢氧化钡溶液
C . 氢氧化钠溶液
D . 氯化钙溶液
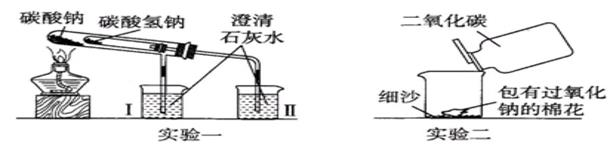
下图是教师在课堂中演示的两个实验装置(铁架台等辅助仪器略去)
请回答下列问题
-
(1) 实验一的实验目的是 , 实验过程中可以观察到烧杯中的现象是 ,加热后试管中发生反应的化学方程式是:
-
(2) 实验二用来验证Na2O2与CO2的反应,观察到的实验现象是:包有Na2O2的棉花燃烧。Na2O2与CO2的反应的化学方程式 ,该实验可以得出许多结论,请你写出由该实验得出的两个结论。
结论1:
结论2:
下列物质的稀溶液相互反应,无论是前者滴入后者,还是后者滴入前者,反应现象都相同的是( )
A . Na2CO3和盐酸
B . AlCl3和NaOH
C . NaAlO2和硫酸
D . Na2CO3和BaCl2
在给定条件下,下列选项所示的物质间转化均能实现的是( )
A .  B .
B . 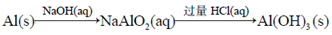 C . Fe
C . Fe  FeCl2
FeCl2 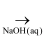 Fe(OH)2
D .
Fe(OH)2
D . 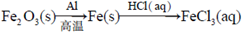
 FeCl2
FeCl2 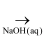 Fe(OH)2
D .
Fe(OH)2
D .
下列实验操作或装置正确的是( )
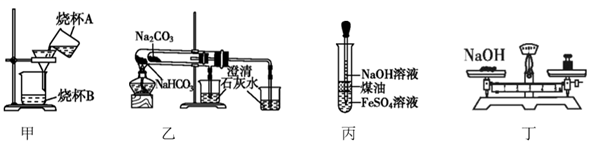
A . 图甲装置可用于完成过滤操作
B . 图乙可用于比较碳酸钠和碳酸氢钠的热稳定性
C . 图丙可实现制备Fe(OH)2并观察其颜色
D . 图丁表示为配制一定物质的量浓度NaOH溶液时称量溶质的操作
将10mL 2mol•L﹣1盐酸注入①、②两个完全相同的装置(如图),然后迅速密封。下列叙述正确的是( )

A . CO2的生成速率:①>②
B . 若忽略温度变化,最终两气球体积:①>②
C . ①中发生反应的离子方程式是CO32﹣+2H+═CO2↑+H2O
D . 若溶液体积变化忽略不计,则最终两试管中Na+的物质的量浓度相等
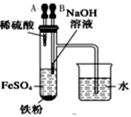
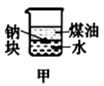
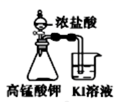
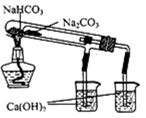
下列装置所示的实验中,不能达到实验目的是( )
| | | | |
| A.长时间看到Fe(OH)2白色沉淀 | B.证明ρ(煤油)<ρ(钠)<ρ(水) | C.探究氧化性:KMnO4>Cl2>I2 | D.比较NaHCO3、Na2CO3 , 的热稳定性 |
A . A
B . B
C . C
D . D
最近更新