探究碳酸钠与碳酸氢钠的性质 知识点题库
-
(1) NaN3是气体发生剂,受热分解产生N2和Na,N2的电子式为 。
-
(2) Fe2O3是主氧化剂,与Na反应生成的还原产物为 (已知该反应为置换反应).
-
(3) KClO4是助氧化剂,反应过程中与Na作用生成KCl和Na2O。KClO4含有化学键的类型为 ,K的原子结构示意图为 。
-
(4) NaHCO3是冷却剂,吸收产气过程中释放的热量而发生分解,其化学方程式为 。
-
(5) 100g上述产气药剂产生的气体通过碱石灰后得到N2 33.6L(标准状况).
①用碱石灰除去的物质为
②该产气药剂中NaN3的质量分数为
NH3+CO2+H2O=NH4HCO3
NH4HCO3+NaCl=NaHCO3↓+NH4Cl
2NaHCO3 Na2CO3+CO2↑+H2O↑
Na2CO3+CO2↑+H2O↑
-
(1) 碳酸氢铵与饱和食盐水反应,能析出碳酸氢钠晶体的原因是________(填字母标号)。A . 碳酸氢钠难溶于水 B . 碳酸氢钠受热易分解 C . 碳酸氢钠的溶解度相对较小,所以在溶液中首先结晶析出
-
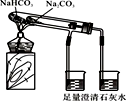
(2) 某探究活动小组根据上述制碱原理,进行碳酸氢钠的制备实验,同学们按各自设计的方法实验。
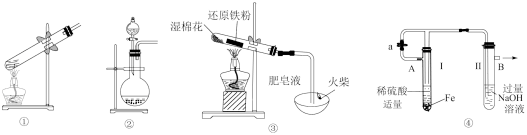
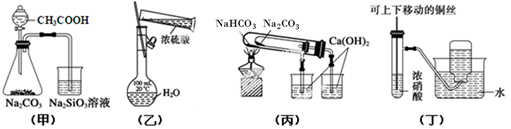
①一位同学将二氧化碳气体通入含氨的饱和食盐水中制备碳酸氢钠,实验装置如下图所示(图中夹持、固定用的仪器未画出):

试回答下列有关问题:
(Ⅰ)乙装置中的试剂是;
(Ⅱ)丁装置中稀硫酸的作用是。
(Ⅲ)实验结束后,分离出NaHCO3晶体的操作是(填分离操作的名称)。
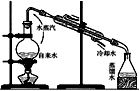
②另一位同学用下图中戊装置(其他装置未画出)进行实验:
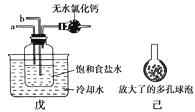
(Ⅰ)实验时,须先从管通入气体,再从管通入气体;
(Ⅱ)有同学建议在戊装置的b管下端连接己装置,原因是。
-
(3) 请你再写出一种实验室制取少量碳酸氢钠的方法:。
 B . 验证Cu与浓硝酸反应的热量变化
B . 验证Cu与浓硝酸反应的热量变化 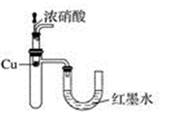 C . 验证NH3易溶于水
C . 验证NH3易溶于水 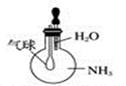 D . 比较Na2CO3与NaHCO3的稳定性
D . 比较Na2CO3与NaHCO3的稳定性 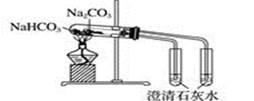
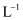 NaHCO3溶液的pH为8.4;取NaHCO3溶液向其中滴加CaCl2溶液至pH=7,滴加过程中产生白色沉淀,但无气体放出。下列分析正确的是( )
NaHCO3溶液的pH为8.4;取NaHCO3溶液向其中滴加CaCl2溶液至pH=7,滴加过程中产生白色沉淀,但无气体放出。下列分析正确的是( )
| | | | |
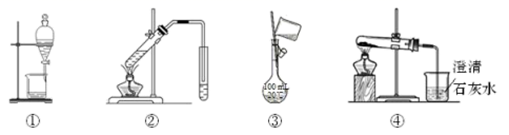
| A.干燥Cl2 | B.分离汽油与食盐溶液 | C.实验室制取少量蒸馏水 | D.比较Na2CO3与NaHCO3的稳定性 |
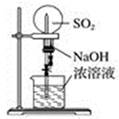
 B . 比较碳酸钠与碳酸氢钠的热稳定性
B . 比较碳酸钠与碳酸氢钠的热稳定性 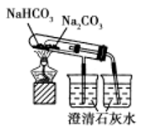 C . 实验室制取少氨气
C . 实验室制取少氨气 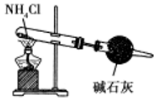 D . 检查装置气密性
D . 检查装置气密性 
 +H+=CO2↑+H2O
B . 钠放入硫酸铜溶液中:2Na+Cu=2Na++Cu2+
C . 金属铁与氯化铁溶液反应:Fe+2Fe3+=3Fe2+
D . 磁性氧化铁溶于稀盐酸:Fe2O3+6H+=2Fe3++3H2O
+H+=CO2↑+H2O
B . 钠放入硫酸铜溶液中:2Na+Cu=2Na++Cu2+
C . 金属铁与氯化铁溶液反应:Fe+2Fe3+=3Fe2+
D . 磁性氧化铁溶于稀盐酸:Fe2O3+6H+=2Fe3++3H2O
①NaHCO3 ②Al2O3 ③Al(OH)3 ④Al ⑤Na2CO3
-
(1) 实验室两瓶固体试剂标签已经模糊,无法区分 Na2CO3和 NaHCO3两种白色固体,该小组设计了下述实验方案,方案或结论不正确的是 。A . 将两种固体分别配制成溶液,滴入澄清石灰水,观察有无浑浊,出现浑浊现象的为Na2CO3 B . 称取等质量的固体粉末装入气球中,倒入装有足量盐酸的试管中,最终气球体积大的为 Na2CO3 C . 将两种固体分别加入试管中加热,将产生的气体通入澄清石灰水,出现浑浊的为NaHCO3 D . 往两种固体中分别滴入适量的水,用温度计测量过程中温度的变化,温度升高的为Na2CO3
-
(2) 确定固体成分后,该小组利用传感器探究 Na2CO3和 NaHCO3的性质。
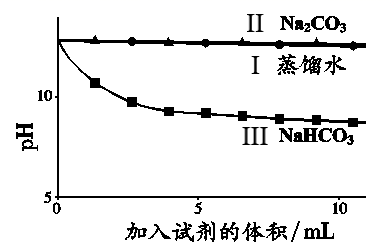
(已知:氢氧根离子的浓度越小,pH 越小,溶液碱性越弱)
实验
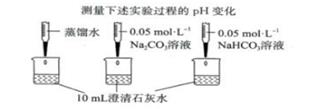
绘图

①实验中,Na2CO3溶液滴入澄清石灰水,发生的离子反应为 ;该反应中 OH-没有参与反应,图给证据是;
②实验中,滴加 NaHCO3溶液的 pH 变化与 Na 2 CO 3 溶液的有明显差异,用离子方程式解释滴加 NaHCO3溶液烧杯中 pH 显著减小的原因;
-
(1) Ⅰ.“钠在空气中燃烧”实验深度探究
Na在空气中燃烧主要产物是(填化学式)。
-
(2) 钠在空气中燃烧后生成的固体粉末中还含有黑色固体物质。通过查阅文献发现,有一种观点认为该黑色固体物质是C和铁的氧化物。
ⅰ.生成C的原因是CO2和Na在加热条件发生如下反应,请配平该化学方程式,并用单线桥表示出电子转移的方向和数目:
CO2+Na= Na2CO3+C
-
(3) ⅱ.产生铁的氧化物的原因是Na单质中含有0.002%左右的铁元素,在钠燃烧的时候铁被氧化为铁的氧化物。为了检验黑色固体物质中是否含有铁元素,进行了如下实验:
实验内容
实验现象
实验结论
①收集黑色固体物质溶于稀硫酸中
少量黑色固体物质不溶解
②取上层清液少许于一支试管中,滴入KSCN溶液
溶液变为红色
-
(4) Ⅱ.“纯碱和小苏打”性质实验的深度探究
该组同学利用下图对“碳酸钠溶液与盐酸反应”进行探究
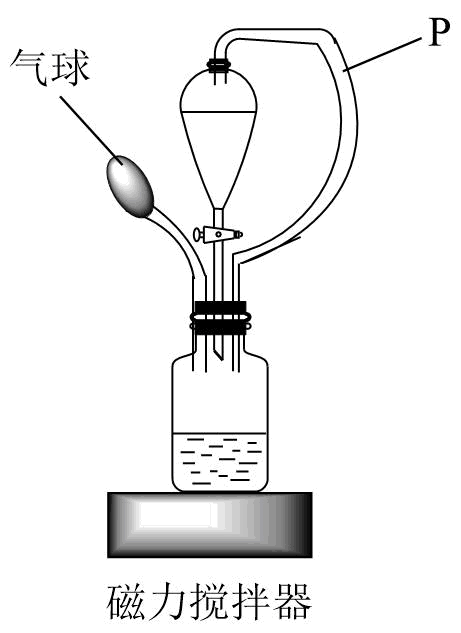
导管P的作用是。
-
(5) 开始实验;
ⅰ.广口瓶中预先盛放10 mL 1 mol/L的Na2CO3溶液,将分液漏斗中10 mL 1 mol/L的HCl溶液缓缓滴入到广口瓶中,观察到的现象是,在分液漏斗再加10 mL 1 mol/L的HCl溶液并滴入广口瓶,发生反应的离子方程式为。
ⅱ.广口瓶中预先盛放10 mL 1 mol/L的HCl溶液,将分液漏斗中的10 mL 1 mol/L Na2CO3溶液中的5 mL溶液快速滴入到广口瓶中,立刻有大量气泡产生,气球膨胀。再将剩余的5 mL 1 mol/L的Na2CO3溶液加入到广口瓶中,几分钟后,气球变扁,变扁的原因是(用化学方程式作答)。
-
(6) 实验结论:
a.Na2CO3与盐酸反应是分步进行的;
b.碳酸钠和碳酸氢钠在一定条件下可以相互转化;
c.
 和
和 中结合H+能力较强的是(填离子符号)。
中结合H+能力较强的是(填离子符号)。
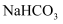 )受热后发生分解反应生成二氧化碳、水和碳酸钠,是常用的膨松剂之一,它可以与酒石酸氢钾、淀粉等按一定比例混合制成复合膨松剂,复合膨松剂遇水会产生二氧化碳,起到膨松作用。下列说法正确的是( )
)受热后发生分解反应生成二氧化碳、水和碳酸钠,是常用的膨松剂之一,它可以与酒石酸氢钾、淀粉等按一定比例混合制成复合膨松剂,复合膨松剂遇水会产生二氧化碳,起到膨松作用。下列说法正确的是( )
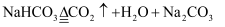 C . 碳酸氢钠作膨松剂时,必须与酒石酸氢钾、淀粉混合使用
D . 复合膨松剂应在干燥的环境中保存
C . 碳酸氢钠作膨松剂时,必须与酒石酸氢钾、淀粉混合使用
D . 复合膨松剂应在干燥的环境中保存
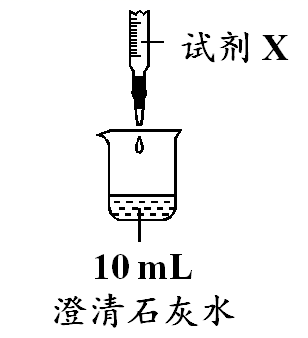
实验装置 | 试剂X | 实验结果 | ||
| I | II | III | ①II、III均产生白色沉淀 ②烧杯中溶液pH变化如下
|
蒸馏水 | 0.05mol·L−1 Na2CO3溶液 | 0.05mol·L−1 NaHCO3溶液 | ||
已知:pH越大,c(OH-)越大,溶液碱性越强。
下列说法错误的是( )
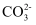 与OH−不反应,II中发生反应:
与OH−不反应,II中发生反应: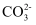 +Ca2+=CaCO3↓
C . III比II的pH曲线降低,说明
+Ca2+=CaCO3↓
C . III比II的pH曲线降低,说明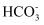 与OH−反应,III中初期发生反应:
与OH−反应,III中初期发生反应: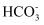 +OH−+Ca2+=CaCO3↓+H2O
D . III中石灰水恰好完全反应时,溶液pH=7
+OH−+Ca2+=CaCO3↓+H2O
D . III中石灰水恰好完全反应时,溶液pH=7