海带成分中碘的检验 知识点题库
某同学设计实验从海带中提取碘:①滴加稀硫酸和双氧水;②在海带中加入少量酒精,点燃使其燃烧为灰烬,在灰烬中加水搅拌;③加四氯化碳并振荡;④过滤;⑤分液.该实验的合理操作顺序是( )
A . ①③⑤②④
B . ②①③④⑤
C . ②④①③⑤
D . ③①②⑤④
溴、碘主要存在于海水中,有“海洋元素”的美称.从海水中提取碘的途径如下所示:
干海带 海带灰
海带灰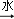 水溶液
水溶液 →碘单质.下列叙述正确的是( )
→碘单质.下列叙述正确的是( )
A . 碘元素在海水中也有游离态存在
B . 在提取的过程中用的氧化剂可以是H2O2
C . 操作A是结晶或重结晶
D . B是提纯操作,常用蒸馏或分馏
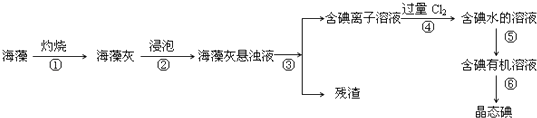
海藻中含有丰富的、以碘离子形式存在的碘元素.在实验室中,从海藻里提取碘的流程和实验装置如下:
-
(1) 写出步骤④对应反应的离子方程式:.
-
(2) 步骤④除了加入过量Cl2 , 下列氧化剂最好选用(填代号).
A.浓硫酸 B.H2O2溶液 C.KMnO4溶液
理由是.
-
(3) 步骤⑤中,某学生选择用苯提取碘的理由是.
-
(4) 设计一种检验提取碘后的水溶液中是否还含有单质碘的简单方法.
海带中含有丰富的碘.为了从海带中提取碘,某研究性学习小组设计并进行了以下实验(苯,一种不溶于水,密度比水小的液体):
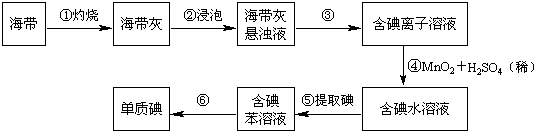
请填写下列空白:
-
(1) 步骤①灼烧海带时,除需要三脚架外,还需要用到的实验仪器是 (从下列仪器中选出所需的仪器,用标号字母填写在空白处).A . 烧杯 B . 坩埚 C . 表面皿 D . 泥三角 E . 酒精灯 F . 干燥器
-
(2) 步骤③的实验操作名称是;步骤⑥的目的是从含碘苯溶液中分离出单质碘和回收苯,该步骤的实验操作名称是.
-
(3) 步骤⑤是萃取、分液,某学生选择用苯来提取碘的理由是.
在分液操作中,应充分振荡,然后静置,待分层后(填标号),以下略.
A.直接将含碘苯溶液从分液漏斗上口倒出
B.直接将含碘苯溶液从分液漏斗下口放出
C.先将水层从分液漏斗的下口放出,再将含碘苯溶液从下口放出
D.先将水层从分液漏斗的下口放出,再将含碘苯溶液从上口倒出
-
(4) 请设计一种检验提取碘后的水溶液中是否还含有单质碘的简单方法是:.
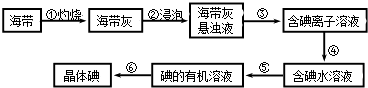
海带中含有丰富的碘.为了从海带中提取碘,某研究性学习小组设计并进行了以下实验:
-
(1) 步骤③的实验操作名称是;步骤⑥的目的是从含碘苯溶液中分离出单质碘和回收苯,该步骤的实验操作名称是.
-
(2) 步骤④需加入的试剂是,反应的离子方程式是.
-
(3) 步骤⑤中,某学生选择用苯来提取碘,理由是.
某化学兴趣小组按如下实验流程提取海带中的碘,他们的设计如下图:
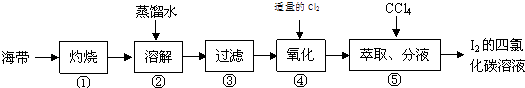
根据以上流程,回答以下问题.
-
(1) 第②步为了加快溶解速率并使碘离子充分进入溶液,可以采取的措施是、(写出两条).
-
(2) 如第④、⑤步通入的Cl2是与NaI溶液反应,再往其中加四氯化碳振荡、静置,现象是;此法还适用于I﹣的检验,I﹣检验的另一方法是向待测溶液中先滴加AgNO3溶液,生成色沉淀,再加足量的HNO3 , 沉淀不溶解.
从海带中提取碘的实验过程中涉及下列操作,其中正确的是( )
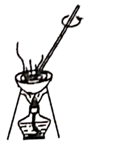
A .  将海带灼烧成灰
B .
将海带灼烧成灰
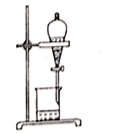
B . 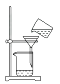 过滤得含I-的盐
C .
过滤得含I-的盐
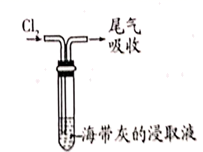
C . 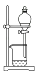 放出碘的苯溶液
D .
放出碘的苯溶液
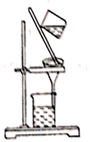
D . 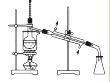 分离碘并回收苯
分离碘并回收苯
 将海带灼烧成灰
B .
将海带灼烧成灰
B .  过滤得含I-的盐
C .
过滤得含I-的盐
C .  分离碘并回收苯
分离碘并回收苯
下列有关说法正确的是( )
①二氧化硅可与NaOH溶液反应,因此可用NaOH溶液雕刻玻璃;
② 明矾溶于水可水解生成Al(OH)3胶体,因此可以用明矾对自来水进行杀菌消毒;
③ 可用蒸馏法、电渗析法、离子交换法等对海水进行淡化;
④ 从海带中提取碘只需用到蒸馏水、H2O2溶液和四氯化碳三种试剂;
⑤地沟油可用来制肥皂、提取甘油或者生产生物柴油;
⑥石英玻璃、Na2O·CaO·6SiO2、淀粉、氨水的物质类别依次为纯净物、氧化物、混合物、弱电解质。
A . ③⑤⑥
B . ①④⑤
C . 除②外都正确
D . ③⑤
下列说法正确的是( )
A . 向3mL95%乙醇溶液中加入几颗CoCl2·6H2O晶体,充分溶解后再滴加蒸馏水至溶液恰好呈粉红色,用酒精灯加热该试管,溶液呈蓝色
B . 金属汞一旦洒落在实验室地面或桌面时,必须尽可能收集,并深埋处理
C . 实验室从海带中提取单质碘的方法是:取干海带→浸泡→过滤→氧化→结晶→过滤
D . 制备KNO3晶体实验中,为得到较大颗粒晶体,可将热KNO3溶液快速冷却
从海带中提取碘要经过灼烧、浸取、过滤、氧化、萃取、分液、蒸馏等操作,下列对应的装置合理,操作规范的是( )
A . 海带灼烧成 灰  B . 过滤含碘离子溶液
B . 过滤含碘离子溶液 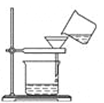 C . 放出碘的苯溶液
C . 放出碘的苯溶液 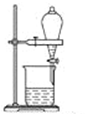 D . 分离碘并回收苯
D . 分离碘并回收苯 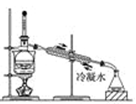
 B . 过滤含碘离子溶液
B . 过滤含碘离子溶液  C . 放出碘的苯溶液
C . 放出碘的苯溶液  D . 分离碘并回收苯
D . 分离碘并回收苯 
海洋资源的利用具有广阔前景。
-
(1) 下图是从海水中提取镁的简单流程。
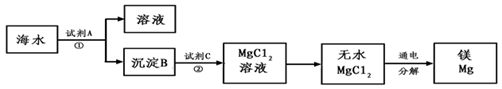
①工业上常用于沉淀Mg2+的试剂A是。
②由无水MgCl2制取Mg的化学方程式是。
-
(2) 海带灰中富含以I-形式存在的碘元素.实验室提取I2的途径如下所示:
干海带
 海带灰
海带灰  滤液
滤液 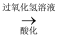
 I2
I2①灼烧海带至灰烬时所用的主要仪器名称是 。
②向酸化的滤液中加过氧化氢溶液,写出该反应的离子方程式。
③反应结束后,加入CCl4作萃取剂,采用萃取—分液的方法从碘水中提取碘,主要操作步骤如图:

甲、乙、丙3步实验操作中,错误的是 (填“甲”、“乙”或“丙”)。
下列有关判断正确的是( )
A . 金属阳离子被还原,一定会得到金属单质
B . 金属冶炼过程中,金属化合物得到电子发生氧化反应
C . 海带中含有碘单质,能使淀粉变蓝
D . 通过铝热反应可以在野外焊接钢轨
海带产量高、价格低,常用作提取碘单质的原料。下列实验装置或操作能达到实验目的的是( )
| A | B | C | D |
| | | | |
| 干海带烧灼为海带灰 | 分离海带灰的浸取液 | 氧化碘离子为碘单质 | 分四离四氯化碳中的碘 |
A . A
B . B
C . C
D . D
为了从海带中提取碘,某研究性学习小组设计并进行了以下实验:
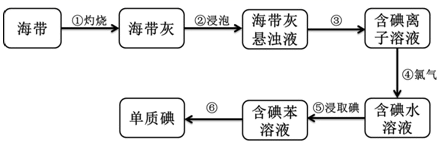
下列说法错误的是( )
A . 步骤③实验用到的主要玻璃仪器是烧杯、漏斗和玻璃棒
B . 步骤④反应的离子方程式:Cl2+2I-=I2+2Cl-
C . 步骤⑤的操作是萃取,可以用无水酒精作为萃取剂
D . 步骤⑥的操作名称是蒸馏
下列说法不正确的是( )
A . 应避免铵态氮肥与草木灰混合施用
B . 工业上可用离子交换法提高海带中碘的提取率
C . 电解饱和食盐水可以得到金属钠和氯气
D . 将生铁进一步炼制减少含碳量,能得到耐腐蚀的钢
下列利用海带提取单质碘的实验原理与装置不能达到实验目的的是( )
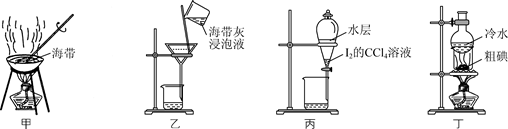
A . 用装置甲灼烧海带
B . 用装置乙过滤海带灰浸泡液
C . 用装置丙得到I2的CCl4溶液
D . 用装置丁提纯粗碘
为了提取饱和碘水中的碘单质,下列实验操作中不需要的步骤是( )
A . 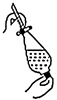 B .
B . 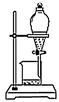 C .
C . 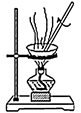 D .
D . 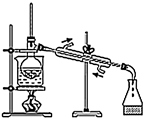
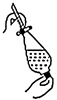 B .
B .  C .
C .  D .
D . 
下列说法正确的是( )
A . 纸层析法分离Fe3+和Cu2+ , 氨熏后纸条上端为棕红色,下端为深蓝色
B . 从海带中提取碘的工业生产过程步骤:灼烧、浸泡、过滤、氧化、结晶、提纯
C . 培养明矾晶体时,将小晶体悬挂在90℃热饱和溶液的烧杯中央,自然冷却至室温
D . 金属钾、钠和白磷暴露空气中易燃烧,均应保存在煤油中
从海水中提取溴的流程如下:
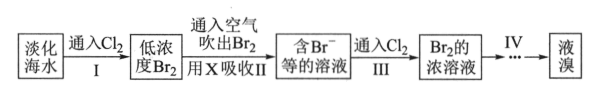
下列有关说法不正确的是( )
A . 从海水中提溴的主要步骤可表示为:氧化→吹出→吸收
B . 步骤Ⅱ的离子反应可能是: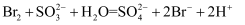 C . 步骤Ⅳ萃取、分液和蒸馏
D . 工业上每获得1mol
C . 步骤Ⅳ萃取、分液和蒸馏
D . 工业上每获得1mol , 需要消耗
, 需要消耗 22.4L(标况)
22.4L(标况)
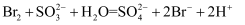 C . 步骤Ⅳ萃取、分液和蒸馏
D . 工业上每获得1mol
C . 步骤Ⅳ萃取、分液和蒸馏
D . 工业上每获得1mol , 需要消耗
, 需要消耗 22.4L(标况)
22.4L(标况)
海带、紫菜等藻类植物中含有丰富的碘元素,下列叙述正确的是( )
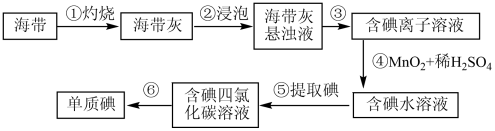
A . 加碘食盐可以使淀枌溶液变蓝
B . 步骤④中发生的反应为2I-+MnO2+4H+=I2+Mn2++2H2O
C . 步骤④如果用碘酸钾氧化,理论上每产生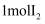 , 转移2mol电子
D . 步骤⑤中提取碘的方法是蒸馏
, 转移2mol电子
D . 步骤⑤中提取碘的方法是蒸馏
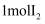 , 转移2mol电子
D . 步骤⑤中提取碘的方法是蒸馏
, 转移2mol电子
D . 步骤⑤中提取碘的方法是蒸馏
最近更新