氮的氧化物的性质及其对环境的影响 知识点题库
-
(1) 铜与浓硝酸反应生成NO2的化学反应方程式是
-
(2) NO2可用水吸收,该反应的化学反应方程式是
-
(3) 工业上可将SO2通入浓的Fe2(SO4)3溶液中来治理污染得副产物绿矾和硫酸,写出该反应的离子方程式
-
(4)
利用反应6NO2+8NH3
 7N2+12H2O也可处理NO2 . 当反应转移0.6mol电子时,则消耗的NH3在标准状况下的体积是
7N2+12H2O也可处理NO2 . 当反应转移0.6mol电子时,则消耗的NH3在标准状况下的体积是 -
(5) 已知:2SO2(g)+O2(g)⇌2SO3(g)△H1=﹣196.6kJ•mol﹣1
2NO(g)+O2(g)⇌2NO2(g)△H2=﹣113.0kJ•mol﹣1
则反应NO2(g)+SO2(g)⇌SO3(g)+NO(g)的△H= kJ•mol﹣1 .
一定条件下,将NO2与SO2以物质的量之比1:2置于恒容密闭容器中发生上述反应.
①下列能说明反应达到平衡状态的是 .
A.体系压强保持不变
B.SO3和NO的体积比保持不变
C.混合气体颜色保持不变
D.每消耗1mol SO3的同时消耗1mol NO2
②测得上述反应平衡时NO2与SO2物质的量之比为1:11,该反应的平衡常数
K= (保留1位小数).
-
(1) 漂白粉的有效成分是;
-
(2) 通常状况下带有特殊气味、不溶于水的液体是;
-
(3) 通常状况下呈红棕色的是;
-
(4) 电子工业中作为半导体材料的是。

-
(1) A中在加热至85℃反应,反应的化学方程式为,该实验装置不够完善,可以改进之处为。为了完成实验,装置从左到右接口的链接顺序是
 。
。
-
(2) 制得的氨水可用于在实验室模拟工业制硝酸的过程,装置如下(夹持装置略去)

① 装置B中反应的化学方程式是:。
② 请在装置图方框处画出必要仪器,并指出所加试剂。
③ 装置D中发生反应的化学方程式为。开始反应一段时间后,撤离热源反应也可以持续进行,原因为。
④ 某同学认为在装置F中可能出现白烟,应在装置D和装置F之间增加下列装置中的(填序号),从而避免此现象发生,提高硝酸的产率。利用改进后的装置进行实验,装置F中发生反应的化学方程式为。

⑤ 该装置还应在之后添加装置。
 Si+2CO↑硅被还原,所以硅的非金属性比碳强
D . 用SiO2制取硅酸,应先使二氧化硅与氢氧化钠溶液反应,然后通CO2
Si+2CO↑硅被还原,所以硅的非金属性比碳强
D . 用SiO2制取硅酸,应先使二氧化硅与氢氧化钠溶液反应,然后通CO2
-
(1) 氨气的制备
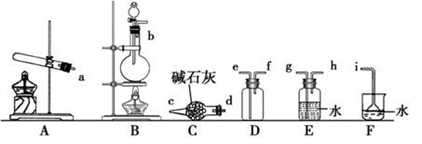
①氨气的发生装置可以选择上图中的,反应的化学方程式为。
②欲收集一瓶干燥的氨气,选择上图中的装置,其连接顺序为:发生装置→(按气流方向,用小写字母表示)。
-
(2) 氨气与二氧化氮的反应
将上述收集到的NH3充入注射器X中,硬质玻璃管Y中加入少量催化剂,充入NO2(两端用夹子K1、K2夹好)。在一定温度下按图示装置进行实验。
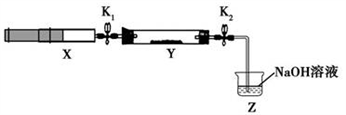
操作步骤
实验现象
解释原因
打开K1 , 推动注射器活塞,使X中的气体缓慢通入Y管中
①Y管中
②反应的化学方程式
将注射器活塞退回原处并固定,待装置恢复到室温
Y管中有少量水珠
生成的气态水凝集
打开K2
③
④
 为证明非金属性强弱:Si<C<S
B .
为证明非金属性强弱:Si<C<S
B .  为制备少量氧气
C .
为制备少量氧气
C .  为配制一定浓度硫酸溶液
D .
为配制一定浓度硫酸溶液
D .  制备并收集少量NO2气体
制备并收集少量NO2气体

 的废水会打破氮循环的稳态
D .
的废水会打破氮循环的稳态
D .  是歧化反应
是歧化反应
 B . 吸收氯化氢
B . 吸收氯化氢  C . 配制一定浓度的硫酸溶液
C . 配制一定浓度的硫酸溶液  D . 制备并收集少量NO2
D . 制备并收集少量NO2 
| 选项 | 实验 | 现象 | 结论 |
| A | 向2支盛有5 mL不同浓度NaHSO3溶液的试管中,同时加入2 mL 5% H2O2溶液 | 观察并比较产生气泡的快慢 | 浓度大的反应速率快 |
| B | 取 Al 和Fe2O3 完全反应后固体,溶于足量稀硫酸,滴加 KSCN 溶液 | 溶液不变红 | 反应后固体中可能含有 Fe2O3 |
| C | 将湿润的淀粉-KI 试纸放入含有红棕色气体的集气瓶中 | 试纸变蓝 | 该气体为 NO2 ,具有氧化性 |
| D | 将少量 Fe(NO3)2 加水溶解后,滴加稀硫酸酸化,再滴加 KSCN 溶液 | 溶液呈血红色 | Fe(NO3)2 已变质 |



