铵盐 知识点题库
某研究性学习小组的同学为家乡农业生产提出了下列建议,其中不合理的是( )
A . 要加大灌溉用水的管理力度,防止水资源的污染和浪费
B . 禁止就地焚烧农作物秸秆,应该将其回收用于制沼气
C . 用熟石灰改良酸性土壤,应同时施加碳铵(NH4HCO3)以提高土壤肥力
D . 要综合利用农家肥和化肥,重视在增施农家肥的基础上,配合使用化肥
“摩尔盐”[(NH4)2Fe(SO4)2•6H2O]是分析化学中的重要试剂.已知摩尔盐在隔绝空气的条件下加热至500℃时可完全分解.根据所学知识和有关原理分析,其分解产物肯定不正确的是( )
A . Fe2O3 SO2 NH3 H2O
B . FeO SO3 NH3 H2O
C . Fe2O3 SO2 SO3NH3 H2O
D . FeO SO2 NH3 H2O
)同时对农作物施用含N、P、K的三种化肥,对给定的下列化肥①K2CO3、②KCl、③Ca(H2PO4)2、④(NH4)2SO4 , ⑤氨水,最适当的组合是( )
A . ①③④
B . ①③⑤
C . ②③④
D . ②③⑤
下列有关物质用途的说法错误的是(
A . 硝酸铵可以用作化肥
B . 钠、钾的化合物可制作烟花
C . 油脂可用来制造肥皂
D . 98%乙醇溶液可用于医疗消毒
硫酸亚铁铵[(NH4)2Fe(SO4)2]是一种重要的化工原料,下列有关说法正确的是( )
A . Na+、Fe3+、K+、ClO﹣ 都可在该物质的溶液中大量共存
B . 检验该物质中Fe2+是否变质的方法是向该物质的溶液中滴入几滴KSCN溶液,观察溶液是否变红色
C . 向0.1mol•L﹣1该物质的溶液中逐滴滴加0.1mol•L﹣1NaOH溶液,生成沉淀的物质的量与加入NaOH溶液体积的关系如上图所示 D . 向该物质的溶液中滴加Ba(OH)2溶液,恰好使SO42﹣完全沉淀的离子方程式为:Fe2++2SO42﹣+2Ba2++2OH﹣═2BaSO4↓+Fe(OH)2↓
D . 向该物质的溶液中滴加Ba(OH)2溶液,恰好使SO42﹣完全沉淀的离子方程式为:Fe2++2SO42﹣+2Ba2++2OH﹣═2BaSO4↓+Fe(OH)2↓
 D . 向该物质的溶液中滴加Ba(OH)2溶液,恰好使SO42﹣完全沉淀的离子方程式为:Fe2++2SO42﹣+2Ba2++2OH﹣═2BaSO4↓+Fe(OH)2↓
D . 向该物质的溶液中滴加Ba(OH)2溶液,恰好使SO42﹣完全沉淀的离子方程式为:Fe2++2SO42﹣+2Ba2++2OH﹣═2BaSO4↓+Fe(OH)2↓
现有(NH4)2SO4、NH4NO3两种化肥,你认为哪种适宜用于酸性土壤?说明理由.
下列叙述不正确的是( )
A . H2S与SO2、NO与O2、NH3与HCl在常温下均不能大量共存
B . (NH4)2SO3、Ca(HCO3)2、NaAlO2均既能和稀硫酸又能和氢氧化钠溶液反应
C . Fe(OH)3、FeCl2、FeCl3均可通过化合反应得到
D . 制备Fe(OH)2时加苯液封,同时将滴管插入苯层液面以下,其目的是防止Fe(OH)2被空气氧化
下列实验现象可用同一原理解释的是( )
A . 品红溶液中分别通入SO2和Cl2 , 品红均褪色
B . 鸡蛋白溶液中分别加入NaCl溶液和HgCl2溶液,均有固体析出
C . 分别加热盛有NH4Cl和单质碘的试管,管口均有固体凝结
D . 溴水分别滴入植物油和裂化汽油中,溴水均褪色
下图表示有关的一种反应物或生成物(无关物质已略去),其中A、C为无色气体,请填写下列空白。

-
(1) 化合物W可能是或,C是,F是。
-
(2) 反应①中若消耗Na2O2 7.8 g,则转移的电子数为。
-
(3) 反应③的离子方程式:。
-
(4) A与CuO在加热条件下能反应生成N2和Cu,请写出该反应的化学方程式: 。
下列说法正确的是( )
A . 分别向等物质的量浓度的Na2CO3和NaHCO3溶液中滴加2滴酚酞溶液,后者红色更深
B . 分别向2 mL5%H2O2溶液中滴加1 mL 0.1 mol·L−1 FeCl3和CuSO4溶液,产生气泡快慢不相同
C . 蛋白质溶液遇饱和Na2SO4溶液或醋酸铅溶液均产生沉淀,沉淀均可溶于水
D . 加热NH4Cl和Ca(OH)2固体的混合物,可将二者分离
下列离子方程式,正确的是( )
A . 稀硫酸滴在铜片上:Cu+2H+=Cu2++H2↑
B . 将铜片插入硝酸银溶液中:Ag++Cu = Cu2++Ag
C . 氢氧化镁与稀盐酸混合OH-+H+=H2O
D . 向浓NaOH溶液中滴入几滴氯化铵溶液并加热:NH4++OH-  NH3↑+H2O
NH3↑+H2O
 NH3↑+H2O
NH3↑+H2O
某溶液中可能含有H+、NH4+、Mg2+、Al3+、Fe3+、CO32-、SO42-、NO3-中的几种.①若加入锌粒,产生无色无味无毒的气体;②若加入 NaOH 溶液,产生白色沉淀,且产生的沉淀的物质的量与加入 NaOH 的物质的量之间的关系如图所示.则下列说法正确的是( )
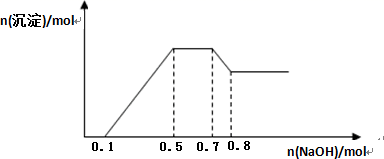
A . 溶液中的阳离子只有 H+、Mg2+、Al3+
B . 溶液中一定不含 CO32- , 一定含有SO42-和NO3-
C . 溶液中 n(NH4+)=0.25mol
D . 三种离子的物质的量之比 n(H+):n(Al3+):n(Mg2+)=2:2:1
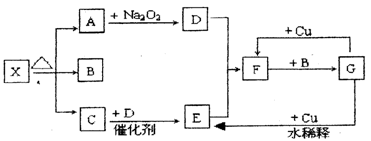
如图的各方框表示有关的一种反应物或生成物(某些物质已经略去),常温下A、C、D为无色气体,C能使湿润的红色石蕊试纸变蓝。
-
(1) 写出下列各物质的化学式:X:A:C:F:。
-
(2) 写出下列变化的化学方程式:
X
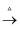 :;
:;C→E:;
F→G:;
-
(3) 检验X中阳离子的方法:。
根据下列实验操作和现象所得到的结论正确的是( )
| 选项 | 实验操作和现象 | 实验结论 |
| A | 向1mL1%的NaOH溶液中加入2mL 的CuSO4溶液, 振荡后再加入0.5mL有机物Y,加热,未出现砖红色沉淀 | Y中不含有醛基 |
| B | 将金属钠在燃烧匙中点燃,迅速伸入集满CO2的集气瓶,瓶中产生大量白烟和黑色颗粒 | CO2具有氧化性 |
| C | 加热盛有少量NH4HCO3固体的试管,并在试管口放置湿润的红色石蕊试纸,石蕊试纸变蓝 | NH4HCO3显碱性 |
| D | 向滴有酚酞的Na2CO3溶液中,逐滴加入BaCl2溶液,溶液红色逐渐褪去 | BaCl2溶液呈酸性 |
A . A
B . B
C . C
D . D
下列叙述中正确的是:( )
①NH3易液化,液氨常用作制冷剂
②可用铁、铝制容器盛装浓硝酸和浓硫酸
③利用氨气极易溶于水,氨气可做喷泉实验
④所有的氮氧化物均易溶于水
⑤铵盐受热分解一定都会产生氨气
⑥可用淀粉-KI试纸鉴别红棕色的Br2蒸气和NO2气体
A . ①③
B . ①②③
C . ①②③④
D . ①②③④⑤⑥
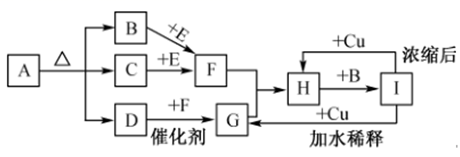
下图所涉及的物质均为中学化学中的常见物质,其中A为(NH4)2CO3 , 其受热分解得到的产物的物质的量比为2:1:1,D能使湿润的红色石蕊试纸变蓝,E为一种淡黄色的化合物,H为红棕色气体,I的浓溶液可在常温下用铝制容器盛装。它们存在如下转化关系,反应中的次要产物均已略去。
-
(1) 写出下列各物质的化学式:H、I。
-
(2) 请写出下列反应的化学方程式:
①C→F
②A受热分解:
-
(3) 请写出I→G的离子方程式:,当有2mol的G生成时反应转移的电子数为。
下列叙述正确的是( )
A . 蔗糖与浓硫酸反应有海绵状的炭生成,说明浓硫酸具有吸水性
B . 向饱和食盐水中通入过量 , 无明显现象;再通入
, 无明显现象;再通入 , 溶液变浑浊
C .
, 溶液变浑浊
C .  溶液可用于铜质印刷线路板制作是因为
溶液可用于铜质印刷线路板制作是因为 能从含
能从含 的溶液中置换出铜
D . 在足量的
的溶液中置换出铜
D . 在足量的 中灼烧
中灼烧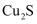 使之转化为CuO,反应后固体物质的质量不变
使之转化为CuO,反应后固体物质的质量不变
 , 无明显现象;再通入
, 无明显现象;再通入 , 溶液变浑浊
C .
, 溶液变浑浊
C .  溶液可用于铜质印刷线路板制作是因为
溶液可用于铜质印刷线路板制作是因为 能从含
能从含 的溶液中置换出铜
D . 在足量的
的溶液中置换出铜
D . 在足量的 中灼烧
中灼烧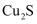 使之转化为CuO,反应后固体物质的质量不变
使之转化为CuO,反应后固体物质的质量不变
下列关于物质的性质叙述正确的是( )
A . 铵盐受热均会分解,但是产物不一定含有氨气
B . 浓硝酸见光易分解,所以保存在棕色广口瓶中
C . 二氧化硅是酸性氧化物,它不溶于任何酸
D . 浓硫酸在常温下可迅速与铜片反应放出二氧化硫气体
关于常见氮肥及其使用,下列说法中错误的是( )
A . 氮肥主要有铵态氮肥、硝态氮肥和尿素
B . 硝态氮肥宜在高温天气、多雨的水田使用
C . 铵态氮肥在使用时不可以跟碱性物质混合使用
D . 尿素是一种中性肥料,肥效高、易保存,对土壤的破坏作用小
下列说法中正确的是( )
A . 吸热反应一定需要加热才能反应,而放热反应在常温下一定能进行
B . 水银和生铁都属于纯金属
C . 用铂丝蘸取某碱金属的盐溶液灼烧,火焰呈黄色,证明其中含有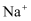 D . 某硫酸铵肥料中只含一种杂质,氮元素的质量分数为20%,可能混有硝酸铵
D . 某硫酸铵肥料中只含一种杂质,氮元素的质量分数为20%,可能混有硝酸铵
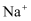 D . 某硫酸铵肥料中只含一种杂质,氮元素的质量分数为20%,可能混有硝酸铵
D . 某硫酸铵肥料中只含一种杂质,氮元素的质量分数为20%,可能混有硝酸铵
最近更新



