化学反应速率与化学平衡的综合应用 知识点题库
 2NH3(g)+CO2(g)。可以判断该分解反应已经达到化学平衡的是( )
2NH3(g)+CO2(g)。可以判断该分解反应已经达到化学平衡的是( )
 CO(g)+H2(g)。下列叙述中不能说明该反应已达到化学平衡状态的是()
CO(g)+H2(g)。下列叙述中不能说明该反应已达到化学平衡状态的是()
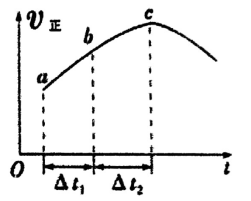
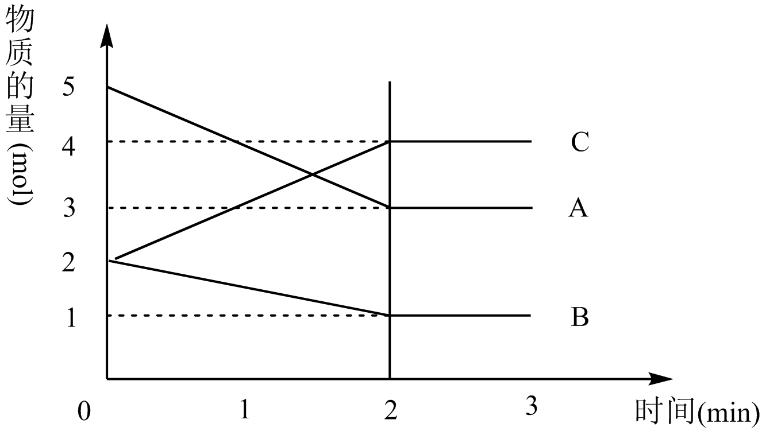
 2C(g),达到平衡后,在不同的时间段,分别改变反应的一个条件,测得容器中各物质的物质的量浓度、反应速率分别随时间的变化如图所示:
2C(g),达到平衡后,在不同的时间段,分别改变反应的一个条件,测得容器中各物质的物质的量浓度、反应速率分别随时间的变化如图所示: 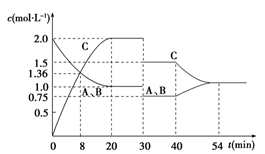
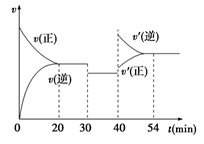
下列说法中正确的是()
-
(1) 反应的化学方程式用A、B、C可表示为。
-
(2) 用A表示在0~10min内的反应速率。
-
(3) 在该条件达到反应的限度时反应物B的转化率为。(计算结果用百分数表示,并保留1位小数)
-
(4) 开始时容器中的压强与平衡时的压强之比为。
 CO2(g)+H2(g)达到平衡,正反应速率随时间变化的曲线如图所示,由图可得出的结论正确的是( )
CO2(g)+H2(g)达到平衡,正反应速率随时间变化的曲线如图所示,由图可得出的结论正确的是( )
 2CO2(g)+N2(g) ΔH=-746.8 kJ·mol-1 ,可净化汽车尾气,如果要同时提高该反应的速率和NO的转化率,采取的措施是( )
2CO2(g)+N2(g) ΔH=-746.8 kJ·mol-1 ,可净化汽车尾气,如果要同时提高该反应的速率和NO的转化率,采取的措施是( )
 xC(g),△H<0;在2min时反应达到平衡状态(温度不变)剩余了0.8molB,并测得C的浓度为0.4mol·L—1 , 请填写下列空白:
xC(g),△H<0;在2min时反应达到平衡状态(温度不变)剩余了0.8molB,并测得C的浓度为0.4mol·L—1 , 请填写下列空白:
-
(1) 从开始反应至达到平衡状态,生成B的平均反应速率为。
-
(2) x=,平衡常数K=,A的转化率为。
-
(3) 若继续向原平衡混合物的容器中通入少量氦气(假设氦气和A、B、C都不反应)后,化学平衡(填字母)________________。A . 向正反应方向移动 B . 向逆反应方向移动 C . 不移动
-
(4) 如果上述反应在相同温度和容器中进行,欲使反应达到平衡时C的物质的量分数与原平衡相等,起始加入的三种物质的物质的量n(A)、n(B)、n(C)之间应该满足的关系式为。
-
(1) 已知:①N2(g)+O2(g)
 2NO(g) ΔH=+180.5kJ/mol;
2NO(g) ΔH=+180.5kJ/mol; ②CO的燃烧热为283.0kJ/mol。
则2NO(g)+2CO(g)
 N2(g)+2CO2(g) ΔH=kJ/mol。
N2(g)+2CO2(g) ΔH=kJ/mol。 -
(2) 在恒温、恒容条件下,将2.0mol NO和1.0mol CO充入一个容积为2L的密闭容器中发生上述反应,反应过程中部分物质的物质的量(n)变化如图所示。

①N2在0~9min内的平均反应速率v(N2)=mol/(L·min);
②第9min时氮气的产率为;
③第12min时改变的反应条件可能为(填字母代号);
A.升高温度 B.加入NO C.加催化剂 D.减小压强 E.降低温度
④若在第24min将NO与N2的浓度同时增加到原来的2倍,化学平衡移动(填“向正反应方向”、“逆反应方向”或“不”)。
-
(3) 若将反应容器改为恒温容积可变的恒压密闭容器,压强为P=3.0MPa,反应物加入的物质的量不变,达到平衡时CO的转化率为50%,该温度下此反应平衡常数Kp=。
反应I CH4(g)+H2O(g)  CO(g)+3H2(g) △H1=+206 kJ/mol
CO(g)+3H2(g) △H1=+206 kJ/mol
反应II CO(g)+H2O(g)  CO2(g)+H2(g) △H2=-41 kJ/mol
CO2(g)+H2(g) △H2=-41 kJ/mol
副反应 CH4(g)  C(s)+2H2(g) △H3=+75 kJ/mol
C(s)+2H2(g) △H3=+75 kJ/mol
-
(1) ①若仅发生反应I,为提高CH4的平衡转化率,宜采用的反应条件为。
A.高温高压 B.低温低压 C.高温低压 D.低温高压
②某研究小组在一定条件下往恒温恒容的密闭容器中通入一定量的甲烷和水蒸气,实验过程中发现CO2的产率远大于CO的产率,请解释可能的原因。
-
(2) 在实际生产过程中,科学家发现使用Ni作为催化剂(当Ni表面吸附大量碳时,会导致催化剂活性下降),可加快反应I的反应速率,从而加快整个反应的进行,提高单位时间内H2的产率。
①某恒容体系中,压强为1.3MPa,水/甲烷的物质的量之比为4,反应相同时间,H2的物质的量随反应温度的变化曲线如图所示。
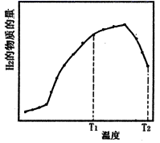
下列说法正确的是
A.对反应I而言,KT1>KT2
B.水/甲烷的物质的量之比等于4,大于初始反应的化学计量数之比,有利于促进CH4的转化,同时也有利于CO转化为CO2
C.使用Ni做催化剂,可增加活化分子百分数,从而加快反应速率,其主要原因是提高分子自身所具有的能量
D.若控制其他条件不变,缩小体积,则CH4的平衡转化率将减小
②在某恒温体系中,体积为1L,水/甲烷的物质的量之比等于4,投入CH4的量为1mol,若仅发生上述一系列反应,一段时间后,测得CH4的转化率为a,其中生成CO的选择性(转化的CH4中,生成CO的百分含量)为b,CO2的浓度为c mol/L,求此时H2的物质的量浓度为,CO的物质的量浓度为
-
(3) 现科学家发现,以Ni-CaO为复合催化剂能在一定程度上促进天然气重整反应的正向进行,使H2体积分数达到95%左右。请从能量利用及平衡移动角度,理论分析以Ni-CaO为复合催化剂的优点。
-
(4) CH4自身也可做为然料电池的原料,其工作原理如图所示。
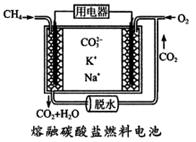
请写出通入甲烷-极的电极反应式为。
-
(1) Ⅰ.SO2+2H2O+I2=H2SO4+2HI;Ⅱ.2HI
 H2+I2 ;Ⅲ.2H2SO4=2SO2+O2+2H2O。
H2+I2 ;Ⅲ.2H2SO4=2SO2+O2+2H2O。 分析上述反应,下列判断正确的是。
a.反应Ⅲ易在常温下进行
b.反应Ⅰ中SO2氧化性比HI强
c.循环过程中需补充H2O
d.循环过程产生1 mol O2的同时产生1 mol H2
-
(2) 一定温度下,向1 L密闭容器中加入1 mol HI(g),发生反应Ⅱ,H2物质的量随时间的变化如图所示。0~2 min内的平均反应速率v(HI)=。该温度下,H2(g)+I2(g)
 2HI(g)的平衡常数K=。相同温度下,若开始加入HI(g)的物质的量是原来的2倍,则是原来的2倍。
2HI(g)的平衡常数K=。相同温度下,若开始加入HI(g)的物质的量是原来的2倍,则是原来的2倍。 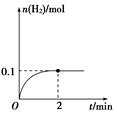
a.平衡常数
b.HI的平衡浓度
c.达到平衡的时间
d.平衡时H2的体积分数
-
(3) 实验室用Zn和稀硫酸制取H2 , 反应时溶液中水的电离平衡移动(填“向左”“向右”或“不”);若加入少量下列试剂中的,产生H2的速率将增大。
a.NaNO3 b.CuSO4
c.Na2SO4 d.NaHSO3
|
时间/s |
0 |
1 |
2 |
3 |
4 |
5 |
|
n(CO)/mol |
0.40 |
0.35 |
0.31 |
0.30 |
0. 30 |
0.30 |
回答下列问题:
-
(1) 0~2 s内用N2表示的反应速率是。
-
(2) 平衡时CO2的物质的量浓度为。
-
(3) 能说明反应已达到平衡状态的是________(填标号)。A . n(CO2)=n(NO) B . n(CO2)=n(CO) C .
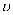 逆(CO)=
逆(CO)= 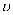 正(CO)
正(CO)

回答下列问题:
-
(1) “浸泡”过程中,钴(III)可转化为CoSO4 , 写出该转化的化学方程式:。
-
(2) “除铜”若选用MnS,计算常温下该“除铜”反应的平衡常数K=。[保留2位有效数字;已知常温下Ksp(MnS)=2.5×10–13 , Ksp(CuS)=1.3×10–36]
-
(3) ①步骤I中加入NaClO3反应的离子方程式为。
②常温下,溶液中金属离子(Mn+)的pM[pM=–lgc(Mn+)]随溶液pH变化关系如图所示,设加入NaClO3后,溶液中的c(CO2+)为0.1mol•L–1 , 依据如图分析,步骤I中加入Na2CO3调整溶液pH范围为。[当c(Mn+)≤10–6 mol•L–1 , 即认为该金属离子沉淀完全]
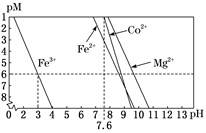
-
(4) 步骤II中加入足量NaF的目的是。
-
(5) 过滤出的CoC2O4•2H2O固体经洗涤后,证明固体已洗净的操作为。
-
(6) 若某工厂用m1kg该铜钴矿石制备了m2kgCo2O3 , 假设产率为a,则该矿石中钴元素的百分含量为。
 、
、  、
、  等是对环境影响较大的几种气体,对它们的合理控制和治理是优化我们生存环境的有效途径。
等是对环境影响较大的几种气体,对它们的合理控制和治理是优化我们生存环境的有效途径。
-
(1) 二甲醚(
 )被誉为“21世纪的清洁燃料”,由
)被誉为“21世纪的清洁燃料”,由  和
和  制备二甲醚的反应原理如下:
制备二甲醚的反应原理如下: 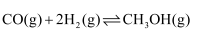
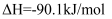

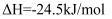
已知:

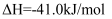
则
 的
的  。
。 -
(2) 200℃,在2L的密闭容器中充入
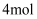
 和
和 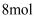
 ,发生反应
,发生反应 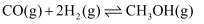 (I);
(I); 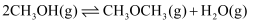 (II),
(II), 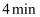 达到平衡,平衡时
达到平衡,平衡时  的转化率为80%,且
的转化率为80%,且 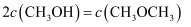 ,则:
,则: ①
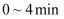 内,反应(Ⅰ)平均反应速率
内,反应(Ⅰ)平均反应速率  。
。②反应(Ⅱ)中
 的转化率
的转化率  。
。 -
(3) 利用电化学原理将
 、
、  转化为重要化工原料,装置如图所示:
转化为重要化工原料,装置如图所示: 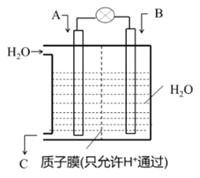
①若A为
 ,B为
,B为  ,C为
,C为  ,则通入
,则通入  一极的电极反应式为。
一极的电极反应式为。②若A为
 ,B为
,B为  ,C为
,C为  ,则负极的电极反应式为。
,则负极的电极反应式为。
| 容器 | 温度(T1>T2) | 起始时物质的量/mol | 平衡时物质的量/mol | |||
| n(Si) | n(HCl) | n(SiCl4) | n(H2) | n(H2) | ||
| Ⅰ | T1 | 0.8 | 0.4 | 0 | 0 | 0.1 |
| Ⅱ | T1 | 0.8 | 0.8 | 0 | 0 | x |
| Ⅲ | T2 | 0 | 0 | 0.1 | 0.2 | y |

 ,一段时间后反应达到平衡,测得有关数据如表所示:
,一段时间后反应达到平衡,测得有关数据如表所示: | | 2 | 4 | 7 | 9 |
| | 0.12 | 0.11 | 0.10 | 0.10 |
下列说法正确的是( )
 B . 其他条件不变,降低温度,反应达到新平衡前
B . 其他条件不变,降低温度,反应达到新平衡前  C . 其他条件不变,起始时向容器中充入0.32 mol气体X和0.32 mol气体Y,达到平衡时,
C . 其他条件不变,起始时向容器中充入0.32 mol气体X和0.32 mol气体Y,达到平衡时, 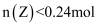 D . 其他条件不变,向平衡体系中再充入0.16 mol气体X,达到新平衡时,气体Y的转化率增大
D . 其他条件不变,向平衡体系中再充入0.16 mol气体X,达到新平衡时,气体Y的转化率增大
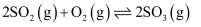 △H=-196.6 kJ/mol,达到平衡,生成1.6 mol SO3并放出热量157.28 kJ。
△H=-196.6 kJ/mol,达到平衡,生成1.6 mol SO3并放出热量157.28 kJ。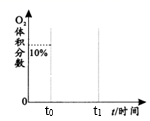
-
(1) 平衡时SO2转化率为;t0时向上述平衡后的容器中再充入a mol SO2 ,
 时重新达到平衡。请在图中用曲线表示出t0后O2的体积分数随时间变化的大致趋势。
时重新达到平衡。请在图中用曲线表示出t0后O2的体积分数随时间变化的大致趋势。
-
(2) T0℃,向另一容积相等的恒压容器中充入2 mol SO2和1 mol O2 , 平衡时放出的热量(填“>”、“<”或“=”) 157.28 kJ;若平衡时升高温度,平衡移动(填“正向”或“逆向”或“不”),该反应的平衡常数(填“增大”或“减小”或“不变”);若测得T1℃平衡时该容器内气体压强为2 MPa,SO3体积分数为70%,计算该温度时反应的平衡常数Kp=
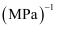 (列出计算式,以分压表示,分压=总压×物质的量分数。)
(列出计算式,以分压表示,分压=总压×物质的量分数。)
 CO(g)+3H2(g) ΔH>0,每次只改变一种条件(X), 其它条件不变,CH4 的平衡转化率 φ 随 X 的变化趋势如图所示。下列说法正确的是( )
CO(g)+3H2(g) ΔH>0,每次只改变一种条件(X), 其它条件不变,CH4 的平衡转化率 φ 随 X 的变化趋势如图所示。下列说法正确的是( )
 ]时,φ 的变化趋势为曲线 M
D . 某条件下,若 CH4(g)、H2O(g)初始浓度均为 0.2mol/L,φ=25%,则 K=
]时,φ 的变化趋势为曲线 M
D . 某条件下,若 CH4(g)、H2O(g)初始浓度均为 0.2mol/L,φ=25%,则 K=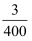
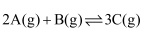
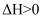 K正。某研究小组研究了在其他条件不变时,改变某一条件对上述反应的影响,下列分析正确的是( )
K正。某研究小组研究了在其他条件不变时,改变某一条件对上述反应的影响,下列分析正确的是( )
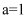
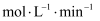 B . 该反应的化学方程式为
B . 该反应的化学方程式为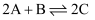 C . 充入He,体系压强增大,反应速率加快
D . 平衡时,A的转化率为40%
C . 充入He,体系压强增大,反应速率加快
D . 平衡时,A的转化率为40%
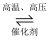
 。请回答下列问题。
。请回答下列问题。
-
(1) 已知:
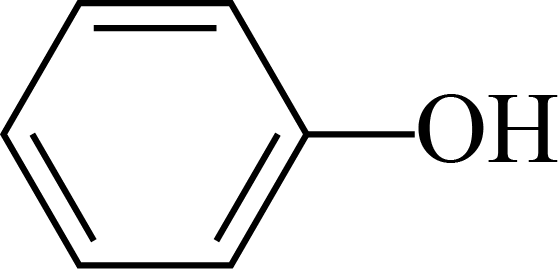

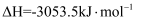 ;
;

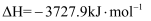 ;
;
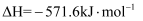 。
。则
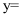 。
。 -
(2) 向体积为50L的恒容密闭容器中充入一定量的
 (g)和
(g)和 不同温度下,反应均进行5min测得反应物的转化率随温度的变化关系如图所示,已知曲线Ⅰ表示苯酚的转化率)。
不同温度下,反应均进行5min测得反应物的转化率随温度的变化关系如图所示,已知曲线Ⅰ表示苯酚的转化率)。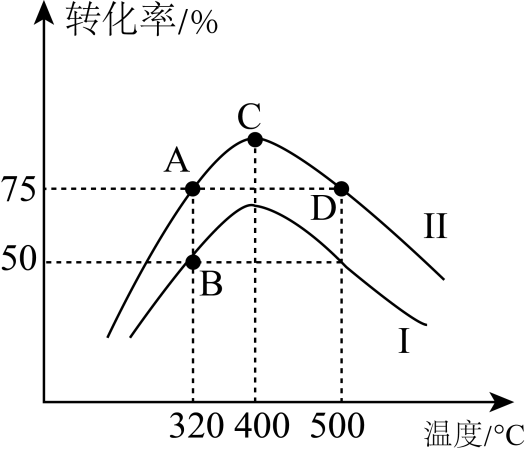
①起始时投入的苯酚和氢气的物质的量之比为。
②A、B、C、D四点对应的正反应速率
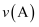 、
、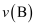 、
、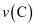 、
、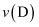 的大小关系为。
的大小关系为。③温度低于400℃时,
 和苯酚的转化率随温度升高而增大的原因是。
和苯酚的转化率随温度升高而增大的原因是。④已知
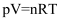 , V代表体积;n代表气体物质的量;T代表温度;R是摩尔气体常数,单位是
, V代表体积;n代表气体物质的量;T代表温度;R是摩尔气体常数,单位是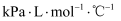 。若初始时向容器中充入的苯酚为1mol,则反应从起始进行到A点,其平均反应速率
。若初始时向容器中充入的苯酚为1mol,则反应从起始进行到A点,其平均反应速率 ;当反应温度为500℃时,反应达到平衡后,
;当反应温度为500℃时,反应达到平衡后,
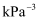 。(
。( 表示用分压代替浓度计算的平衡常数,结果用含R的代数式表示)
表示用分压代替浓度计算的平衡常数,结果用含R的代数式表示) -
(3) 氢原子和苯分子吸附在金属催化剂表面活性中心时,才能发生反应。当
 中混有微量
中混有微量 杂质时,相同时间内测得环已醇的产率降低。推测其可能原因为。
杂质时,相同时间内测得环已醇的产率降低。推测其可能原因为。