铵离子检验 知识点
铵离子检验 知识点题库
选项 | 实验操作 | 实验现象 | 结论 |
A | 向某溶液中滴加稀NaOH溶液,将湿润红色石蕊试纸置于试管口 | 试纸不变蓝 | 原溶液中无NH4+ |
B | 将少量的溴水滴入FeCl2、NaI的混合溶液中,在滴加CCl4 , 振荡、静置,向上层溶液中滴加KSCN溶液.再向上层溶液中滴加溴水 | 实验现象1: 上层溶液不变红 下层溶液紫色红 实验现象2: 上层溶液变红 | 氧化性:Br2>Fe3+>I2 |
C | 淀粉在稀硫酸的作用下水解后,滴加NaOH溶液至碱性,再加入新制Cu(OH)2后加热 | 有砖红色沉淀生成 | 淀粉已经完全水解 |
D | BaSO4固体加入饱和Na2CO3溶液中,过滤,箱滤渣中加入盐酸 | 有气体生成 | Ksp(BaCO3)<Ksp(BaSO4) |
⑴第一份加入足量的烧碱并加热,产生气体在标准状况下的体积为224mL。
⑵第二份先加入足量的盐酸,无现象,再加入足量的BaCl2溶液,过滤,得固体2.33g。
⑶在(2)的滤液中滴入AgNO3 , 产生白色沉淀,加稀硝酸,沉淀不溶解。
下列说法正确的是( )
| 操作 | 现象 | 结论 | |
| A | 先滴加BaCl2溶液,再加稀HNO3 | 生成白色沉淀,且沉淀不溶解 | 原溶液中有SO42﹣ |
| B | 滴加氯水和CCl4 , 振荡、静置 | 下层溶液显紫红色 | 原溶液中有I﹣ |
| C | 用洁净铂丝蘸取溶液进行焰色反应 | 火焰呈黄色 | 原溶液中有Na+、K+ |
| D | 滴加NaOH溶液加热,将红色石蕊试纸置于试管口 | 试纸不变蓝 | 原溶液中无NH4+ |
| 选项 | 实验 | 现象 | 结论 |
| A | 向FeBr2溶液中加入少量氯水,再加CCl4振荡 | CCl4层无色 | Fe2+的还原性强于Br- |
| B | 向盐酸中滴入少量NaAlO2溶液 | 无明显现象 | AlO2-与H+未发生反应 |
| C | 向某溶液里滴加NaOH溶液并将湿润的红色石蕊试纸置于试管口 | 试纸颜色无明显变化 | 原溶液中无NH4+ |
| D | 向某溶液中滴加KSCN溶液 | 溶液未变血红色 | 溶液中不含铁元素 |
| | | | |
| A.在某溶液中加入盐酸后无现象,再加BaCl2产生白色沉淀证明有SO42- | B.样品中加NaOH溶液加热,蓝色石蕊试纸变红,证明检验样品中有NH4+的存在 | C.将混有少量氯化钾的硝酸钾饱和溶液在冰水中冷却,KNO3晶体先析出 | D.将灼热的铜丝伸入盛有氯气的集气瓶中,铜丝剧烈燃烧,产生棕黄色的烟 |
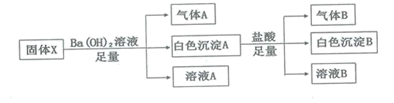
下列说法正确的是( )
| 选项 | 操作 | 现象 | 解释或结论 |
| A | 向某无色溶液中加入足量稀盐酸酸化的Ba(NO3)2溶液 | 出现白色沉淀 | 溶液中一定存在 |
| B | 用光照射装有甲烷和氯气的混合气体气体的试管 | 颜色逐渐变浅,试管内壁出现油状液滴 | 甲烷与氯气发生了反应 |
| C | 向蔗糖溶液中加3~5滴稀硫酸,将混合液煮沸几分钟,冷却;向冷却后的溶液中加入银氨溶液,水浴加热 | 没有银镜产生 | 蔗糖未发生水解 |
| D | 向盛有某溶液的试管中滴加稀NaOH溶液,将湿润红色石荔试纸置于试管口 | 试纸不变蓝 | 原溶液中无 |
-
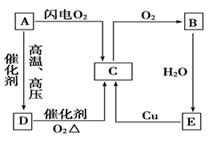
(1) 除去C中的B所用的试剂为
-
(2) 写出A的电子式
-
(3) 检验试管中盛装的是D的方法为
-
(4) E→C的离子方程式
-
(5) 写出实验室制备D的化学方程式
| 选项 | 实验操作 | 结论 |
| A | 溶液X的焰色反应呈黄色 | X中含 |
| B | 向固体Y中加入稀盐酸,有无色气体生成 | Y一定是碳酸盐 |
| C | 向固体Z中加入盐酸酸化的 | Z一定含有 |
| D | 向固体W中加入浓 | W一定含有 |
①铵根离子水解显酸性;②  与
与 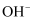 间发生反应加热后产生氨气;③
间发生反应加热后产生氨气;③  能电离出
能电离出  和
和 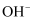 ;④石蕊在碱性条件下变为蓝色
;④石蕊在碱性条件下变为蓝色
 的流程如下:
的流程如下:
-
(1) 粗盐中含有大量的NaCl,以及少量的
 、
、 、
、 等离子。为得到纯净的饱和NaCl溶液,对粗盐溶液进行了如下操作。下列操作步骤排序不合理的是____(填正确答案标号)
等离子。为得到纯净的饱和NaCl溶液,对粗盐溶液进行了如下操作。下列操作步骤排序不合理的是____(填正确答案标号)a.加入过量的氢氧化钠溶液;
b.加入过量的碳酸钠溶液;
c.加入过量的氯化钡溶液;
d.加入足量的稀盐酸;
e.过滤;
f.加热煮沸一段时间,得到饱和NaCl溶液。
A . acbedf B . cabedf C . acbdef D . cbaedf -
(2) 向“饱和NaCl溶液”通入
 和
和 的顺序是先通入,后通入。
的顺序是先通入,后通入。
-
(3) 过滤用到的玻璃仪器除烧杯和玻璃棒外,还需要。
-
(4) 反应Ⅰ的化学方程式为。
-
(5) 纯碱和小苏打都是白色固体,下列区分这两种物质的方法正确的是____。(填正确答案标号)A . 分别用炒锅加热两种样品,全部分解挥发,没有残留物的是小苏打 B . 用洁净铁丝蘸取两种样品在煤气火焰上灼烧,使火焰颜色发生明显变化的是小苏打 C . 用两只小玻璃杯,分别加入等量的两种样品,再逐滴加入食醋,产生气泡快的是小苏打 D . 先将两种样品配成溶液,分别加入足量石灰水,无白色沉淀生成的是小苏打
-
(6) “过滤”后的母液中最主要的成分是 (填写化学式)。检验这一成分中的阳离子的具体方法是。
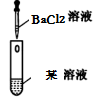

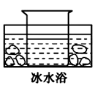
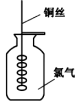


 不含
不含 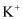
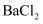 溶液,有白色沉淀
溶液,有白色沉淀 溶液,产生的气体能使湿润的红色石蕊试纸变蓝
溶液,产生的气体能使湿润的红色石蕊试纸变蓝


