海水资源及其综合利用 知识点
海水资源及其综合利用 知识点题库
①将海带焙烧成灰(生成KI) ②加水使KI溶解,充分搅拌后过滤 ③在滤液通入足量Cl2④加CCl4振荡⑤静置后,用分液漏斗分液 合理的操作顺序是.
选项 | 叙述I | 叙述II |
A | H2有还原性,浓硫酸有强氧化性 | 不能用浓硫酸干燥H2 |
B | CuS难溶于水和硫酸 | 反应:H2S+CuSO4=CuS↓+H2SO4 可以发生 |
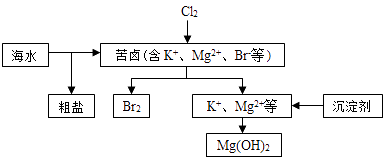
C | 海水中含有大量的Cl﹣、Br﹣等离子 | 向海水中通入F2可大量获得Cl2、Br2 |
D | SO2具有酸性和漂白性 | 往紫色石蕊溶液中通入SO2 , 溶液先变红再褪色 |
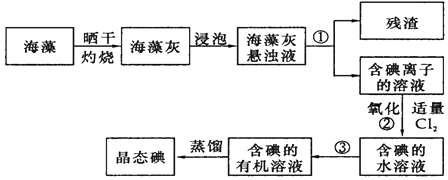
指出提取碘的过程中有关实验操作名称:①,③;写出过程②中有关反应的离子方程式.
-
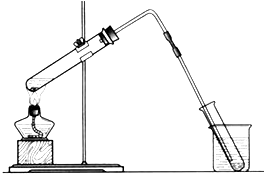
(1) 如图是用海水制取少量蒸馏水的简易装置,其原理与课本中的实验原理完全相同.装置中使用了较长的玻璃管,其作用是,烧杯中还应盛装的物质是.
-
(2) 海带中含有丰富的碘,海带提碘可将海带灼烧、溶解、煮沸、过滤得含I﹣的滤液,滤液经酸化、氧化得含单质碘的溶液.回答下列问题:
①海带灼烧时用来盛装海带的仪器是(填仪器名称)
②已知KMnO4、H2O2、Cl2等均可与I﹣反应生成I2 , 且KMnO4、H2O2、Cl2对应的生成物分别为Mn2+、H2O、Cl﹣ . 从绿色化学的角度看I﹣转化成I2 , 最好选 (上述三种中选择)
-
(3) 海水晒盐得到的盐含有较多的杂质.某学习小组欲设计实验提纯粗盐.
①若只除去其中的不溶性杂质,应经过的实验步骤是、、.
②若要进一步除去上述粗盐中的可溶性杂质,应选择合理的除杂试剂.请填写表:
杂质
CaCl2
MgCl2
Na2SO4
除杂试剂
③为确保杂质除尽,所加试剂应适当过量.如何判断SO42﹣是否除尽?
④上述除杂试剂加入的先后顺序应满足的一般条件是
⑤按顺序加入上述除杂试剂过滤后,还应加入适量稀HCl,其目的是,判断加入稀HCl适量的方法可以是.
A.把盛有溶液的分液漏斗放在铁架台的铁圈中;
B.把50mL碘水和15mL CCl4 加入分液漏斗中,并盖好玻璃塞;
C.倒转漏斗用力振荡,并不时旋开活塞放气,最后关闭活塞,把分液漏斗放正;
D.检验分液漏斗活塞和上口的玻璃塞是否漏液;
E.静置,分层;
F.从分液漏斗上口倒出上层水溶液;
G.将漏斗上口的玻璃塞打开或使塞上的凹槽(或小孔)对准漏斗口上的小孔;
H.旋开活塞,用烧杯接收溶液.
就此实验,完成下列填空:
-
(1) 正确操作步骤的顺序是:(用上述各操作的编号字母填写)
→→→A→G→→H→F.
-
(2) 上述H步骤的操作中应注意.上述G步骤操作的目的是.
-
(3) 四氯化碳是色、密度比水的密度的液体.E中下层液体的颜色为色.
-
(4) 能选用CCl4从碘水中萃取碘的原因是.

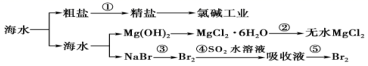
回答下列问题:
-
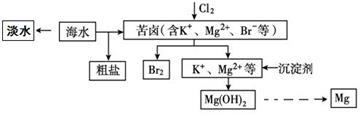
(1) NaCl 溶液由粗盐水精制而成,为除去Ca2+和Mg2+ , 要加入的试剂分别为、。
-
(2) 写出步骤Ⅰ 中反应的总化学方程式为NaCl+═NaClO3+。
-
(3) 已知MgCl2 溶液受热时易水解(和水反应)生成Mg(OH)Cl,写出该过程的化学方程式。
-
(4) 步骤Ⅳ中,电解熔融MgCl2 得到的镁需要在保护气中冷却,下列气体可以作为保护气的是_______________。A . N2 B . H2 C . CO2 D . 空气
 Mg(OH)2
Mg(OH)2  Mg
B . 海水
Mg
B . 海水  MgCl2溶液
MgCl2溶液  MgCl2熔融
MgCl2熔融  Mg
C . 海水
Mg
C . 海水 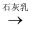 Mg(OH)2
Mg(OH)2  MgO
MgO  Mg
D . 海水
Mg
D . 海水 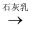 Mg(OH)2
Mg(OH)2  MgCl2溶液
MgCl2溶液  MgCl2熔融
MgCl2熔融  Mg
Mg

苦卤水 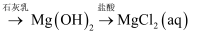

下列说法正确的是( )
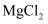 在阴极可得Mg
B . 将
在阴极可得Mg
B . 将 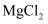 溶液蒸干可得无水
溶液蒸干可得无水 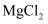 C . 反应
C . 反应 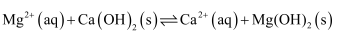 的
的  D . 常温下,
D . 常温下, 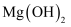 溶于盐酸所得
溶于盐酸所得 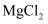 溶液中
溶液中 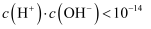
-
(1) 小组1:收集了500ml奉贤海湾的海水,在实验室中提取粗盐,并检验杂质离子。
该小组将100.00ml海水样品蒸发结晶,得到乳白色粗盐晶体m1g,若要检验该粗盐中是否含有硫酸根离子,方法是。取一半该粗盐,若将SO
 转化成硫酸钡沉淀,如何判断SO
转化成硫酸钡沉淀,如何判断SO 已沉淀完全;洗涤干燥后,称量得到0.0233g沉淀,则该海水中SO
已沉淀完全;洗涤干燥后,称量得到0.0233g沉淀,则该海水中SO 的含量为mol/L,若未洗涤,则测得结果(填“偏大”、“偏小”或“无影响”)。
的含量为mol/L,若未洗涤,则测得结果(填“偏大”、“偏小”或“无影响”)。 -
(2) 小组2:将小组1所得粗盐的一半进行精制,除去杂质离子Ca2+、Mg2+和SO
 , 操作流程如下:
, 操作流程如下: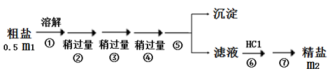
步骤⑤操作中用到的玻璃仪器有,实验过程中多次产生沉淀,共需要过滤次。若m2=1.346g,据此能否计算该海水样品中的氯化钠的物质的量浓度?若能,请写出计算结果;若不能,请解释原因:。
-
(3) 小组3:利用小组2得到精盐的水溶液及铅笔、饮料瓶、电池等自制84消毒液。
请对比该小组设计的两种制备装置甲和乙,你认为哪种装置更好,请说明理由。




