зҰ»еӯҗй”®зҡ„еҪўжҲҗ зҹҘиҜҶзӮ№йўҳеә“
в‘ иҙЁеӯҗж•°зӣёеҗҢзҡ„еҫ®зІ’дёҖе®ҡеұһдәҺеҗҢдёҖз§Қе…ғзҙ
в‘Ўе…ұд»·еҢ–еҗҲзү©дёӯдёҚеӯҳеңЁзҰ»еӯҗй”®
в‘ўиҙЁеӯҗж•°зӣёеҗҢпјҢз”өеӯҗж•°д№ҹзӣёеҗҢзҡ„дёӨз§Қеҫ®зІ’пјҢдёҚеҸҜиғҪжҳҜдёҖз§ҚеҲҶеӯҗе’ҢдёҖз§ҚзҰ»еӯҗ
в‘Јз”өеӯҗж•°зӣёеҗҢзҡ„еҫ®зІ’дёҚдёҖе®ҡжҳҜеҗҢдёҖз§Қе…ғзҙ
в‘ӨйқһйҮ‘еұһе…ғзҙ д№Ӣй—ҙдёҚеҸҜиғҪеҪўжҲҗзҰ»еӯҗй”®
в‘ҘзҰ»еӯҗй”®жҳҜжҢҮйҳҙйҳізҰ»еӯҗй—ҙзҡ„йқҷз”өеҗёеј•еҠӣ
в‘Ұж°ҙеҸ—зғӯдёҚе®№жҳ“еҲҶи§ЈпјҢеҺҹеӣ жҳҜж°ҙеҲҶеӯҗй—ҙеӯҳеңЁж°ўй”®
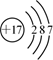 B .
B . в‘ еҢ–еӯҰй”®жҳҜеҸҜд»ҘдҪҝзҰ»еӯҗзӣёз»“еҗҲпјҢд№ҹеҸҜд»ҘдҪҝеҺҹеӯҗзӣёз»“еҗҲзҡ„дҪңз”ЁеҠӣ в‘ЎеҸӘеҗ«е…ұд»·й”®зҡ„зү©иҙЁдёҖе®ҡжҳҜе…ұд»·еҢ–еҗҲзү© в‘ў 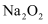 дёӯеҗ«жңүзҰ»еӯҗй”®е’ҢйқһжһҒжҖ§й”® в‘ЈзҰ»еӯҗеҢ–еҗҲзү©дёҺе…ұд»·еҢ–еҗҲзү©зҡ„еҢәеҲ«еҸҜд»ҘзңӢжҳҜеҗҰжңүйҮ‘еұһе…ғзҙ
дёӯеҗ«жңүзҰ»еӯҗй”®е’ҢйқһжһҒжҖ§й”® в‘ЈзҰ»еӯҗеҢ–еҗҲзү©дёҺе…ұд»·еҢ–еҗҲзү©зҡ„еҢәеҲ«еҸҜд»ҘзңӢжҳҜеҗҰжңүйҮ‘еұһе…ғзҙ
в‘ еңЁж°ҙдёӯж°ўгҖҒж°§еҺҹеӯҗй—ҙеқҮд»ҘеҢ–еӯҰй”®зӣёз»“еҗҲ в‘ЎжүҖжңүйҮ‘еұһе’ҢйқһйҮ‘еұһеҢ–еҗҲеҪўжҲҗзҰ»еӯҗй”® в‘ўзҰ»еӯҗй”®жҳҜйҳізҰ»еӯҗгҖҒйҳҙзҰ»еӯҗзҡ„зӣёдә’еҗёеј• в‘ЈдёӨдёӘйқһйҮ‘еұһеҺҹеӯҗй—ҙдёҚеҸҜиғҪеҪўжҲҗзҰ»еӯҗй”® в‘ӨйқһйҮ‘еұһеҺҹеӯҗй—ҙдёҚеҸҜиғҪеҪўжҲҗзҰ»еӯҗй”® в‘ҘзҰ»еӯҗеҢ–еҗҲзү©дёӯеҸҜиғҪжңүе…ұд»·й”® в‘Ұе…ұд»·еҢ–еҗҲзү©дёӯдёҚеҸҜиғҪжңүзҰ»еӯҗй”®



