癌症的预防与治疗 知识点题库
VK2/(μmol•L﹣1) | 0 | 10 | 20 | 30 | 40 |
细胞凋亡率/% | 3.15 | 6.37 | 14.70 | 19.31 | 26.42 |
下列叙述中,最合理的是( )
(1)为验证该酶对上述两种细胞的影响,某兴趣小组进行了以下实验.
实验材料:正常细胞、淋巴瘤细胞、L﹣天冬酰胺酶、培养基(含细胞生长所需物质)等
实验步骤:
实验组:培养基+L﹣天冬酰胺酶+淋巴瘤细胞
对照组:培养基+
两个组在相同且适宜条件下培养后,观察细胞生长状况,检测L﹣天冬酰胺含量.实验结果(如下):
实验分组 | 生长状况 | L﹣天冬酰胺含量 | |
培养基中 | 细胞内 | ||
实验组 | 抑制 | 缺乏 | 缺乏 |
对照组 | ? | 缺乏 | 正常 |
结果分析:
对照组细胞生长状况为 ,细胞内L﹣天冬酰胺含量正常的原因是 .两个组的细胞应保持大小相当、活力相同、 .
(2)患者多次静脉注射外源性L﹣天冬酰胺酶后疗效降低,经检测,在患者的血液发现了抗体与L﹣天冬酰胺酶结合物,说明患者产生了 免疫.
(3)L﹣天冬酰胺酶口服无疗效.兴趣小组依据上述研究结果设计了如下方案进行验证.
实验组:
步骤一:向2ml的L﹣天冬酰胺酶溶液加入2ml 溶液(甲液),将混合液(a液)pH调至1.5左右,37℃水浴保温10min;向a液加入4ml胰蛋白酶溶液(乙液),将混合液(b液)pH调至8左右,37℃水浴保温20min;
步骤二:向b液中加入含量为A的L﹣天冬酰胺,将混合液(c液)PH调至8左右,37℃水浴保温20min,检测c液中L﹣天冬酰胺的含量为B.
对照组:设置情况是 ;步骤二检测L﹣天冬酰胺的含量为C.
预期结果:若L﹣天冬酰胺的含量情况为 时,证明L﹣天冬酰胺酶口服无疗效.
实验材料:肝部长有肿瘤的小鼠,二氯二乙胺溶液,蒸馏水,生理盐水,含有全部营养物质的细胞培养液,显微镜,血球计数板,试管,吸管等.
-
(1) 其中某位同学的实验操作如下:(请将实验内容补充完整)
①取洁净的培养皿一个,加入适量的培养液,从小鼠肝部切取肿瘤组织,剪碎,并用处理,使其分散开来,置于培养皿中培养.
②取洁净的试管5支,加入等量的培养液,编号1,2,3,4,5,并在1~4号试管中加入等量的不同浓度的二氯二乙胺溶液,5号试管中加入 .
③从培养皿中吸取等量的培养液置于1﹣5号试管中,振荡后,在冰箱中培养一段时间.
④从静置的5支试管中吸取适量的培养液置于血球计数板内,在显微镜下计数,记录数据.
-
(2) 请你纠正上面这位同学操作上的错误
①;
② .
-
(3) 另一位同学按照正确的方法进行实验,得到的结果如下:
实验组别
1
2
3
4
5
二氯二乙胺浓度(mg/mL)
0.1
0.2
0.3
0.4
0
细胞数目(个/mL)
320
275
186
96
560
根据实验结果,你能得出的结论是 .
苦马豆素(SW)是从灰苦马豆中分离出来而得名,被认为是“未来的肿瘤治疗药物”.以下是相关的实验研究过程及结果:
①将等量的小鼠肝癌Hepal﹣6细胞悬液,分别接种于若干支含等量培养液的培养瓶中.
②将培养瓶放于37℃、5%CO2培养箱中培养24h,静置、去除上清液;
③分别加入等量但含不同浓度SW的培养液,于37℃、5%CO2培养箱中继续培养;
④分别在24h、48h、72h时吸取培养液,观察结果,得到不同浓度SW对细胞存活率影响曲线(如图).

请回答:
-
(1) 处于间期的肝癌Hepal﹣6细胞,其分子水平的主要变化是.
-
(2) ③实验要设置对照组,对照组的处理方法应为.步骤③中每个实验组设置5个培养瓶同时进行培养,计数后统计,这是为了,使实验结果更可信.
-
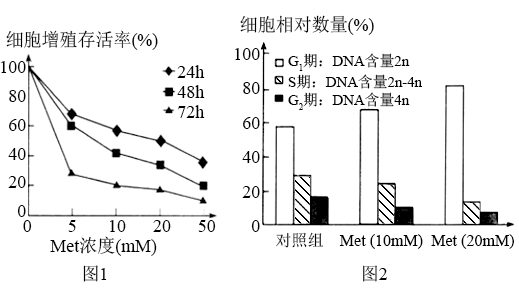
(3) 分析图1中曲线可知,SW对肝癌Hepal﹣6细胞作用效果的特点是:
①,对细胞生长(存活)的抑制作用越强;
②,对细胞生长(存活)的抑制作用越强.
-
(4) 将培养48h的培养液离心,去除上清液后经过一系列的处理及分析,得到下表结果:
表:培养48h细胞数目及凋亡蛋白Bax和Bcl﹣2的表达量
SW
癌细胞数目
凋亡细胞数目
Bax蛋白
Bcl﹣2蛋白
2微克/mL
+
++++
++++
+
1微克/mL
++
+++
+++
++
0.5微克/mL
+++
++
++
+++
0微克/mL
++++
+
+
++++
注:“+”的数量表示相对值的多少
据此推测,SW可能是通过诱发癌细胞来抑制肿瘤生长的,其原因可能是SW促进了癌细胞内基因的表达.

-
(1) 在工蜂毒腺细胞的核糖体上,蜂毒素是以为模板合成的。
-
(2) 在适宜的条件下进行体外培养,癌细胞能够,在此过程中细胞内的DNA含量将持续出现周期性的变化。如图表示癌细胞在一定浓度的蜂毒素培养液中培养几小时后,DNA含量不同的细胞数。据此推测,蜂毒素能将癌细胞阻断在有丝分裂的期。
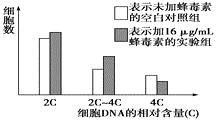
-
(3) 研究表明,阻断癌细胞增殖周期可引起细胞凋亡。科研人员为研究蜂毒素对人胃癌细胞的影响及作用机制,进行了以下实验。请完善实验并回答问题。
①方法步骤:
a.取4只相同的培养瓶,编号,分别加入等量的完全培养液并接种等量的离体胃癌细胞。
b.1号培养瓶为空白对照,向2~4号培养瓶中分别加入μg/mL蜂毒素溶液。
c.培养48 h后,检测并统计,结果如图甲所示。
d.重复a、b步骤,检测凋亡基因(Bax、Bel-2)的表达,结果如图乙所示。
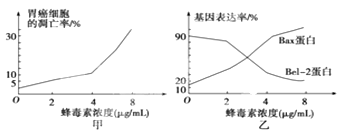
②分析讨论:
a.图甲表明。
b.图甲、图乙表明:从基因水平上看,蜂毒素诱导胃癌细胞凋亡与有关。当Bel2蛋白/Bax蛋白的比值出现趋势时,将会诱导胃癌细胞凋亡。

-
(1) 细胞自噬现象最早发现于酵母菌中。酵母菌液泡内富含水解酶,科学家在研究液泡与自噬的关系时,以野生型酵母菌为对照组,以液泡水解酶缺陷型酵母菌为实验组,在饥饿状态下,酵母菌液泡中出现自噬体大量堆积的现象。
-
(2) 当细胞中的线粒体受损后,由的无核糖体附着区脱落的双层膜包裹形成自噬体,随后自噬体与溶酶体融合,最终被降解。受损的线粒体功能逐渐退化,会直接影响有氧呼吸的第二、三阶段。细胞及时清除受损线粒体的意义是。
-
(3) 细胞内受损蛋白质可与热休克蛋白形成复合物,与溶酶体膜上的结合,并在其作用下转入溶酶体腔被降解;细胞自噬后的降解产物,一部分以代谢废物的形式排出细胞外,另一部分。据研究,癌细胞中热休克蛋白比正常细胞内的含量多,据图推测癌细胞能在营养条件较为恶劣环境下存活的原因可能是。基于上述原理,请提出治疗癌症的思路。(答出一项即可)。

-
(1) 分裂间期为分裂期提供物质准备,主要完成DNA分子复制和的合成,同时细胞体积。
-
(2) 检测点B为DNA损伤检测点,可感受DNA损伤的信息,并启动细胞在相关酶的作用下以为原料对损伤的DNA加以修复,或者激发引起细胞凋亡。
-
(3) 检测点D为染色体复制是否完成检测点。若检测到细胞能进入M期,但此时染色体数目没有变化的原因是。
-
(4) 放射治疗癌症前用药物使癌细胞同步化,治疗效果会更好。诱导细胞同步化的方法主要有两种,一种是DNA合成阻断法:用药物特异性抑制癌细胞的DNA合成,使其无法通过检测点(代号)被阻滞在S期;另一种是分裂中期阻断法:用秋水仙碱抑制的形成,使癌细胞无法通过检测点(代号)而停滞于中期。



