中考化学试题
取一定量Fe2O3与Al2O3的混合物,加入含溶质9.8g的稀硫酸,恰好完全反应.原混合物中氧元素的质量是( )
A.0.8g B.1.6g C.3.2g D.6.4g
采用下列实验方法鉴别物质,能达到目的的是
A.硬水和软水——滴加紫色石蕊溶液 B.黄铜和铜——加入硝酸银溶液
C.纯碱和小苏打——加稀盐酸 D.氯化铵和尿素——加熟石灰研磨,闻气味
下列实验不能达到相应目的的是
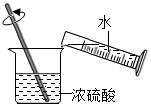
A .  比较蜡烛与水的密度 B .
比较蜡烛与水的密度 B . 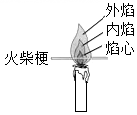 比较火焰各层温度
比较火焰各层温度
C .  验证质量守恒定律 D .
验证质量守恒定律 D .  验证产物有水
验证产物有水
下列反应中属于中和反应的是( )
A.Zn + CuSO4 = ZnSO4 + Cu B.SO2 + 2NaOH = Na2SO3 + H2O
C.2NaOH + H2SO4 = Na2SO4 + 2H2 O D.Na2CO3+ 2HCl = 2NaCl + H2O + CO2↑
某同学为验证铁、铜、银三种金属的活动性顺序,他设计了以下四种实验方案,其中能达到目的是
A. 将Fe、Cu分别加入AgNO3溶液中
B. 将Fe、Cu、Ag分别加入稀盐酸中
C. 将Fe分别加入CuSO4、AgNO3溶液中
D. 将Fe、Ag分别加入CuSO4溶液中
食盐是一种重要的化工原料,请回答下列问题。
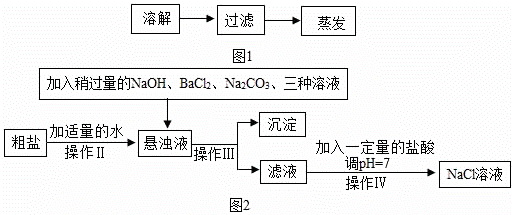
(1)如图1是实验室除去粗盐中泥沙等难溶性杂质的实验步骤。操作Ⅰ的名称是_____。
(2)由于粗盐中还含有少量的MgCl2、CaCl2、Na2SO4等可溶性杂质,不能满足化工生产的要求。因此必须将粗盐进行精制。其流程如图2所示:
①加入稍过量的Na2CO3溶液的目的是除去溶液中的_____ (填离子符号)。
②通过操作Ⅲ所得滤液中的溶质有三种,除了氯化钠外,还有两种,请分别写出它们的化学式_____、_____。
(2018·临沂)如图是实验室制取氢气的一种发生装置。
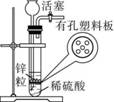
(1)检查该装置的气密性:关闭活塞,向长颈漏斗中加水,当出现
现象时,说明该装置的气密性良好。
(2)若液面刚好不与锌粒接触而又无稀硫酸可加,要制取H2且不影响生成H2的量,下列可以从长颈漏斗中加入的试剂是 (填序号)。
a.碳酸钠溶液
b.氯化钠溶液
c.氢氧化钠溶液
下列化学方程式书写正确的是
A.![]()
B.![]()
C.![]()
D.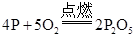
烧碱具有较好的杀菌消毒作用且廉价易得,但工业烧碱中常含有杂质碳酸钠。某科学学习小组同学围绕工业烧碱样品纯度测定问题,展开了讨论与探究。
(原理思路)利用Na2CO3与稀H2SO4反应产生CO2,通过CO2 质量的测定,确定样品中碳酸钠的质量,从而计算样品纯度。
(实验方案)小华同学根据以上思路,设计了如图的实验方案(固定装置省略)。如何检验A装置的气密性________________________。
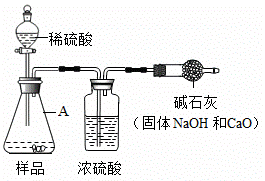
(交流讨论)小明认为上图实验方案的设计有缺陷,会导致难以避免的误差。你认为下列哪些因素会导致实验结果偏高_____________(填序号)。
①加入的稀硫酸量不足 ②装置内空气中的CO2没有排出
③反应产生的CO2未被完全吸收 ④干燥管与空气直接相通
(方案改进)为减少误差,使CO2质量的测定更准确,该小组同学根据以上讨论,对上图方案进行改进,设计了如下图的实验方案(固定装置省略)。
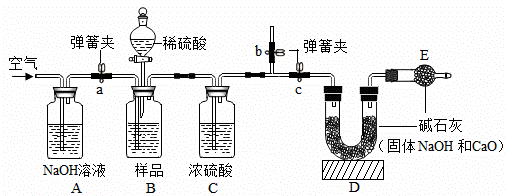
(1)装置B中样品在与稀硫酸反应前和停止反应后,都要通过量的空气。反应前通空气时a、b、c三个弹簧夹的控制方法是_______________。停止反应后,通过量的空气的目的是__________。
(2)写出装置A中发生反应的化学方程式:_______________________。
(数据分析)
(3)若反应过程中,装置B中滴加稀硫酸的速度太快,则烧碱的纯度将____________(填“偏高”、“偏低”或“无影响”)。
(4)若原样品共Ag,实验结束测得C装置增重Bg,D装置增重Cg,则原样品的纯度(质量分数)为_____________________________________。
(拓展延伸)
(5)D装置用装有氢氧化钠固体的U形管,而不用装有澄清石灰水的洗气瓶的原因:_________;请写出CO2与澄清石灰水反应的化学方程式:_______________________。
(6)实验结束后,小华、小明一起探讨时,发现按目前所学知识还有其它实验方案测定工业烧碱样品纯度,请你帮他们设计一个新方案:____________________________。
下列物质的名称、化学式、俗称均一致的是
A. 汞 Hg 水银
B. 氢氧化钙 CaO 熟石灰
C. 碳酸钠 Na2CO3 小苏打
D. 乙醇 CH3COOH 酒精
根据下列装置图回答问题:
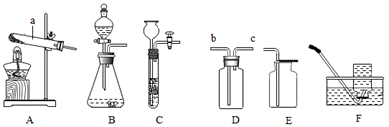
(1)仪器a的名称是_______________。
(2)用氯酸钾和MnO2制取较纯净的O2时,应选择的装置是___________(填标号),化学方程式是____________,若用向上排空气法收集氧气,验满的方法是__________________。
(3)碳酸钙粉末与稀硫酸反应可制得CO2,化学方程式是__________________。
(4)实验室制取H2时,通过控制液体流速,从而得到平稳气流,选择的发生装置是______________(填标号),若用排水法收集H2,应从D装置的____________(填“b”或“c”)口通入气体。
2019 年 8 月,太原市又购进 1000 台纯电动公交车,代替了之前的燃气公交车,进一步改善了城市麦通与人们的居住环境。
(1)以往燃气公交车所用燃气为石油化工产品——丙烷(C3H8),丙烷完全燃烧的化学方程式是 ___________________________________。
(2)使用纯电动公交车与燃气公交车相比,其优点是_______________________________。
利用推理、归纳的方法得出以下结论,其中正确的是
A.金刚石、石墨是组成元素相同的单质,所以化学性质相似
B.氧化物中一定含有氧元素,所以含氧元素的化合物一定是氧化物
C.碱溶液pH>7,所以pH>7的溶液均为碱溶液
D.铁的金属活动性比铝弱,所以铁制品比铝制品更耐腐蚀
氯化钠是一种常见的化学物质。下列说法不正确的是
A . 氯化钠是常见的食品调味剂 B . 氯化钠可用于生产氯气、烧碱
C . 蒸发海水即可获得纯净的氯化钠固体 D . 氯化钠可用于腌制食品
如图为元素周期表前四周期的部分信息:

结合如图分析,下列选项正确的是( )
A.N的原子序数是14
B.第2周期ⅠA族元素的原子易得到电子
C.第3周期ⅡA族元素的原子具有两个电子层
D.元素周期表是根据元素的原子结构和性质,把它们科学有序地排列起来得到的
(2020·红河模拟)云南围棋厂生产的“云子”围棋因其优良的品质得到全世界围棋爱好者的青睐。石英(SiO2)是制作围棋的原料之一。SiO2中Si的化合价为( )
A. +4 ![]() B. +2
B. +2 ![]() C. 0
C. 0 ![]() D. -4
D. -4
(2020·锦江模拟)化学反应的微观示意图如下图所示,下列说法错误的是( )
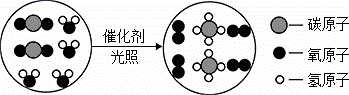
A. 从微观构成看:四种物质均由分子构成
B. 从物质分类看:该反应涉及到1种单质和3种氧化物
C. 从反应价值看:该反应能获取清洁能源和氧气,延缓温室效应
D. 从表示方法看:该反应的化学方程式为CO2+2H2O  CH4+2O2
CH4+2O2
实验室常用下列 A 、 B 、 C 装置制取气体, D 、 E 、 F 装置收集气体。

回答下列问题:
(1)A 装置中仪器 X 的名称是 ___________ 。
(2) 若用 B 装置制取氧气,反应的化学方程式为 ___________ 。在 D 、 E 中需选择 ___________ 集氧气,选择的依据是 ___________ 。
(3) 实验室常以氯酸钾、二氧化锰为原料,用 C 装置制取、 F 装置收集氧气。实验前需检查装置的气密性:连接装置 C 、 F ,微热 C 中试管,若 F 中产生气泡、且恢复常温后玻璃管内水面 ___________ 水槽的水面,就证明装置气密性良好。将反应后剩余固体溶解、过滤、洗净、干燥后又得到二氧化锰固体,其质量与反应前相比 ___________ ( 填 “ 增大 ”“ 减小 ” 或 “ 不变 ”) 。
(4) 若以高锰酸钾为原料、用 C 装置制取氧气,需要在 ___________ 塞一团棉花。
下列各组物质的溶液,不用其他试剂,无法将其一一区别的是
A. (NH4)2SO4 NaCl NH4Cl Ba(OH)2
B. H2SO4 NaOH Na2SO4 FeCl3
C. CaCl2 Na2SO4 Na2CO3 NaNO3
D. HCl H2SO4 BaCl2 K2CO3
下列实验操作正确的是
| | | | |
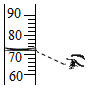
| A .稀释浓硫酸 | B .滴加液体 | C .读液体体积 | D .熄灭酒精灯 |
A . A B . B C . C D . D