高三化学上册专题练习题带答案和解析
| 1. 选择题 | 详细信息 |
|
下列物质的转化在给定条件下能实现的是 A. B. C. D. |
|
| 2. 选择题 | 详细信息 |
A,B,C,D四种物质之间的转化关系如图所示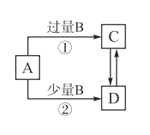 A.若A为 B.若A为Fe,B可能为稀硝酸,反应 C.若A为NaOH溶液,B可能为 D.若A为 |
|
| 3. 选择题 | 详细信息 |
|
A.25% B.75% C.88% D.32% |
|
| 4. 选择题 | 详细信息 |
取等物质的量浓度的NaOH溶液两份A和B,每份10mL,分别向A、B中通入不等量的CO2,再继续向两溶液中逐滴加入0.2mol/L的盐酸,标准状况下产生的CO2气体体积与所加的盐酸溶液体积之间的关系如图所示,下列叙述正确的是( )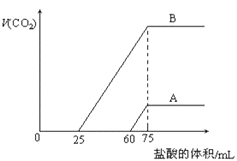 A. A曲线表明原NaOH溶液中通入CO2后,所得溶液中的溶质成分是Na2CO3和NaHCO3 B. B曲线中消耗盐酸0<v(HCl)<25mL时发生的离子反应为:OH-+H+=H2O H++CO32-=HCO3- C. B曲线表明原NaOH溶液中通入CO2后,所得溶液加盐酸后产生CO2气体体积(标准状况)的最大值为224mL D. 原NaOH溶液的物质的量浓度为1.0mol/L |
|
| 5. 选择题 | 详细信息 | |||||||||||||||
所谓合金,就是不同种金属(也包括一些非金属)在熔化状态下形成的一种熔合物,下表为四种金属的熔、沸点:
|
||||||||||||||||
| 6. 选择题 | 详细信息 |
|
已知A、B、C、D、E是短周期中原子序数依次增大的五种元素,A原子在元素周期表中原子半径最小;B与E同主族,且E的原子序数是B的两倍;C、D是金属元素,它们的氢氧化物相互之间可以发生反应。下列说法不正确的是( ) A.单质D可用于冶炼某些难熔金属 B.工业上常用电解法制得C和D的单质 C.稳定性:A2B>A2E D.简单离子的半径:C>D>E>B |
|
| 7. 选择题 | 详细信息 | |||||||||||||||||||||||||
下表各组物质中,不可以实现
|
||||||||||||||||||||||||||
| 8. 选择题 | 详细信息 |
|
在某100mL混合液中,HNO3和H2SO4的物质的量浓度分别是0.4mol/L和0.1mol/L。向该混合液中加入1.92g铜粉,加热,待充分反应后,所得溶液中的Cu2+的物质的量浓度是( )mol/L A. 0.15 B. 0.225 C. 0.35 D. 0.45 |
|
| 9. 选择题 | 详细信息 | ||||||||||||||||||||
下列各组物质中,不满足组内任意两种物质在一定条件下均能发生反应的是
|
|||||||||||||||||||||
| 10. 选择题 | 详细信息 |
|
认识反应条件对化学反应的影响,对学好化学具有重要意义。下列说法中正确的是 A. 镁在空气中或纯净氧气中燃烧的产物都只有MgO B. 钠在敞口容器中存放或在空气中燃烧的产物都是Na2O2 C. 将四氧化三铁溶解于过量的硝酸中,所得溶液中含有Fe3+、Fe2+ D. 氯化铝和过量的氨水反应一定得到Al(OH)3沉淀 |
|
| 11. 选择题 | 详细信息 |
|
下列试剂的保存或使用正确的是( ) A. 金属锂保存在煤油中,使用前要用滤纸吸干煤油 B. 过氧化钠比氧化钠稳定,因此过氧化钠可露置在空气中 C. 称量NaOH固体时,应先在天平两个托盘上各放一张等质量的纸,左边纸上放NaOH,右边纸上放砝码 D. 做焰色反应实验时,透过蓝色钴玻璃,观察到火焰颜色为紫色,证明被检验物中一定有钾元素 |
|
| 12. 选择题 | 详细信息 |
|
下列操作中,溶液的颜色不发生变化的是( ) A.碳酸氢钠溶液中滴加稀盐酸 B.硫酸铁溶液中滴加硫氰化钾溶液 C.氯化亚铁溶液中滴加氯水 D.三氯化铁溶液中加入过量Cu粉 |
|
| 13. 选择题 | 详细信息 |
|
下列化学用语表达正确的是 A. NaHS的电离:NaHS = Na+ + H+ + S2- B. 把金属铁放入稀硝酸中: Fe + 2H+ = Fe2+ + H2↑ C. NaHCO3溶液与少量的澄清石灰水反应:HCO3- + OH- + Ca2+ = CaCO3↓+ H2O D. HClO的电离:HClO |
|
| 14. 选择题 | 详细信息 |
|
自然界中只有极少数金属(如金和铂等)能以单质形式存在。它们应具备的性质是 A.不易被氧化 B.还原性较强 C.可与强酸反应放出氢气 D.可与空气中的氧气反应形成保护膜 |
|
| 15. 选择题 | 详细信息 |
|
在下列物质中,分别加入金属钠,不能产生氢气的是 A.无水酒精 B.蒸馏水 C.苯 D.硫酸铜溶液 |
|
| 16. 选择题 | 详细信息 |
|
A. B. C.1 mol D.标准状况下, |
|
| 17. 选择题 | 详细信息 |
|
把含有氧化铁的铁片投入到足量的稀盐酸中,直到铁片完全溶解,经分析该溶液中无 A.1:1 B.2:5 C.4:1 D.3:1 |
|
| 18. 选择题 | 详细信息 |
|
下列类比关系正确的是 A. B.Al与 C.Fe与 D. |
|
| 19. 选择题 | 详细信息 |
|
将 A.生成白色沉淀 C.无气泡产生 |
|
| 20. 选择题 | 详细信息 |
|
将一小块钠投入到盛有煤油和水的试管中(煤油和水均足够多),想一想可能观察到的现象是 A. 钠浮在试管的液面上 B. 钠沉入试管底部 C. 钠处于煤油和水的交界处 D. 钠燃烧起来 |
|
| 21. 填空题 | 详细信息 |
|
铁、铜及其化合物在工农业生产中应用广泛。 (1)在潮湿空气中,钢铁发生电化学腐蚀转化为Fe(OH)2的反应方程式为_______。在含有等浓度硫酸溶液的下列装置中,铁腐蚀的速率由快到慢的顺序是____________(用序号填写)。 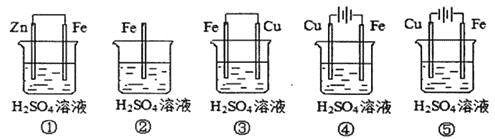 (2)已知:①3Fe(s)+2O2(g)=Fe3O4(s) ②2Al(s)+3/2O2(g)=A12O3(s) 则焊接钢轨时铝与Fe3O4发生反应生成铁和Al2O3的热化学方程式为______________。 (3)Na2FeO4具有强氧化性,其电解制法如图所示,请写出阳极的电极反应式______。Na2FeO4是一种既能杀菌、消毒,又能絮凝净水的水处理剂,其原理是______________。 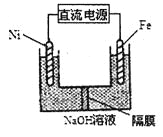 (4)工业上常用FeCl3溶液腐蚀印刷线路板,发生反应的离子方程式是____________。若腐蚀铜板后的溶液中,Cu2+、Fe3+和Fe2+浓度均为0.1 mol·L-1,结合下图分析,当混合溶液中通入氨气调节溶液的pH=5.6时,溶液中存在的金属阳离子为____。从图中数据计算Fe(OH)2的溶度积Ksp[Fe(OH)2]=______。 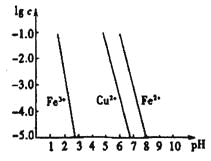 已知:横坐标为溶液的pH,纵坐标为金属离子的物质的量浓度的对数(当溶液中金属离子浓度 |
|
| 22. | 详细信息 | |||||||||||||||
镀作为一种新兴材料日益被重视,有“超级金属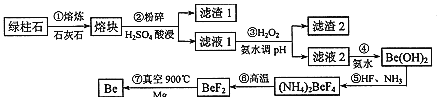 按元素周期表的对角线规则,Be和Al性质相似;几种金属阳离子的氢氧化物沉淀时的pH如表。回答下列问题:
|
||||||||||||||||
| 23. 综合题 | 详细信息 |
|
铜是重要金属,Cu的化合物在科学研究和工业生产中具有许多用途,如 A. B.在 C. D. 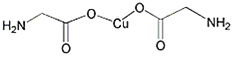 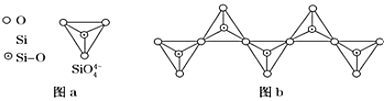 |
|
| 24. 综合题 | 详细信息 | |||||||||||||||
|
雾霾天气严重影响人们的生活质量,其中氮氧化物和硫氧化物是造成雾霾天气的主要原因之一。消除氮氧化物和硫氧化物有多种方法。 (1)氮、氧元素非金属性较强的是_____。(用元素符号回答) (2)NH3催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术。反应原理如图1所示: 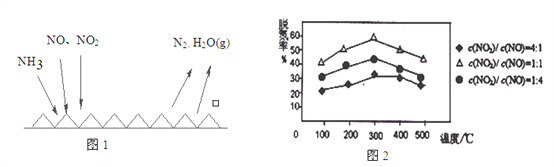 ①由图1可知SCR技术中的氧化剂为:_________________。 ②用Fe做催化剂时,在氨气足量的情况下,不同c(NO)/c(NO2)对应的脱氮率如图2所示,效果最佳的c(NO)/ c(NO2)=_________。 (3)硝酸厂常用如下烧碱吸收法处理氦氧化物(NO与NO2)尾气。氮氧化物(NO与NO2)用烧碱进行吸收,产物为NaNO2、NaNO3和H2O。现有含0.5mol氮氧化物的尾气,恰好被一定体积的25%NaOH溶液(密度1.28g/cm3)完全吸收。已知反应后溶液中含有0.35mo1NaNO2。则尾气中NO与NO2的物质的量之比为______。(已知:2NO2+2NaOH=NaNO3+NaNO2+H2O、NO+NO2+2NaOH=2NaNO2+H2O) (4)现将一定量的铁和铜的混合物分为等质量的4份,分别加入等浓度不同体积的稀硝酸[假设反应中稀硝酸的还原产物只有NO),产生气体在标准状况下的体积与剩余固体的质量如下表:
|
||||||||||||||||
| 25. 推断题 | 详细信息 |
X、Y、Z、Q、R 是五种短周期元素,原子序数依次增大。X、Y 两元素最高 正价与最低负价之和均为 0;Q 与 X 同主族;Z、R 分别是地壳中含量最高的非金属元素和 金属元素。请回答下列问题: |
|
最近更新



