西安市2018年高二上半年化学期中考试带参考答案与解析
| 1. 选择题 | 详细信息 |
|
关于下列物质的用途的说法错误的是 A.酚类化合物有毒,不能用于杀菌消毒 B.乙二醇可用于配制汽车防冻液 C.部分卤代烃可用作灭火剂 D.甲醛的水溶液(福尔马林)可用于防腐 |
|
| 2. 选择题 | 详细信息 |
|
下列各组中分子式所代表的物质一定互为同系物的是 A. C2H4O与C3H6O B. C2H4O2与C3H6O2 C. C7H8与C8H10(均含苯环) D. C7H8O与C8H10O(均含苯环) |
|
| 3. 选择题 | 详细信息 |
|
某物质中可能有甲醇、甲酸、乙醇、甲酸乙酯几种物质中的一种或几种,在鉴定该物质时有下列现象:①有银镜反应;②加入新制的Cu(OH)2悬浊液,沉淀不溶解;③与含有酚酞的NaOH溶液共热时发现溶液中红色逐渐变浅。下列叙述中正确的是 A. 有甲酸乙酯和甲酸 B. 有甲酸乙酯,可能有甲醇 C. 有甲酸乙酯和乙醇 D. 几种物质都有 |
|
| 4. 选择题 | 详细信息 |
|
下列是除去括号内杂质的有关操作,其中正确的是 A. 乙醇(乙醛)——加水,振荡静置后分液 B. 乙酸乙酯(乙酸)——加乙醇、浓硫酸加热 C. 乙烯(乙炔)——将气体通过盛KMnO4溶液的洗气瓶 D. 苯(苯酚)——加足量NaOH溶液,振荡静置后分液 |
|
| 5. 选择题 | 详细信息 |
|
A. 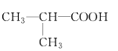 B. C. 乙醛的同系物 D. 丁醛的同分异构体 |
|
| 6. 选择题 | 详细信息 |
|
分子式为C10H20O2的有机物A,能在酸性条件下水解生成有机物C和D,且C在一定条件下可转化成D,则A的可能结构有 A. 4种 B. 8种 C. 12种 D. 16种 |
|
| 7. 选择题 | 详细信息 |
|
下列各组物质中不管以何种比例混合,只要总质量一定,充分燃烧后生成的二氧化碳的量不变的是 ( ) A. 乙炔和乙烯 B. 乙醇和丙醇 C. 乙醇和乙醚(C2H5OC2H5) D. 甲醛和乙酸 |
|
| 8. 选择题 | 详细信息 |
|
已知烯烃在一定条件下氧化时, A. 1—己烯 B. 2—己烯 C. 2—甲基—2—戊烯 D. 3—己烯 |
|
| 9. 选择题 | 详细信息 |
|
某有机物A由C、H、O三种元素组成,相对分子质量为90。将4.5 g A完全燃烧的产物依次通过足量的浓硫酸和碱石灰,分别增重2.7 g和6.6 g。A能与NaHCO3溶液产生CO2,且两分子A之间脱水可生成六元环状化合物。有关A的说法正确的是 A. 有机物A的分子式为C3H8O3 B. 0.1 mol A与足量Na反应生成2.24 L H2 C. A催化氧化的产物不能发生银镜反应 D. A能在一定条件下发生缩聚反应生成 |
|
| 10. 选择题 | 详细信息 |
|
有下列物:①乙醇、②苯酚、③乙醛、④丙烯酸(CH2=CHCOOH)、⑤乙酸乙酯。其中与溴水、酸性KMnO4溶液、NaHCO3溶液都能反应的是( ) A. ①③ B. ②⑤ C. ④ D. ③④ |
|
| 11. 选择题 | 详细信息 |
|
对复杂的有机物的结构,可以用键线式简化表示,如有机物CH2===CHCHO,可简化写成 |
|
| 12. 选择题 | 详细信息 |
食品化学家A.SaariCsallany和Christine Seppanen研究发现,当豆油被加热到油炸温度(185 ℃)时,会产生如下所示高毒性物质,许多疾病和这种有毒物质有关,如帕金森症。下列关于这种有毒物质的判断不正确的是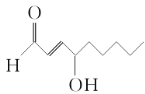 A. 该物质属于烃的衍生物 B. 该物质的分子式为C9H14O2 C. 该物质分子中含有三种官能团 D. 该物质最多可以和2 mol H2发生加成反应 |
|
| 13. 选择题 | 详细信息 |
|
下列依据热化学方程式得出的结论正确的是( ) A. 已知2SO2(g)+O2 B. 已知C(石墨,s)=C(金刚石,s) △H>0,则金刚石比石墨稳定 C. 已知H+(aq)+OH-(aq)=H2O(1),△H=-57.3kJ/mol,则任何酸碱中和反应的热效应均为57.3 kJ D. 已知2C(s)+2O2(g)=2CO2(g) △H1,2C(s)+O2(g)=2CO(g) △H2 则△H1<△H2 |
|
| 14. 选择题 | 详细信息 |
|
已知:2H2(g)+O2(g) ===2H2O(l) ΔH=-571.66 kJ·mol-1 CO(g)+1/2O2(g) ===CO2(g) ΔH=-282.9 kJ·mol-1 若氢气与一氧化碳的混合气体完全燃烧可生成2.7 g H2O(l),并放出57.02 kJ热量,则混合气体中CO的物质的量约为( ) A. 0.22 mol B. 0.15 mol C. 0.1 mol D. 0.05 mol |
|
| 15. 选择题 | 详细信息 |
|
一定条件下,充分燃烧一定量的丁烷生成二氧化碳和气态水时放出热量Q kJ(Q>0)。经测定完全吸收生成的CO2需消耗5 mol·L-1的KOH溶液100 mL,恰好生成正盐。则此条件下反应C4H10(g)+13/2O2(g) A. +8Q B. +16Q C. -8Q D. -16Q |
|
| 16. 选择题 | 详细信息 |
|
已知:P4(g)+6Cl2(g)===4PCl3(g) ΔH=a kJ·mol-1, P4(g)+10Cl2(g)===4PCl5(g) ΔH=b kJ·mol-1, 又知形成或拆开1 mol化学键放出或吸收的能量称为该化学键的键能。P4具有正四面体结构,PCl5中P-Cl键的键能为c kJ·mol-1,PCl3中P-Cl键的键能为1.2c kJ·mol-1。下列叙述正确的是 A. P-P键的键能大于P-Cl键的键能 B. 可求Cl2(g)+PCl3(g)===PCl5(s)的反应热ΔH C. Cl-Cl键的键能为(b-a+5.6c)/4 kJ·mol-1 D. P-P键的键能为(5a-3b+12c)/8 kJ·mol-1 |
|
| 17. 综合题 | 详细信息 |
|
(1)13 g C2H2(g)完全燃烧生成CO2和H2O(l)时,放出659 kJ的热量,写出表示该物质燃烧热的热化学方程式___________________________。 (2)已知反应:Cl2+2HBr===Br2+2HCl。 Ⅰ.当有0.2 mol HCl生成时放出8.1 kJ的热量。 Ⅱ.其能量变化示意图如图: 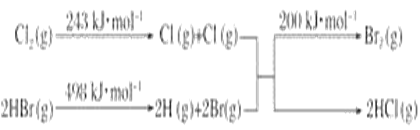 则该反应的热化学方程式为_____________________________________。由上述数据判断断开1 mol H—Cl 键与断开 1 mol H—Br键所需能量相差约为________kJ。 (3)已知:①2CO(g)+O2(g) ===2CO2(g) ΔH=-566 kJ·mol-1 ②Na2O2(s)+CO2(g) ===Na2CO3(s)+1/2O2(g) ΔH=-226 kJ·mol-1 则CO(g)与Na2O2(s)反应放出509 kJ热量时,电子转移数目为________。 (4)已知CO 、H2 、CH4 的燃烧热分别为283 kJ·mol-1、286 kJ·mol-1、890 kJ·mol-1。若将a mol CH4、CO和H2的混合气体完全燃烧,生成CO2气体和液态水,且CO2和水的物质的量相等时,则放出热量(Q)的取值范围是____。 |
|
| 18. 实验题 | 详细信息 |
|
盐酸或硫酸和NaOH溶液的中和反应没有明显的现象。某学习兴趣小组的同学为了证明NaOH溶液与盐酸或硫酸发生了反应,从中和反应的热效应出发,设计了下面几种实验方案。请回答有关问题: (1)方案一:如图装好实验装置,图中小试管用细线吊着,细线的上端拴在细铁丝上。开始时使右端U形管两端红墨水相平。实验开始,向下插细铁丝,使小试管内盐酸和广口瓶内NaOH溶液混合,此时观察到的现象是________________________________,原因是__________________________________________________。 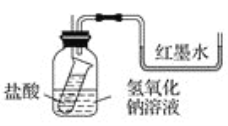 (2)方案二:该小组借助反应溶液温度的变化来判断反应的发生。如果NaOH溶液与盐酸混合前后有温度的变化,则证明发生了化学反应。该小组同学将不同浓度的NaOH溶液和盐酸各10 mL混合,用温度计测量反应前后温度的变化,测得的部分数据如下表: 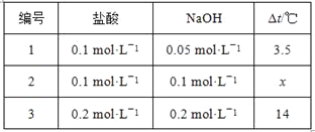 则x=______。假设盐酸和NaOH溶液的密度都是1 g·cm-3,又知中和后生成溶液的比热容c=4.18 J·g-1·℃-1,依据该小组的实验数据计算,写出表示稀盐酸和稀NaOH溶液反应的中和热的热化学方程式________________________________________。 (3)若H+(aq)+OH-(aq) ===H2O(l) ΔH=-57.3 kJ·mol-1;现有:①稀H2SO4与Ba(OH)2(aq) ②浓H2SO4与Ba(OH)2(aq) ③稀HNO3与Ba(OH)2(aq)反应生成1 mol H2O(l)的反应热分别为ΔH1、ΔH2、ΔH3,则ΔH1、ΔH2、ΔH3三者由小到大的关系为 ______________________。 |
|
| 19. 综合题 | 详细信息 |
聚醋酸乙烯酯是黏合剂,应用广泛。下面是该有机物的合成路线: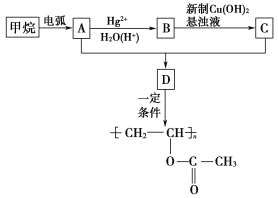 提示:①甲烷在电弧的作用下生成炔烃。 ②CH3C≡CH 请回答下列问题: (1)甲烷合成A的化学反应中原子利用率为________。 (2)B的结构简式为________。 (3)B生成C的反应中除新制Cu(OH)2悬浊液外还需要的条件是________。 (4)A与C反应生成D的反应类型是________。 (5)写出由D生成 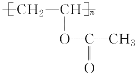 反应的化学方程式:____________________________________________________。 反应的化学方程式:____________________________________________________。(6)写出能既能溴水褪色又能使紫色石蕊溶液变红的D的同分异构体的结构简式:_____________________________________。 |
|
| 20. 综合题 | 详细信息 |
下图中A、B、C、D、E、F、G、H均为有机化合物。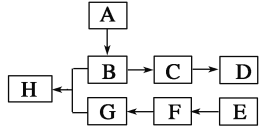 回答下列问题: (1)有机化合物A的相对分子质量小于60,A能发生银镜反应,1 mol A在催化剂作用下能与3 mol H2反应生成B,则A的结构简式是__________________,由A生成B的反应类型是__________; (2)B在浓硫酸中加热可生成C,C在催化剂作用下可聚合生成高分子化合物D,由C 生成D的化学方程式是_________________________________________________; (3)①芳香族化合物E的分子式是C8H8Cl2 ,E的苯环上的一溴取代物只有一种,则E的所有可能的同分异构体共有________种; ②E在NaOH溶液中可转变为F,F用高锰酸钾酸性溶液氧化生成G(C8H6O4)。1 mol G与足量的NaHCO3溶液反应可放出44.8 L CO2(标准状况),由此确定E的结构简式是_____________________________________; (4)G和足量的B在浓硫酸催化下加热反应可生成H,则由G和B生成H的化学方程式是________________________________________________________该反应的反应类型是__________。 |
|
| 21. 推断题 | 详细信息 |
有机物A~M有如图所示转化关系,A与F分子中所含碳原子数相同,且均能与NaHCO3溶液反应,F的分子式为C9H10O2,且不能使溴的CCl4溶液褪色,D能发生银镜反应,M与NaOH溶液反应后的产物,其一氯代物只有一种。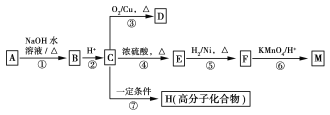 已知: 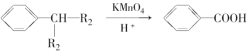 (R1、R2表烃基或氢原子) (R1、R2表烃基或氢原子)请回答: (1)B、F的结构简式分别为________、________。 (2)反应①~⑦中,属于消去反应的是________(填反应序号)。 (3)D发生银镜反应的化学方程式为______________________________;反应⑦的化学方程式为______________________________。 (4)A的相对分子质量在180~260之间,从以上转化中不能确认A中的某一官能团,确定该官能团的实验步骤和现象为__________________________________________。 (5)符合下列条件的F的同分异构体共有________种。 a.能发生银镜反 b.能与FeCl3溶液发生显色反应 c.核磁共振氢谱上有四个峰,其峰面积之比为1∶1∶2∶6 |
|
最近更新



