鲁科版选择性必修1第2章化学反应的方向、限度与速率第2节综合训练
| 1. 选择题 | 详细信息 |
|
某温度下,体积一定的密闭容器中发生如下可逆反应:2X(g)+Y(s) A. 消耗2 mol X同时生成3 mol Z,说明达到了平衡状态 B. 加入少量的Y正反应速率加快 C. 气体的密度不变时,说明达到了平衡状态 D. 加入少量的X,Q变大 |
|
| 2. 选择题 | 详细信息 |
|
一定条件下的密闭容器中:4NH3(g)+5O2(g) A.4molNH3和5molO2反应,达到平衡时放出热量为905.9kJ B.平衡时v正(O2)= C.平衡后降低压强,混合气体平均摩尔质量增大 D.平衡后升高温度,混合气体中NO含量降低 |
|
| 3. 选择题 | 详细信息 | |||||||||||||||
下列选项中的原因或结论与现象不对应的是( )
|
||||||||||||||||
| 4. 选择题 | 详细信息 | ||||||||||
|
在一定温度下,将气体X和气体Y各0.16mol充入10L恒容密闭容器中,发生反应 X(g)+Y(g)
|
|||||||||||
| 5. 选择题 | 详细信息 | ||||||||||||||||||
相同温度下,体积均为0.25 L的两个恒容密闭容器中发生可逆反应:N2(g)+3H2(g)
|
|||||||||||||||||||
| 6. 选择题 | 详细信息 |
对于反应 A. 实验c条件下,从反应开始至达到平衡时 B. 实验a条件下,用浓度表示的平衡常数为100 C. 该反应的 D. 比较实验a、c可判断升高温度反应速率加快 |
|
| 7. 选择题 | 详细信息 |
工业上利用Ga与NH3高温条件下合成固体半导体材料氮化稼(GaN)同时有氢气生成。反应中,每生成3molH2时放出30.8kJ的热量。恒温恒容密闭体系内进行上述反应, 下列有关表达正确的是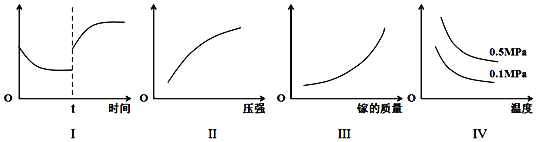 A. I图像中如果纵坐标为正反应速率,则t时刻改变的条件可以为升温或加压 B. II图像中纵坐标可以为镓的转化率 C. III图像中纵坐标可以为化学反应速率 D. IV图像中纵坐标可以为体系内混合气体平均相对分子质量 |
|
| 8. 选择题 | 详细信息 |
甲、乙、丙三个容器中最初存在的物质及其数量如图所示,三个容器最初的容积相等、温度相同,反应中甲、丙的容积不变,乙中的压强不变,在一定温度下反应达到平衡。下列说法正确的是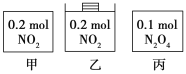 A.平衡时各容器内c(NO2)的大小顺序为乙>甲>丙 B.平衡时N2O4的百分含量:乙>甲=丙 C.平衡时甲中NO2与丙中N2O4的转化率不可能相同 D.平衡时混合物的平均相对分子质量:甲>乙>丙 |
|
| 9. 选择题 | 详细信息 |
|
下列事实不能用勒夏特列原理解释的是 A. 开启啤酒瓶后,瓶中马上泛起大量泡沫 B. 合成氨反应,为提高氨的产率,理论上应采取降低温度的措施 C. 工业上生产硫酸的过程中使用过量的空气以提高二氧化硫的利用率 D. 对于2HI(g) |
|
| 10. 选择题 | 详细信息 | ||||||||||||
在容积为1 L的密闭容器中,投入1 mol N2和3 mol H2分别在以下不同实验条件下进行反应。下列分析正确的是
|
|||||||||||||
| 11. 选择题 | 详细信息 |
甲醇是重要的化工原料,具有广泛的开发和应用前景。在体积可变的密闭容器中投入0.5molCO和1molH2,不同条件下发生反应:CO(g)+2H2(g)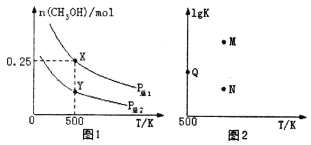 A.P总1<P总2 B.混合气体的密度不再发生变化,说明该反应已达到平衡状态 C.图2中M点能正确表示该反应平衡常数的对数(1gK)与温度的关系 D.若P总1=0.25MPa,则Y点的平衡常数Kp=64(MPa)-2 |
|
| 12. 综合题 | 详细信息 | ||||||||
合成氨技术的创立开辟了人工固氮的重要途径,其研究自正确的理论指导,合成氨反应N2+3H2
|
|||||||||
| 13. 综合题 | 详细信息 | ||||||||||
|
能源是人类共同关注的重要问题。页岩气是从页岩层中开采出来的一种非常重要的天然气资源,页岩气的主要成分是甲烷,是公认的洁净能源。 (1)页岩气不仅能用作燃料,还可用于生产合成气(CO和H2)。CH4与H2O(g)通入聚焦太阳能反应器,发生反应CH4(g)+H2O(g)=CO(g)+3H2(g) △H1 已知:①CH4、H2、CO的燃烧热(△H)分别为-a kJ•mol-1、-b kJ•mol-1、-c kJ•mol-1; ②H2O(l)=H2O(g);△H=+d kJ•mol-1 则△H1=____(用含字母a、b、c、d的代数式表示)kJ•mol-1。 (2)用合成气生成甲醇的反应为:CO(g)+2H2(g) 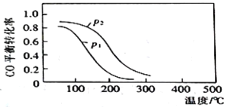
|
|||||||||||
 恒定时,温度、压强对平衡混合气中CH4含量的影响如图所示:
恒定时,温度、压强对平衡混合气中CH4含量的影响如图所示: