浙江高二化学期末考试(2019年下册)网上在线做题
| 1. 选择题 | 详细信息 |
|
化学与人类生产、生活、社会可持续发展密切相关,下列有关说法不正确的是 A. 高纯硅广泛应用于太阳能电池、计算机芯片,是一种重要的半导体材料 B. 氟利昂和NOx都能破坏臭氧层,从而导致“温室效应” C. 中国是目前全球最大的稀土生产国和出口国,对稀土元素及其化合物的研究是获得优良催化剂的一种重要途径 D. 华为发布的首款5G折叠屏手机,用镁铝合金制成的手机外壳具有轻便抗压的特点 |
|
| 2. 选择题 | 详细信息 |
|
下列表示正确的是 A. 绿矾的化学式:FeSO4·7H2O B. H2O2的电子式: C. 次氯酸的结构式:H-Cl-O D. 比例模型 |
|
| 3. 选择题 | 详细信息 |
|
下列有关实验现象的描述正确的是 A. 铁在氧气中剧烈燃烧,放出耀眼的白光,集气瓶内壁附着黑色固体 B. 溴水中滴加裂化汽油,溶液褪色且分层 C. 铜在氯气中燃烧,产生白烟,加水溶解后可得到绿色溶液 D. 用洁净的玻璃棒蘸取碳酸钾粉末在酒精灯火焰上灼烧,可观察到明亮的紫色火焰 |
|
| 4. 选择题 | 详细信息 |
|
设NA为阿伏加德罗常数的值。下列说法正确的是 A. 20g 49%的硫酸中,H2SO4分子数为0.01NA B. 100mL 0.1mol·L-1 Na2CO3溶液中阴离子总数小于0.01NA C. 1 mol Cl2溶于水,溶液中Cl-、HClO、ClO-粒子数之和小于2 NA D. 标准状况下,3.36L氯仿的分子数为0.15 NA |
|
| 5. 选择题 | 详细信息 |
|
Cl2是纺织工业中常用的漂白剂,Na2S2O3可作漂白布匹后的“脱氯剂”,S2O32-和Cl2反应的产物之一为SO42-。下列说法中不正确的是 A. 该反应中Cl2发生还原反应 B. 根据该反应可判断还原性:S2O32->Cl- C. 脱氯反应后,溶液的酸性增强 D. SO2与氯气的漂白原理相同,所以也可以用SO2作纺织工业的漂白剂 |
|
| 6. 选择题 | 详细信息 |
|
下列离子方程式正确的是 A. 向硫酸铝溶液中滴加过量氨水:Al3++4NH3·H2O=AlO2-+2H2O+4NH4+ B. 过氧化钠投入水中:2O22-+2H2O=4OH-+O2↑ C. 向碳酸氢钙溶液中滴入少量的澄清石灰水:Ca2++HCO3-+OH-=CaCO3↓+H2O D. 向碳酸氢铵溶液中滴加过量氢氧化钠溶液:NH4++OH-=NH3↑+H2O |
|
| 7. 选择题 | 详细信息 |
|
下列说法正确的是 A. 蒸馏时,加热之前先通冷却水,停止加热后,仍要继续通冷却水一段时间 B. 用纸层析法分离Cu2+和Fe3+,滤纸上端呈棕黄色,说明Fe3+在有机溶剂中的溶解能力较Cu2+小 C. 用冷却结晶法除去NaCl中混有少量的KNO3 D. 将镀锌铁皮投入一定浓度的硫酸中反应至金属表面气泡突然减小,取出,直接小火烘干称量,由此测得的镀锌层厚度将偏大 |
|
| 8. 选择题 | 详细信息 |
|
下列叙述正确的是 A. 某晶体在固态与液态时均能导电,该晶体是离子晶体 B. H2O的热稳定性比H2S强,说明水分子内的氢键强 C. Na2O固体上滴加少量水,有共价键和离子键的破坏及形成 D. N2、CO2、CCl4等化合物中所有原子均符合8电子稳定结构 |
|
| 9. 选择题 | 详细信息 |
有关下图及实验的描述正确的是 A. 用装置甲量取15.00mL的NaOH溶液 B. 用装置乙制备Cl2 C. 装置丙中X若为CCl4,可用于吸收NH3或HCl,并防止倒吸 D. 用装置丁电解精炼铝 |
|
| 10. 选择题 | 详细信息 |
A、B、C、D、E均为短周期主族元素,B、C、D在周期表中的位置关系如下图所示。A元素的某种同位素原子没有中子,D元素的原子序数是C的2倍,E是短周期主族元素中半径最大的元素。下列说法不正确的是 A. 简单离子的半径大小关系:B>C>E B. D、E两种元素形成的化合物,可能含有离子键和共价键 C. A、B、C三种元素形成的化合物的水溶液均显酸性 D. D、E分别和C形成的化合物,均可能使溴水或品红溶液褪色 |
|
| 11. 选择题 | 详细信息 |
|
室温下,下列有关溶液说法正确的是 A. 为确定某酸H2A是强酸还是弱酸,可测NaHA溶液的pH B. 某溶液中由水电离出的c(H+)=1×10-a mol·L-1,若a>7时,则溶液的pH为a或14-a C. 等体积等物质的量浓度的NaClO溶液和NaCl溶液中离子总数大小N前>N后 D. 常温下,pH=3的HA溶液与pH=11的BOH等体积混合,溶液pH>7,则BOH为强碱 |
|
| 12. 选择题 | 详细信息 |
|
下列说法正确的是 A. 按系统命名法,  的名称为2-甲基-3-乙基丁烷 的名称为2-甲基-3-乙基丁烷B. 聚乙烯(PE)和聚氯乙烯(PVC)的单体都是不饱和烃,均能使溴水褪色 C.  分子中至少有11个碳原子处于同一平面 分子中至少有11个碳原子处于同一平面D. 有机物 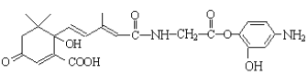 与NaOH溶液反应,最多消耗4mol NaOH 与NaOH溶液反应,最多消耗4mol NaOH |
|
| 13. 选择题 | 详细信息 |
NH4X(X为卤素原子)的能量关系如下图所示。下列说法正确的是 A. ∆H1<∆H5 B. ∆H6=∆H1+∆H2+∆H3+∆H4+∆H5 C. 已知NH4Cl溶于水吸热,则∆H6>0 D. 相同条件下,NH4Cl的(∆H2+∆H3+∆H5)比NH4Br的大 |
|
| 14. 选择题 | 详细信息 |
《Journal of Energy Chemistry》报导我国科学家设计CO2熔盐捕获与转化装置如图。下列有关说法正确的是 A. b为电源的正极 B. 电子流向:c→a→b→d C. c极电极反应式为2C2O52――4e-=4CO2+O2 D. 转移0.4mol电子可捕获CO2 2.24L |
|
| 15. 选择题 | 详细信息 |
大气中CO2含量的增多除了导致地球表面温度升高外,还会影响海洋生态环境。某研究小组在实验室测得不同温度下(T1,T2)海水中CO32-浓度与模拟空气中CO2浓度的关系曲线。下列说法不正确的是 A. T1>T2 B. 海水温度一定时,大气中CO2浓度增加,海水中溶解的CO2随之增大,导致CO32-浓度降低 C. 当大气中CO2浓度确定时,海水温度越高,CO32- 浓度越低 D. 大气中CO2含量增加时,海水中的珊瑚礁将逐渐溶解 |
|
| 16. 选择题 | 详细信息 |
已知:pKa=-lgKa,25℃时,H2SO3的pKa1=1.85,pKa2=7.19。常温下,用0.1mol·L-1NaOH溶液滴定20mL 0.1mol·L-1H2SO3溶液的滴定曲线如图所示。 下列说法不正确的是 A. 点A所得溶液中:Vo>10mL B. 点B所得溶液中:c(H2SO3)+c(H+)=c(SO32-)+c(OH-) C. 点C所得溶液中:c(Na+)>3c(HSO3-) D. 点D所得溶液中 |
|
| 17. 选择题 | 详细信息 |
某实验小组利用BaS的还原性提纯HBr溶液,并制取 下列说法不正确的是 A. 还原步骤中可能会产生有毒气体 B. 沉淀步骤中可用 C. 滤渣的成分为S和 D. |
|
| 18. 选择题 | 详细信息 |
某溶液X含有K+、Mg2+、Fe3+、Al3+、Fe2+、Cl-、CO32-、OH-、SiO32-、NO3-、SO42-中的几种,已知该溶液中各离子物质的量浓度均为0.20mol·L-1(不考虑水的电离及离子的水解)。为确定该溶液中含有的离子,现进行了如下的操作: 下列说法正确的是 A.无色气体可能是NO和CO2的混合物 B.由步骤③可知,原溶液肯定存在Fe3+ C.溶液X中所含离子种类共有4种 D.另取100mL原溶液X,加入足量的NaOH溶液,充分反应后过滤,洗涤,灼烧至恒重,理论上得到的固体质量为2.4g |
|
| 19. 推断题 | 详细信息 |
|
有一应用前景广阔的纳米材料甲,其由A、B两种短周期非金属元素组成,难溶于水,且硬度大,熔点高。取材料甲与熔融的烧碱反应,生成一种含A元素的含氧酸盐乙和一种含B元素的气体丙,丙能使湿润的红色石蕊试纸变蓝;乙能溶于水,加盐酸产生白色沉淀,盐酸过量沉淀不溶解。 (1)甲的化学式为____________,其晶体属于____________晶体。 (2)乙的水溶液可以用来做________________________(写出一种用途)。 (3)B元素的一种氢化物丁,相对分子质量为32,常温下为液体,其燃烧放热多且燃烧产物对环境无污染,因此可用作火箭燃料、燃料电池燃料等。则 ①丁的电子式为_____。 ②丁可由次氯酸钠与过量氨气反应制得,其化学方程式________________________。 甲的制备过程中氨气需要过量的理由是____________________________________。 ③丁的水溶液呈弱碱性,室温下其电离常数K1≈1.0×10-6,则0.01 mol·L-1丁水溶液的pH等于____________(忽略丁的二级电离和H2O的电离)。 |
|
| 20. 推断题 | 详细信息 |
盐X由三种元素组成,其具有良好的热电性能,在热电转换领域具有广阔的应用前景。为研究它的组成和性质,现取12.30g化合物X进行如下实验: 试根据以上内容回答下列问题: (1)X的化学式为_____________。 (2)无色溶液B中通入过量CO2产生白色沉淀的离子方程式为______________。 (3)蓝色溶液F中通入中SO2气体会产生白色沉淀,该沉淀中氯元素质量分数为35.7%,其离子方程式为____________。 (4)白色沉淀C煅烧的固体产物与D高温反应可生成化合物X,其化学方程式为__________。 |
|
| 21. 综合题 | 详细信息 |
|
甲醛在木材加工、医药等方面有重要用途。 I.利用甲醇(CH3OH)制备甲醛 脱氢法:CH3OH(g)⇌HCHO(g)+H2(g) △H1=+92.09kJ·mol-1 氧化法:CH3OH(g)+1/2O2(g)⇌HCHO(g)+H2O(g) △H2 (1)脱氢法制甲醛,有利于提高平衡产率的条件有____________。 A.低温 B.高温 C.低压 D.高压 E.催化剂 (2)已知:2H2(g)+O2(g)=2H2O(g) △H3=-483.64kJ·mol-1,则△H2=________。 (3)750K下,在恒容密闭容器中,充入一定量的甲醇,发生反应CH3OH(g)⇌HCHO(g)+H2(g),若起始压强为101kPa,达到平衡转化率为50.0%,则反应的平衡常数Kp=__________(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数,忽略其它反应)。 (4)Na2CO3是甲醇脱氢制甲醛的催化剂,有研究指出,催化反应的部分机理如下: 历程i:CH3OH→·H+·CH2OH 历程ⅱ:·CH2OH→·H+HCHO 历程ⅲ:·CH2OH→3·H+CO 历程iv:·H+·H→H2 如图所示为在体积为1L的恒容容器中,投入1molCH3OH,在碳酸钠催化剂作用下,经过5min反应,测得甲醇的转化率(X)与甲醛的选择性(S)与温度的关系(甲醛的选择性:转化的CH3OH中生成HCHO的百分比),回答下列问题: 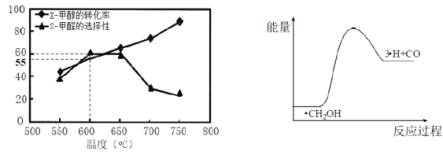 ①600℃时,5min内甲醛的反应速率为____________。 ②650℃-750℃甲醛选择性随温度下降,而甲醇转化率随温度升高的可能原因为________; ③700℃时,历程iii能量~反应过程如图所示,在答卷纸上绘制历程ii的“能量~反应过程”示意图。___________ II.室内甲醛超标会危害人体健康,通过传感器可以监测空气中甲醛的含量。一种燃料电池型甲醛气体传感器的原理所示,则工作电极的电极反应式为_____________。  |
|
| 22. | 详细信息 |
以黄铜矿(CuFeS2)、FeCl3和乳酸[CH3CH(OH)COOH]为原料可制备有机合成催化剂CuCl和补铁剂乳酸亚铁{[CH3CH(OH)COO]2Fe}。其主要实验流程如下: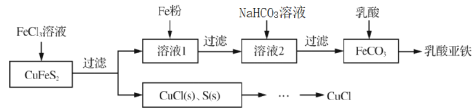 已知:①乳酸亚铁是绿白色晶体,溶于水,几乎不溶于乙醇。 ②CuCl为白色晶体,难溶于水和乙醇,在空气中易氧化;可与NaCl溶液反应,生成易溶于水的NaCuCl2。 ③NaCuCl2可水解生成CuCl,温度、pH对CuCl产率的影响如图所示。  (1)FeCl3溶液与黄铜矿发生反应的离子方程式为_______________。 (2)向溶液1中加入过量铁粉的目的是______________。 (3)下列有关实验说法不正确的是______________。(填编号) A.减压过滤使用的滤纸,为确保把所有的孔都覆盖住,应使滤纸大于布氏漏斗内径 B.为得到干燥的乳酸亚铁晶体,采用高温烘干的方式干燥 C.洗涤CuCl沉淀时,关小抽气泵,向布氏漏斗中加乙醇没过沉淀,并用玻璃棒搅拌 D.为得到较大的乳酸亚铁晶体颗粒,可投入几粒晶种并减缓溶液冷却速度 (4)若向NaHCO3溶液中加入FeSO4溶液,得到的FeCO3不纯,其原因是___________。 (5)用高锰酸钾标准液测定乳酸亚铁产品纯度,配制该标准溶液时,下列仪器中不必要用到的有_________。(用编号表示)。 ①电子天平 ②烧杯 ③量筒 ④玻璃棒 ⑤容量瓶 ⑥胶头滴管 ⑦移液管 下列操作会引起结果偏高的是____________(用编号表示)。 A.滴定前,滴定管和锥形瓶分别用标准液与待测液润洗 B.配制高锰酸钾溶液定容时,仰视刻度线 C.滴定前滴定管尖嘴内无气泡,滴定后尖嘴内有气泡 D.加待测液前锥形瓶内有少量水 E.滴定前俯视读数,滴定后仰视读数 (6)由CuCl(s)、S(s)混合物提纯CuCl的实验方案为:将一定量的混合物溶于饱和NaCl溶液中,_______。(需要用到下列所有操作,给出正确的顺序) ①滤液加热至60℃左右 ②趁热过滤 ③过滤 ④用乙醇洗净所得固体 ⑤滴加加0.1mol·L-1H2SO4至pH为2.0~2.5 ⑥置于真空干燥箱中干燥 |
|
| 23. 推断题 | 详细信息 |
吡喹酮(H)是一种治疗血吸虫病的药物,合成路线如下图所示: 已知:i  (1)下列说法正确的是______________。 A.1molC最多消耗2molH2 B.可以用双缩脲鉴别H与F C.化合物E、F均可发生消去反应 D.化合物H的分子式为C19H24N2O2 (2)试剂a的结构简式______________,E→F的反应类型为______________。 (3)D→E的化学方程式是__________________________________________。 (4)写出同时符合下列条件的C的所有同分异构体的结构简式______________。 ①分子中有苯环而且是苯环的邻位二取代物; ②1H-NMR谱表明分子中有6种氢原子;IR谱显示存在碳氮双键(C=N)。 (5)G→H三步反应依次为氧化、加成、取代反应,则G→H的合成路线为:______________。 |
|
高中化学 试卷推荐
- 2015-2016年高一上半期化学期中考试在线测验(广东省深圳市翠园中学)
- 2016-2017年高二上册期中考试化学考试(河北省邯郸市)
- 邯郸市高三化学2019年前半期月考测验在线答题
- 高中化学人教版 必修1 第二章 化学物质及其变化 3.氧化还原反应 氧化还原反应
- 长沙市高一化学月考测验(2018年后半期)带答案与解析
- 2018年至2019年高二上册联考化学在线测验完整版(广东省肇庆市香山中学孔子中学汉台中学三校)
- 2017-2018年高二上学期第三次月考化学考卷带参考答案和解析(江西省南昌市第二中学)
- 高中化学人教版 必修1 第三章 金属及其化合物 2.几种重要的金属化合物 铁的重要化合物
最近更新



